
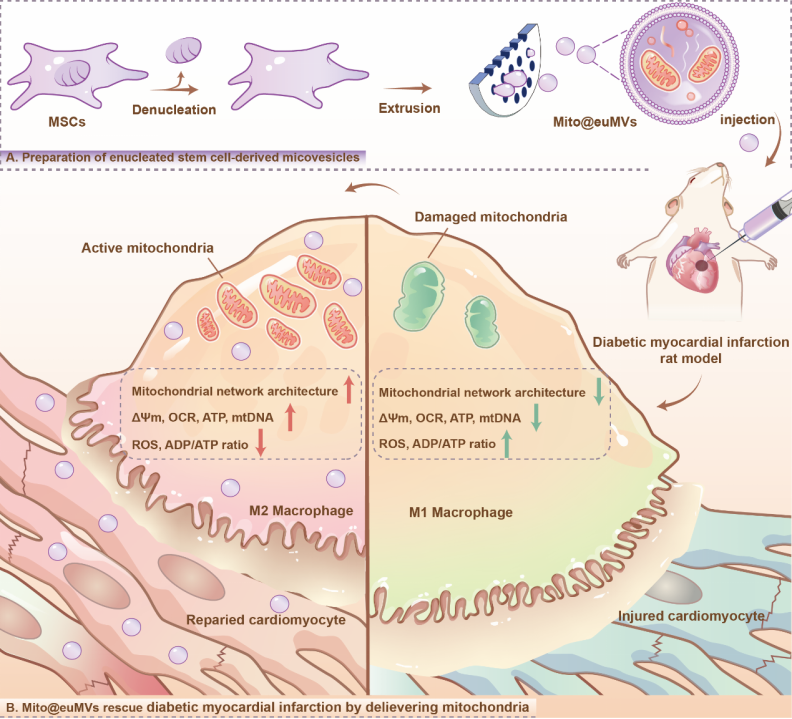
Schematic illustration of enucleated MSC-derived microvesicles containing mitochondria (Mito@euMVs) facilitate diabetic myocardial infarction repair by delivering mitochondria to macrophages.
糖尿病与心肌梗死的发生和预后密切相关。然而,目前的治疗策略主要集中于处理心肌梗死本身,常常忽视了糖尿病标志性特征高血糖的有害影响。高血糖破坏了巨噬细胞从M1表型向M2表型的关键转换,从而加剧了心肌梗死诱导的组织损伤并阻碍心肌修复。线粒体已成为巨噬细胞表型的关键调节因子,这提示了通过线粒体递送调控巨噬细胞的潜力。在本研究中,采用脂质体挤压技术,开发了源自去核间充质干细胞的、含有活性线粒体的微囊泡(Mito@euMVs)。通过粒径控制,本研究实现了71.7%的Mito@euMVs含有活性线粒体,且不存在核物质。体外实验表明,Mito@euMVs 可以被巨噬细胞高效内吞并将活性线粒体递送给巨噬细胞,改善巨噬细胞的线粒体网络结构与功能。更重要的是,本研究发现在高糖环境下,Mito@euMVs 也可以通过改善巨噬细胞的线粒体促进巨噬细胞从M1表型向M2表型转换。进一步使用糖尿病大鼠心肌梗死模型的体内研究证实了其心脏修复特性。在糖尿病大鼠心肌梗死后28天,Mito@euMVs治疗使射血分数提高了24.55±4.33%,短轴缩短率提高了15.48±4.04%,全面提升心功能。此外,Mito@euMVs减轻了梗死左心室壁变薄和纤维化。进一步研究发现,Mito@euMVs 可能通过增强 M2 巨噬细胞表型,降低心梗局部活性氧水平,进而减轻细胞凋亡与心肌肥大,保护心肌结构与细胞间通讯,促进血管新生,最终促进心肌修复。此项研究强调了通过Mito@euMVs进行线粒体递送可全面改善巨噬细胞线粒体功能,进而有效调控巨噬细胞表型,并突显了其在治疗糖尿病合并心肌梗死方面的巨大潜力。
付晓玲教授课题组介绍:
面向重要生命器官损伤修复与功能重建这一重大临床需求,聚焦于心血管、皮肤及骨组织修复的瓶颈问题,从关键病理特征出发,依托生命科学与材料科学、制造科学等的交叉与融合,通过材料的理性设计与合成、干细胞细胞/干细胞衍生物的工程化构建等手段,开发生物适配组织修复新材料/技术。研究方向:组织修复材料、干细胞治疗。研究成果:近年来在包括The Proceedings of the National Academy of Sciences (PNAS)、Advanced Functional Materials、Advanced Science、Biomaterials、Acta Biomaterialia、J Materials Chemistry B等国际著名杂志发表SCI收录论文二十余篇。承担包括国家自然科学基金、广东省科技项目、广州市科技项目等多项国家级、省部级科研基金。