国家人体组织功能重建工程技术研究中心王迎军院士团队王琳研究员、郝丽静副研究员与重庆医科大学附属第二医院楚磊副主任医师,在《Advanced Materials》期刊(IF=25.90)发表了一篇题为“3D Printed Titanium Scaffolds with Bi-Directional Gradient QK-Functionalized Surface”的研究论文。

由于其优异的生物相容性和耐腐蚀性,钛及其合金在临床实践中被广泛用作骨科植入物,特别是用于修复因创伤、感染、肿瘤和先天性骨骼异常引起的骨缺损。最近出现的3D打印技术通过构建复杂的形状和多孔结构,成功地解决了传统钛骨科植入物的局限性。这种可控的成型能力允许个性化的维修解决方案,而可控的多孔结构有助于与骨组织的弹性模量匹配,以防止应力屏蔽并为组织向内生长提供空间,确保卓越的骨整合。目前,越来越多的3D打印技术,包括选择性激光烧结(SLS)、熔融沉积建模(FDM)、立体光固化成型(SLA)和3D绘图(3DP),被用于开发各种类型的钛骨科植入物,例如人工关节和椎间融合装置。
然而,临床反馈表明,3D打印多孔钛植入物内的组织向内生长通常非常有限,通常只有几毫米。会显著增加植入物松动、感染和失效的概率,进而严重影响植入物在体内的长期使用稳定性。导致此问题的主要因素之一是钛的生物惰性表面,这给在多孔3D打印植入物内部诱导血管形成提出了挑战。血管形成被认为是促进骨结合的关键因素。这个过程涉及新血管的形成,这些血管有助于将必需的氧气、营养物质和信号分子输送到植入物和骨骼之间的界面。这反过来又促进了成骨细胞向植入物表面的迁移和增殖,从而产生富含胶原蛋白的基质,使植入物矿化并形成骨组织。在缺乏足够的血管形成的情况下,植入物容易被纤维组织包覆,阻碍骨骼向内生长并增加植入物失败的风险。因此,促进血管形成对于促进骨结合和确保植入物的长期稳定性至关重要。
本研究使用3D打印和梯度表面策略创建了一个模块化多孔钛支架,以双向梯度分布将QK肽固定在表面上。这种设计的特点是内部肽密度高,两端肽密度低,旨在诱导细胞从末端迁移到内部,从而增强支架内的血管形成和骨整合。
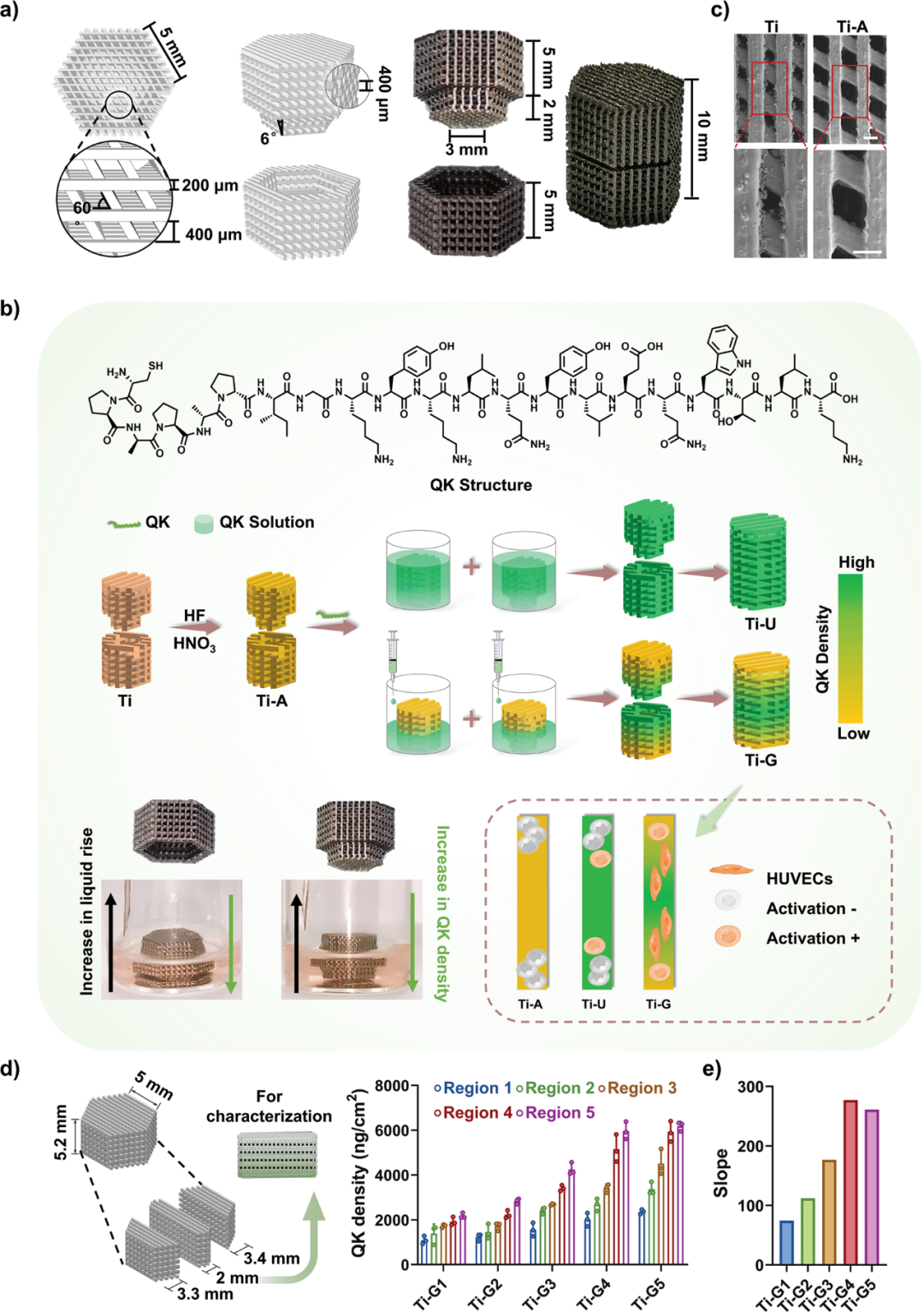
图1. 具有双向梯度QK功能化表面的3D打印模块化支架的制备和表征
研究团队采用3D打印技术制备了模块化钛支架,该植入物由上、下两部分通过凸凹结构组装而成(图1a),形成中间高密度、末端低密度的QK梯度分布(图1b)。SEM分析显示,酸蚀处理(Ti-A)使支架表面变得光滑(图1c)。随后,团队通过巯基-羟基反应将QK肽固定在支架各部分。为研究梯度效应,选用5.2mm高的无连接结构多孔支架(图1d)。荧光检测表明,Ti-G系列样品的MFI和QK密度均随区域数增加而升高,其中Ti-G4表现出最显著的梯度变化(图1e)。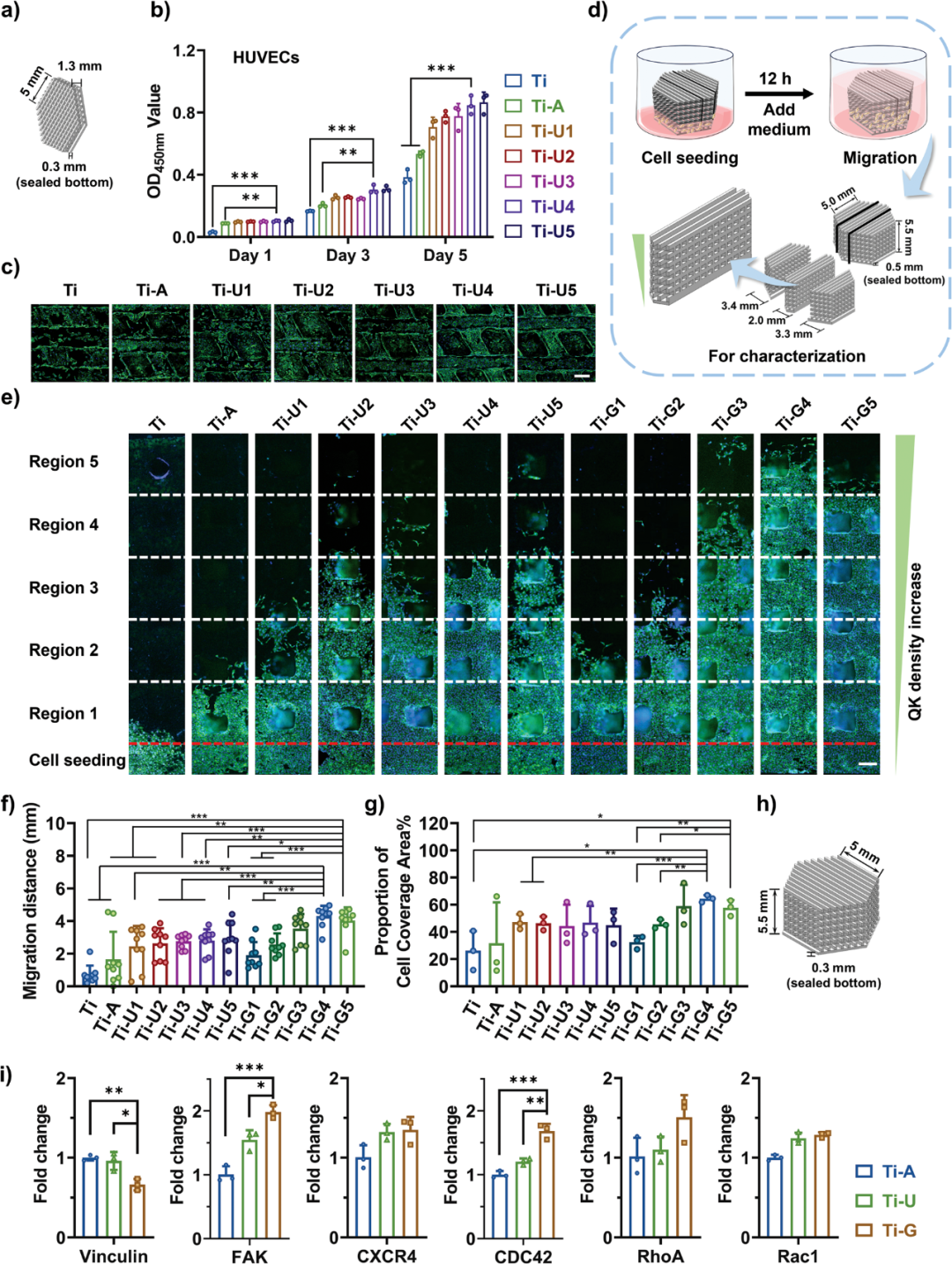
图2. 功能化支架的体外细胞测定
研究团队采用底部密封(0.3mm)和顶部多孔(1mm)的复合结构设计(图2a),通过梯度QK修饰(Ti-U1至Ti-U5)显著提升了植入物性能。实验表明酸蚀处理(Ti-A)较原始Ti显著改善细胞相容性;梯度修饰的Ti-G4组展现出最优异的细胞迁移性能,其迁移距离可达区域5,qRT-PCR证实该组通过调控Vinculin、FAK等基因表达有效促进细胞迁移(图2d-e,h-i)。这为优化植入物表面改性提供了重要依据。
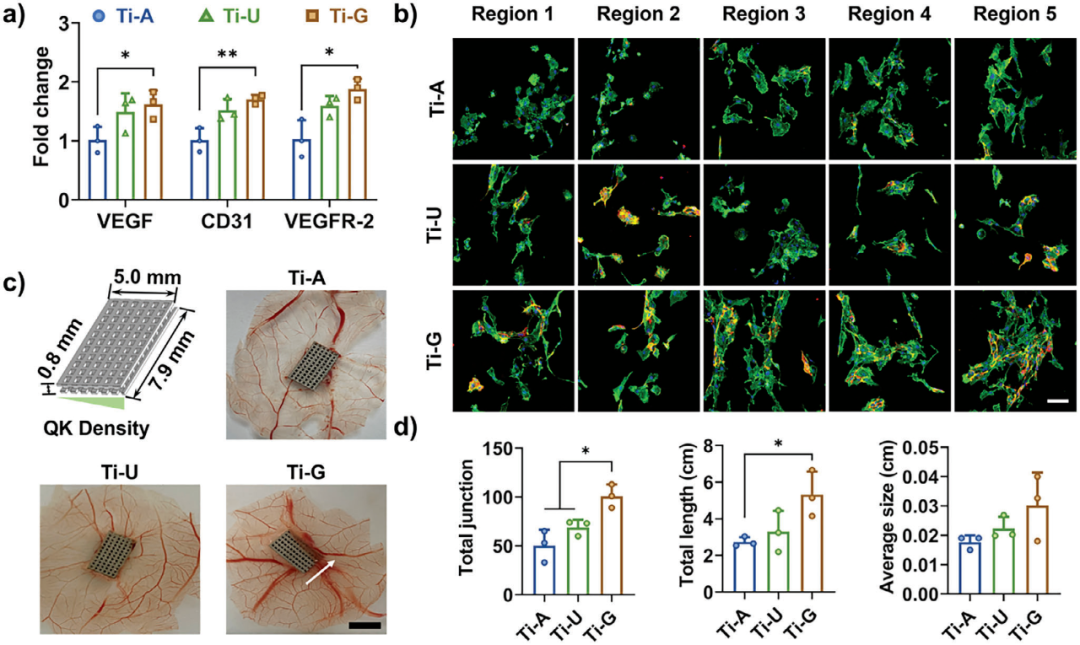
图3. 具有QK功能化梯度表面的3D打印植入物的体外血管生成
 图4. 通过新西兰白兔节段性骨缺损模型对支架进行体内测定
图4. 通过新西兰白兔节段性骨缺损模型对支架进行体内测定研究团队通过兔桡骨模型评估植入物的体内性能。30天后组织学分析显示:Ti-A组血管和新骨主要分布于植入物两端,内部极少(图4b);Ti-U和Ti-G组则显著促进支架内部血管化,尤其在Ti-G组最内层也观察到大量新生骨组织(图4c)。H&E染色证实Ti-G组组织向内生长最显著(图4d-e),并含有更多成熟骨组织(图4f-g)。显微CT显示三组表面均有新骨形成,但仅Ti-G组在中央区域呈现显著骨长入(图4h),证实梯度修饰可协同促进血管化和成骨。
 图5.植入90天后绵羊脊柱修复模型中支架的体内测定
图5.植入90天后绵羊脊柱修复模型中支架的体内测定
结论:在这项研究中,研究团队开发了一种模块化支架,其功能化表面具有QK(Ti-G) 的双向梯度分布。该设计旨在将生物活性与QK的梯度分布协同结合,以促进细胞向内部迁移并促进增强的血管形成。与Ti-A和Ti-U的对照组相比,观察到支架内促进的血管生成,使Ti-G在修复节段性骨缺损和脊柱缺损时与周围组织形成紧密结合的结构。这种双向梯度的概念代表了增强肽功能化表面生物活性的有效策略,并为各种 3D 打印支架具有重要前景。
