国家人体组织功能重建工程技术研究中心宁成云教授、广东食品药品职业学院翟锦霞博士、华南农业大学王珍高副教授、在Bioactive Materials(IF=20.3)杂志上发表了一篇题为《Zwitterionic multifunctional coatings with strong hydration for ureteral stents to inhibit infectious encrustation. 》的文章。

输尿管支架结垢是泌尿外科领域的重大临床挑战。在独特的泌尿系统生理环境下,输尿管支架面临尿盐沉积导致的结壳问题,这不仅破坏支架通畅性和功能持续性,还显著降低表面润滑性,增加取出难度。更关键的是,结壳与细菌感染形成双向恶性循环:粗糙表面促进细菌附着,而细菌代谢产物又加速矿物盐沉积,进一步加剧结壳。传统表面改性策略主要采用结晶抑制剂(如肝素、软骨素硫酸盐)或抗菌剂(金属离子、抗菌肽),但存在功能单一、长期稳定性差等局限。本研究基于水合层屏障机制,以两性离子聚合物SBMA为基础,在PU支架表面成功开发出一种多功能涂层(PU/ATS),为解决支架结垢问题提供了新思路。
分子动力学模拟揭示SBMA的抗结壳机制(图1)。径向分布函数分析显示,PU-pSBMA界面在0.28nm处出现g(r)峰值(9879.6),显著高于PU界面(3262.8),证实SBMA形成更致密的水合层。离子-表面相互作用能分析表明,结垢离子与PU表面表现为吸引能(E<0),而与PU-pSBMA表面呈现排斥能(E>0)。10ns模拟后,PU表面出现明显离子聚集,而PU-pSBMA表面几乎没有离子附着,这表明水合层作为一种能量屏障,阻挡并排斥靠近的结壳离子,从而减少了离子附着到表面的可能性。
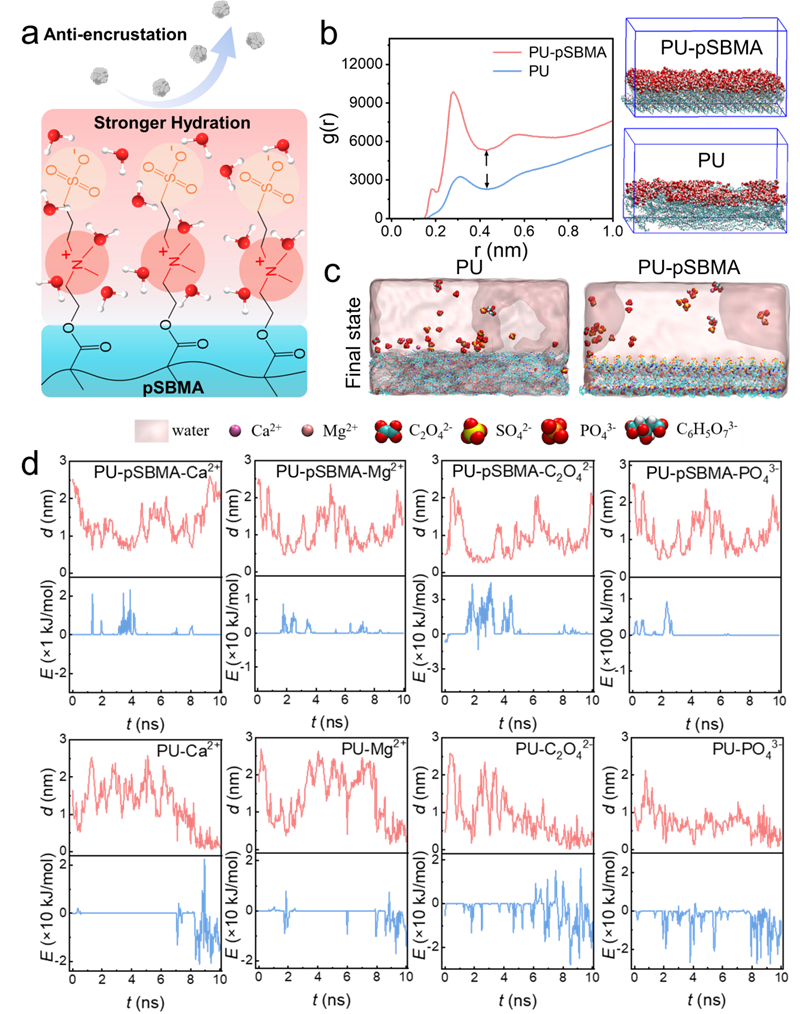
图1:水合层的抗结壳机制.(a)通过强水化作用实现抗结壳机制的示意图(b)PU/水和 PU-pSBMA/水界面的径向分布函数(g(r)),使用最后 10 纳秒的分子动力学模拟数据绘制;插图展示了平衡状态下的 PU-pSBMA/水和 PU/水界面的 3D 视图;红色珠子代表水合层内的水分子,截止距离为 g(r) 所示的谷值位置(黑色箭头)(c)人工尿液中结壳离子在 PU和 PU-pSBMA 表面的最终状态,离子在 PU 表面聚集并附着,而在 PU-pSBMA 表面未观察到附着现象(d)结壳离子(Ca2+、Mg2+、PO43−、C2O42−)与表面原子(PU 和 PU-pSBMA)之间随时间(t)的变化的最小距离(d)和总相互作用能(E)
基于分子动力学模拟结果,采用 SBMA、TMAPMA 和 AAm,我们设计了具有低(PU/ATS-1)、中(PU/ATS-2)和高(PU/ATS-3)SBMA 密度的多功能抗结壳涂层支架,以探究 SBMA 密度对支架性能的影响。涂层采用UV引发自由基聚合法结合浸涂技术制备。以丙烯酰胺(AAm)、SBMA和TMSPMA为单体,先在PU支架表面通过氧等离子体处理引入羟基,再吸附疏水引发剂BP,最后浸涂预聚液并UV固化。通过SEM、FTIR、XPS等手段表征涂层的形貌和化学结构(图2)。SEM显示涂层厚度均匀(15-20 μm),无界面分离;FTIR光谱在1670 cm-1(AAm的C=O)、1040 cm-1(SBMA的SO3-)和964 cm-1(TMSPMA的Si-O)处出现特征吸收峰。此外XPS检测到S2p和Si2p特征峰,这些都证实SBMA和TMSPMA成功引入。
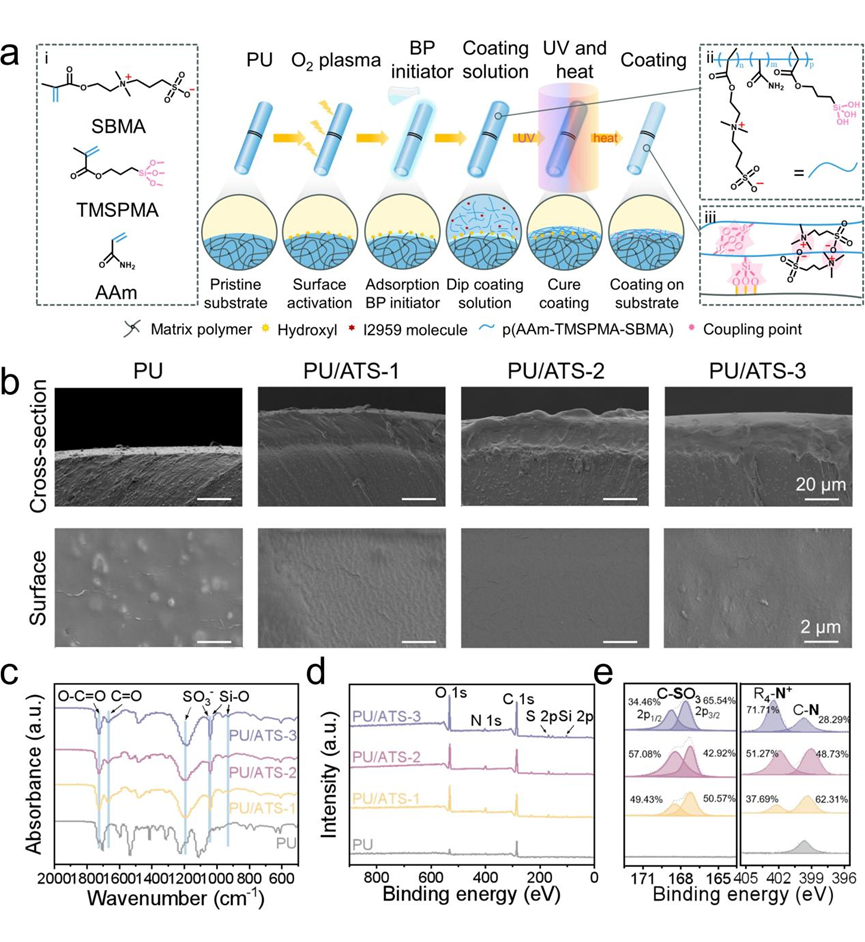
图2:PU/ATS的制备、形态及结构.(a)制备流程示意图,(i、ii)SBMA、TMSPMA 和AAm 的分子结构以及涂层溶液,(iii)聚合物交联方法和涂层与基底的粘附方式(b)横截面和表面扫描电子显微镜图像(c)傅里叶变换红外光谱(d)XPS 全谱图(e)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)的S2p和N1s的高分辨率XPS谱图
输尿管支架在植入和取出过程中与组织摩擦易引发患者疼痛。本研究开发的PU/ATS涂层通过两性离子聚合物SBMA与亲水单体AAm的协同作用,形成强效水合层,显著提升支架表面润滑性和亲水性(图3)。该涂层利用SBMA与AAm的协同作用,在37℃模拟临床环境中将摩擦系数从1.405显著降低至0.061(降幅达23倍),并展现出优异的润滑稳定性(50次循环测试后仍保持稳定)。同时,涂层赋予支架超亲水特性(接触角<5°),且六个月后仍维持此性能。机械性能上,涂层支架的断裂伸长率>300%,硬度维持在80 HA。在稳定性方面,依据GB/T 14233.1-2022标准进行提取实验,涂层在70°C水浸24 h后吸光度<0.15,pH变化<0.3;30天浸泡实验表明涂层无质量损失。这些数据证明PU/ATS兼具低摩擦、高亲水和长期稳定性。
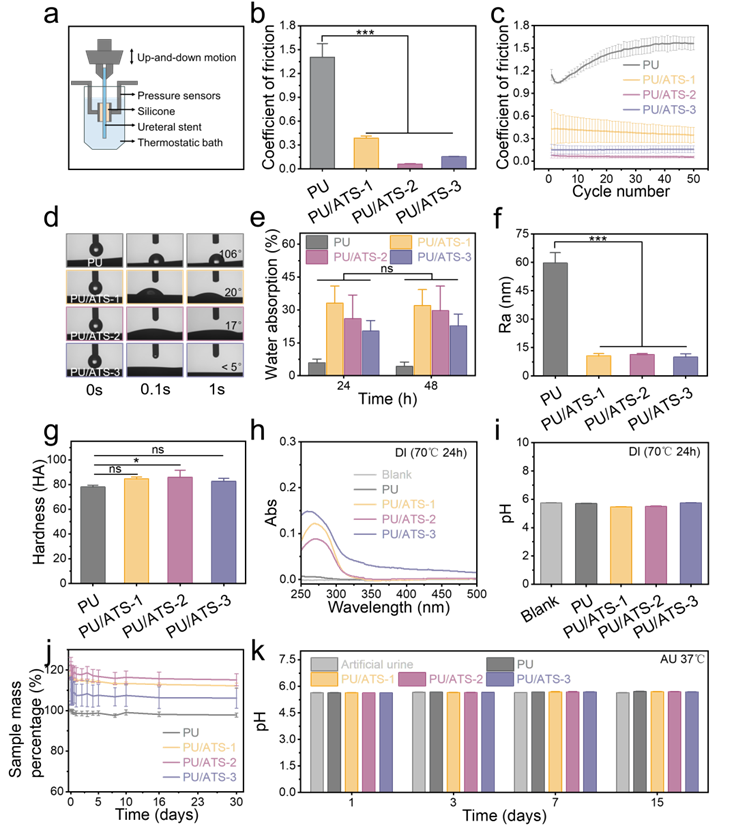
图3:PU/ATS 的润滑性、亲水性和稳定性.(a)输尿管支架滑动摩擦测试的示意图(b)摩擦系数以及(c)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)在 50 次循环后的平均摩擦系数值(d)接触角(e)吸水率(f)粗糙度,以及(g)硬度,这些数据均来自PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)(h)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)在 70℃的去离子水中浸泡 24 小时后的紫外-可见光谱和 pH 测量值(i)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)在37 ℃的水中不同浸泡时间后的残留质量百分比(j)在 37 ℃的水中不同浸泡时间后,PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)的残留质量百分比(k)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)在人工尿液中的 pH 值,在不同的浸泡时间段内变化情况.
通过建立体外动态尿流模型模拟人体尿液环境,系统评估了不同SBMA密度涂层对矿物盐附着的抑制效果(图4)。实验结果显示,PU/ATS-3在30天和90天的测试中分别实现96.1%和83.5%的结壳抑制率,表现出最优异的抗结壳性能。扫描电镜观察显示无涂层PU表面出现大量钙磷结晶聚集,而PU/ATS-3表面仅零星分布少量晶体。ICP元素分析进一步证实涂层表面Ca2++Mg2+沉积量从142.4μg/cm²(无涂层PU)降至5.5μg/cm²,DSC测试揭示其高结合水含量是形成有效水合屏障的关键因素。此外,还对支架在模拟结壳前后的摩擦系数进行表征。经过30天后的模拟结壳,所有涂层样品的摩擦系数均低于无涂层PU,且PU/ATS-3在结壳后仍保持了其原始的润滑性能。
 图4:PU/ATS 在体外动态尿流模型中的抗结壳评估.(a)体外动态尿流模型的示意图(b)SBMA 密度对结壳矿物质盐附着影响的示意图(c)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)在动态尿液流动模型中30 天后的实物图、代表性SEM以及对应的 EDS 元素图(Ca:蓝色,P:红色)(d)表面的 Ca2+和 Mg2+的总离子含量(e)涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)中的自由水和结合水的比例(f)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)结壳前后的摩擦系数(g)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)摩擦系数的平均值
图4:PU/ATS 在体外动态尿流模型中的抗结壳评估.(a)体外动态尿流模型的示意图(b)SBMA 密度对结壳矿物质盐附着影响的示意图(c)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)在动态尿液流动模型中30 天后的实物图、代表性SEM以及对应的 EDS 元素图(Ca:蓝色,P:红色)(d)表面的 Ca2+和 Mg2+的总离子含量(e)涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)中的自由水和结合水的比例(f)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)结壳前后的摩擦系数(g)PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)摩擦系数的平均值
尿路感染也是输尿管支架植入后的主要并发症之一。细菌感染,尤其是奇异变形杆菌的感染,也会促进支架结壳的形成。因此抑制细菌对支架表面的粘附对于预防感染和结壳至关重要。在本研究中,选用三种常见尿路感染菌株(大肠杆菌、金黄色葡萄球菌、奇异变形杆菌)进行抗菌粘附实验(见图5)。菌落计数结果表明,PU/ATS-3对三种菌的粘附抑制率分别达到98.69%、92.82%和89.27%。支持信息中,扫描电镜观察也证实了无涂层PU、PU/ATS-1、PU/ATS-2和PU/ATS-3支架表面粘附细菌数量的逐渐减少。总而言之,PU/ATS-3、涂层由于具有强大的水合层表现出卓越的抗细菌黏附性能。
为了比较评估,我们选用市售的Bard® InLay Optima®支架作为对照组。经过30天的模拟感染性结壳后,PU/ATS涂层支架在对抗结壳方面仍然有效。体式显微镜图像显示,无涂层PU支架表面覆盖了大量结壳,而PU/ATS-3表面仅有少量结壳。随后,我们通过ICP定量测定了支架表面的Ca2+、Mg2+离子含量,PU/ATS-3表面的总离子含量最低。
通过大鼠膀胱植入模型进行28天体内实验,PU/ATS在非感染和感染条件下分别实现99.6%和86.7%的结壳抑制率。SEM和EDS结果显示PU支架表面覆盖大量结壳,而涂层支架保持光滑。组织学分析证实主要器官(心、肝、脾、肺、肾、膀胱、输尿管)未出现炎症、坏死或纤维化改变,H&E染色显示膀胱组织形态完整,涂层组在感染条件下仅见轻微黏膜炎症,显著优于PU。这进一步证实了PU/ATS涂层支架在抑制结壳形成方面的显著优势。
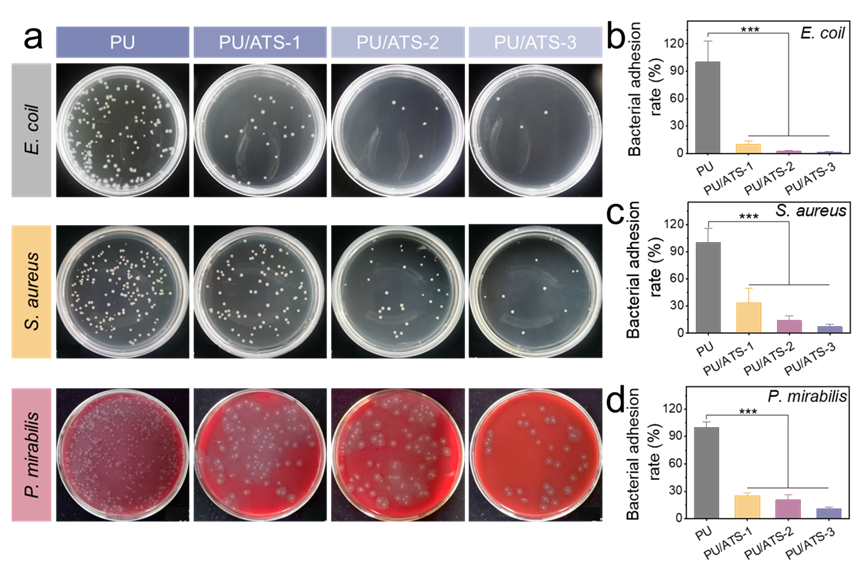
图5:PU/ATS 在体外的抗菌黏附活性.(a)琼脂平板照片以及(b)大肠杆菌、(c)金黄色葡萄球菌和(d)奇异变形杆菌在PU和涂层样品(PU/ATS-1、PU/ATS-2、PU/ATS-3)上的细菌黏附率
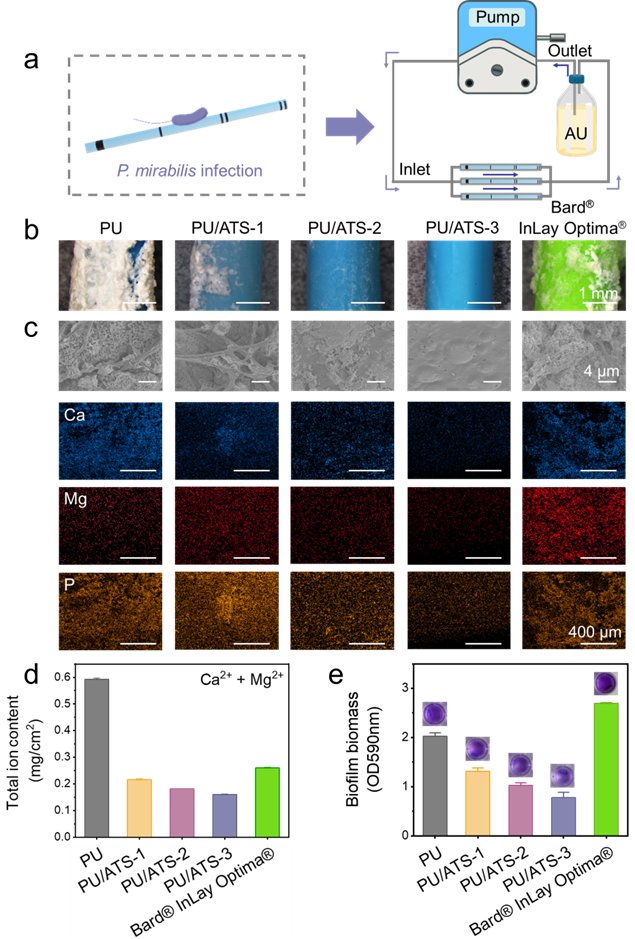
图6:30 天的体外动态尿流感染模型中抗结壳实验.(a)动态尿流流动感染模型支架的示意图(b)30 天后PU、PU/ATS-1、PU/ATS-2、PU/ATS-3 和商业Bard® InLay Optima® 支架上的结壳情况(c)代表性的扫描电子显微镜图像及相应的能谱元素图(钙:蓝色,镁:橙色,磷:红色)显示了结壳情况(d)在动态尿流感染模型中 30 天后PU、PU/ATS-1、PU/ATS-2、PU/ATS-3 和商业Bard® InLay Optima® 支架上钙离子和镁离子的总离子含量(e)动态尿流感染模型中 30 天后PU、PU/ATS-1、PU/ATS-2、PU/ATS-3 和商业Bard® InLay Optima® 支架上的生物膜含量
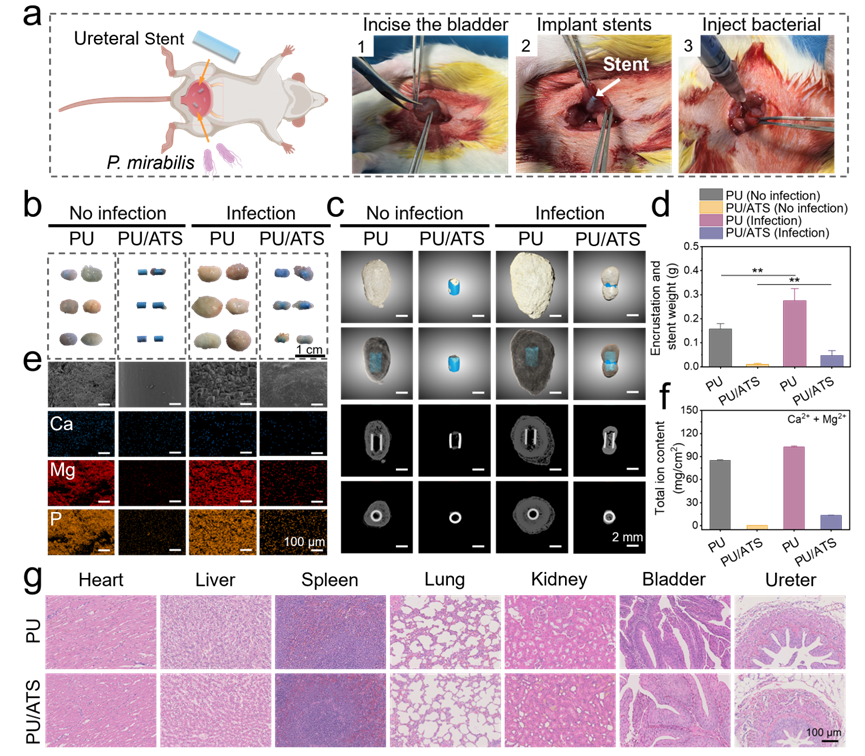
图7:体内抗结壳性能.(a)动物模型及手术流程示意图(b)实物图以及(c)在体内非感染和感染两种情况下PU和PU/ATS支架上结壳的高分辨X射线3D显微镜图像(d)结壳重量(e)结壳SEM/EDS图像以及(f)在非感染和感染两种情况下PU和PU/ATS支架的总结壳离子含量(g)在非感染条件下大鼠主要器官(心脏、肝脏、脾脏、肺、肾、膀胱和输尿管)的 H&E 染色图像
本研究成功开发基于两性离子聚合物SBMA的多功能涂层,通过强水合层机制有效抑制输尿管支架结壳。系统实验证实涂层在体外和体内均表现出优异抗结垢、抗菌性能和生物相容性。该策略为尿路医疗器械表面改性提供了新范式,具有重要临床应用前景。
