
M-BiNanoAb由功能化磁性纳米颗粒、抗CD3抗体(aCD3)和抗PD-L1抗体(aPDL1)通过超分子作用组装而成。静脉注射后,它像一枚“智能磁钉”,能精准识别并锚定在血液循环中的CD3+ T细胞表面。如此一来,无需复杂的体外基因工程、细胞培养和回输流程,直接在体内“就地生产”出功能完备的“仿CAR-T细胞”. aCD3 模拟了传统CAR结构中的胞内信号域,激活T细胞,将其转化为具备攻击能力的效应细胞。aPDL1 模拟了传统CAR结构中的胞外抗原识别域,使被改造的T细胞能够特异性识别并靶向高表达PD-L1的肿瘤细胞。
传统CAR-T细胞在实体瘤中浸润不足。M-BiNanoAb携带的磁性纳米颗粒赋予了这些“仿CAR-T细胞”磁响应能力。在肿瘤部位施加外部磁场,可以像“导航”一样,主动引导大量工程化T细胞克服血流剪切力和组织屏障,定向迁移并富集到肿瘤内部,显著提升瘤内杀伤细胞的密度。
aPDL1不仅用于识别肿瘤细胞,还能阻断PD-1/PD-L1这一关键的免疫抑制通路。这相当于在武装T细胞的同时,还为其清扫了战场上的主要障碍,有效缓解了T细胞在免疫抑制微环境中的功能耗竭,让其保持持久的战斗力。
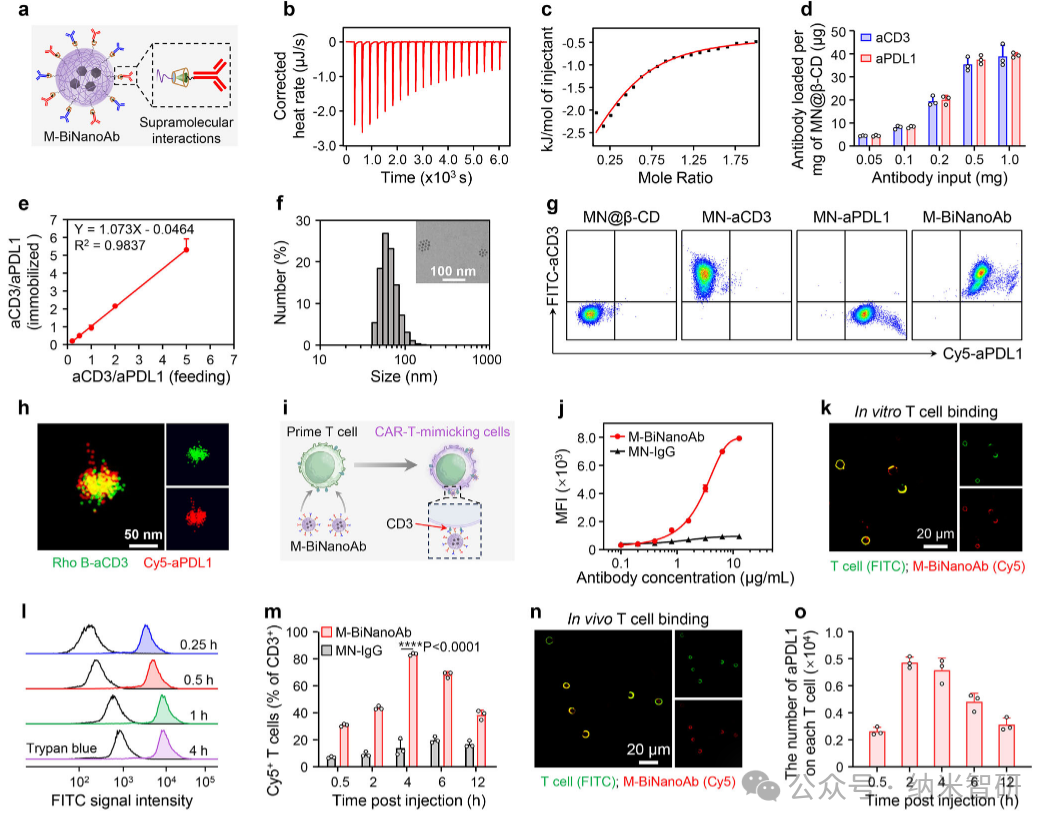
图1.
首先,作者证明M-BiNanoAb通过超分子作用成功负载双抗体,能高效结合T细胞并在体内快速生成仿CAR-T细胞。
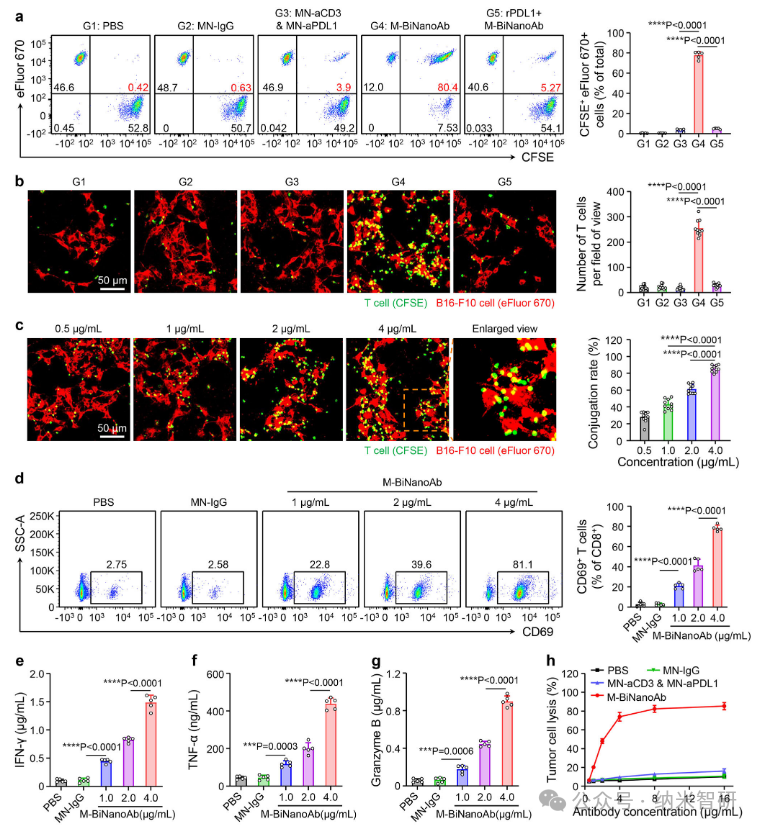
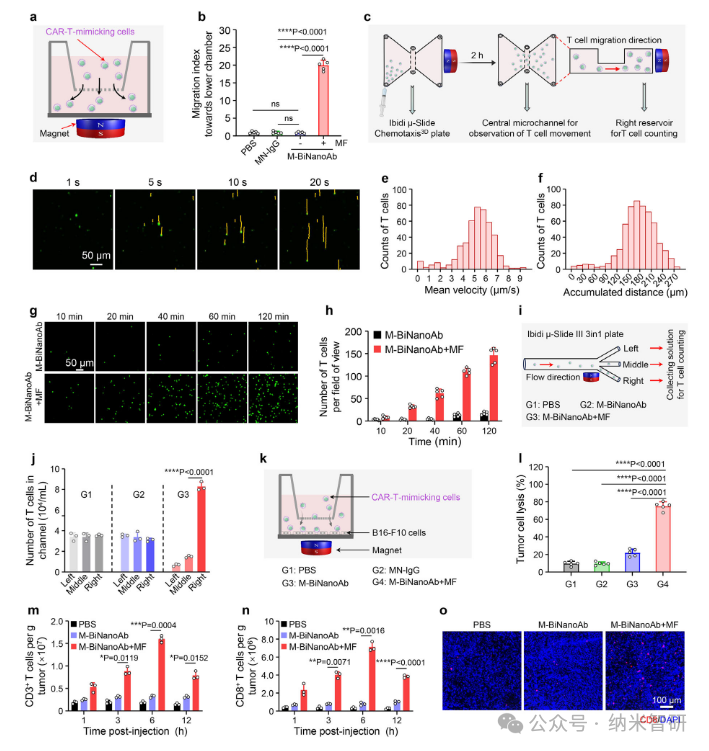
图2.
其次,M-BiNanoAb工程化的仿CAR-T细胞能特异性识别肿瘤细胞,激活并释放细胞因子,展现出强大的体外杀伤能力。

图3.
接下来,在磁场引导下,仿CAR-T细胞可实现定向迁移,增强肿瘤浸润,并在体内模型中显著提升瘤内T细胞数量。
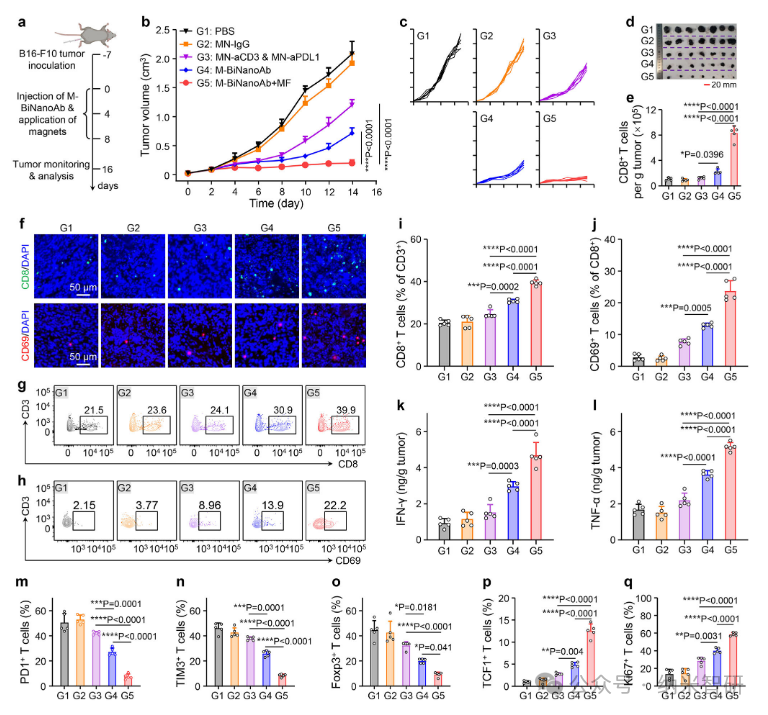
图4.
随后,在B16-F10黑色素瘤模型中,磁导航M-BiNanoAb治疗展现出超过90%的肿瘤抑制率,并改善瘤内T细胞功能与亚群分布。
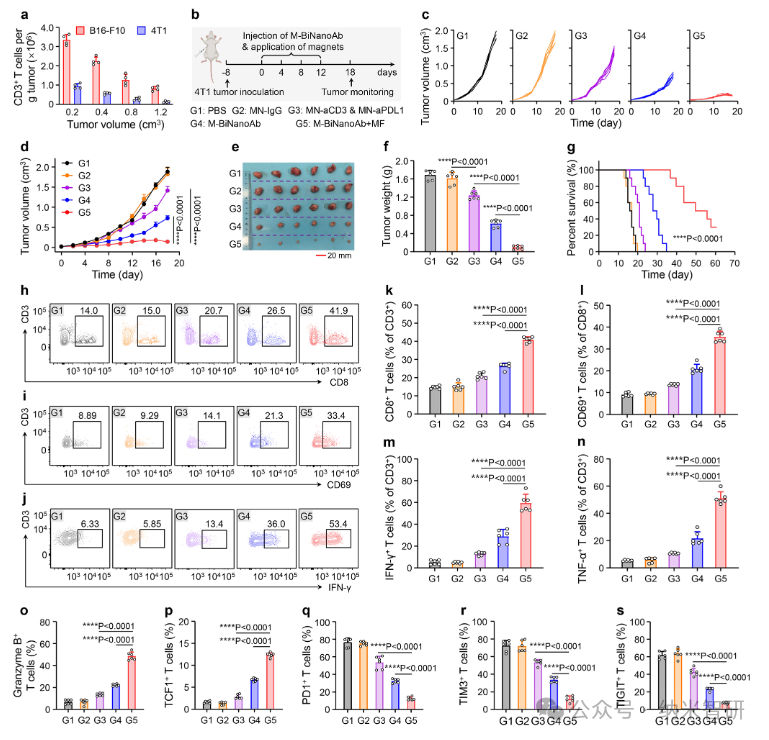
图5.
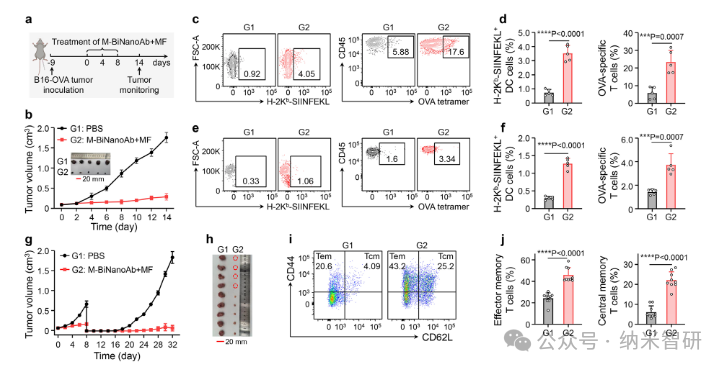
图6.
接着,在4T1“冷肿瘤”模型中,M-BiNanoAb联合磁场治疗同样显著抑制肿瘤生长,延长生存期,并重塑肿瘤免疫微环境。
最后,磁导航仿CAR-T细胞不仅能直接杀伤肿瘤,还能引发抗原表位扩散并建立长效免疫记忆,抵抗肿瘤再挑战。
总之,作者为实体瘤的CAR-T治疗提供了一条更简单、更安全、更有效的全新思路,是纳米技术与免疫治疗深度融合的典范,标志着我们向着攻克实体瘤的目标又迈出了坚实的一步。
