国家人体组织功能重建工程技术研究中心边黎明教授课题组在Journal of the American Chemical Society(IF=15.6)杂志上发表了一篇题为《A Tunable Coacervate Matrix Emulates Embryonic Extracellular Matrix(ECM) Biophysical Cues To Regulate Stem Cell Fate》的文章。

胚胎发育的机械信号调控与体外模拟挑战。
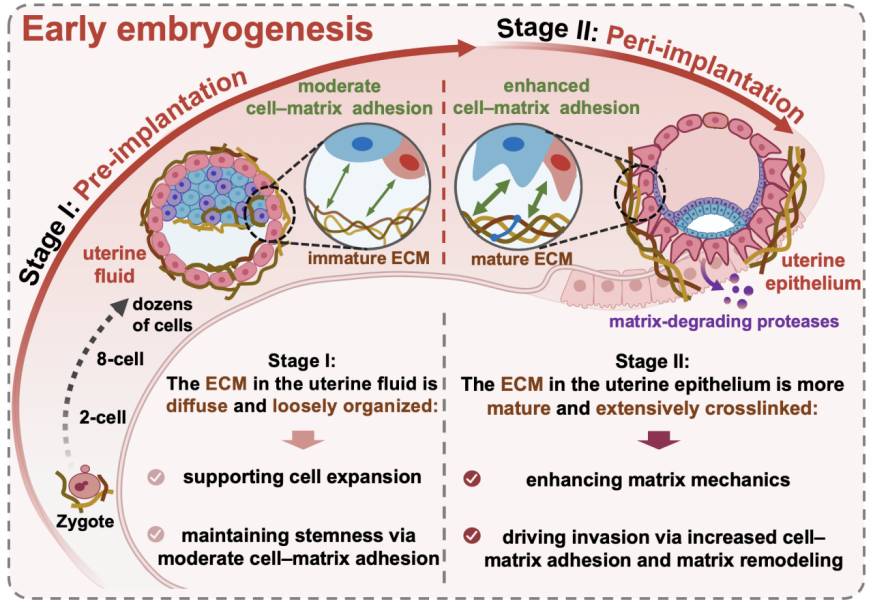
在胚胎早期发育过程中,子宫环境的生物物理信号(如细胞外基质ECM的力学特性)对细胞命运具有重要调控作用:着床前阶段,子宫液中的ECM呈现松散、动态的未成熟结构,支持受精卵从单细胞扩增为数十个细胞的囊胚,并维持内细胞团的干性;着床阶段,囊胚接触的子宫上皮ECM转变为高度交联的成熟基质,其硬度显著增加,诱导滋养层细胞通过增强粘附及分泌基质降解酶实现侵入行为,从而启动营养交换。
然而,在体外模型中复现上述阶段特异性ECM微环境仍面临挑战。传统明胶涂层二维基质因粘附过强易损害胚胎细胞干性维持;三维水凝胶支架则因网络结构过于静态,无法模拟着床前ECM的类流体动力学特性,同时可能限制细胞团簇的生长与收集。
文章要点:基于凝聚层的相变设计与功能实现
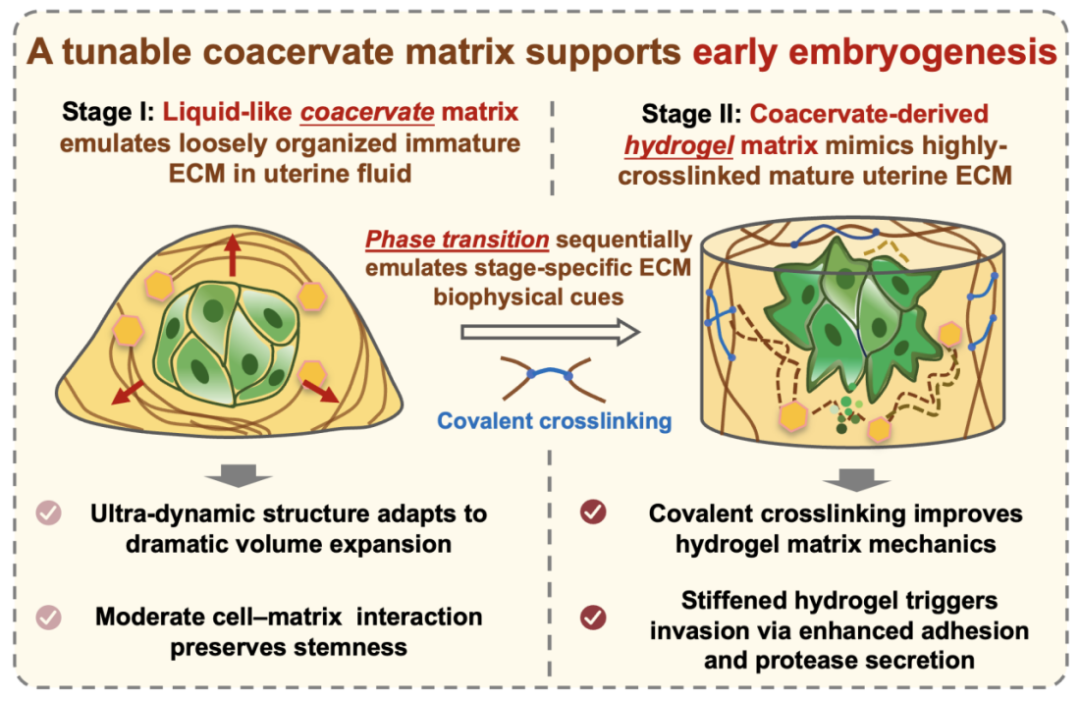
本研究开发了一种基于明胶的凝聚层系统,其通过疏水修饰的明胶分子在水相中自组装形成液相凝聚层,并具备相变介导的可调力学特性。该系统通过凝聚体相和凝胶相两种相变行为模拟胚胎发育不同阶段的ECM微环境:
1. 凝聚体相模拟着床前ECM:疏水作用驱动的可逆交联赋予基质类液体超动态结构,支持胚胎干细胞团簇的快速体积扩张,并通过适度的细胞-基质相互作用维持干性。
2. 水凝胶相模拟着床期ECM:通过共价交联,凝聚层可转变为硬度提升的水凝胶网络。封装其中的干细胞感知硬度变化后,表现出增强的粘附能力及基质降解酶分泌,模拟滋养层的侵入性表型。
该凝聚层系统通过简单的化学修饰与相变控制,实现了对胚胎发育早期ECM生物物理线索的时序性模拟,为研究干细胞命运调控提供了新工具。
该工作以“A Tunable Coacervate Matrix Emulates Embryonic Extracellular Matrix (ECM) Biophysical Cues To Regulate Stem Cell Fate”为题发表在《Journal of the American Chemical Society》上。文章第一作者为谢宪博士,现担任香港城市大学研究助理教授,以及闫旭博士,现为北京大学深圳医院骨关节科-北医三院联合培养博士后,从事牵张成骨的力学生物学机制和力学信号调控干细胞命运机制的研究。文章共同通讯作者为香港大学医学院林思恩教授与华南理工大学国家人体组织功能重建工程技术研究中心边黎明教授。
边黎明教授2021年获聘教育部长江学者特聘教授,为华南理工大学国家人体组织功能重建工程技术研究中心固定人员。边教授长期致力于发展先进纳米材料与水凝胶材料在生物医学领域的应用,并且逐渐建立了从基础材料学,生物医学研究到医疗应用研究的多方向的深度研究。边教授课题组近期在高水平学术期刊发表多篇论文,相关详细内容可查阅边教授实验室网站:https://www.x-mol.com/groups/bian_lab
