国家人体组织功能重建工程技术研究中心付晓玲教授课题组在ACS Nano(IF=16.5)杂志上发表了一篇题为《Fusogenic Hybrid Gelled Nanovesicles Combining Mesenchymal Stromal Cell Cargo with Cholesterol-Modified Macrophage Membranes for Targeted Myocardial Infarction Therapy》的文章。

心肌梗死(MI)是一种由血管栓塞引起的,具有高发病率和高死亡率的缺血性心脏病。目前,经皮冠状动脉介入治疗(PCI)是临床上恢复梗死心肌血流供应的主要方式,然而,常规介入手段只能通过延阻血管闭塞来缓解缺血症状,无法恢复受缺血影响的周围组织的再生以及功能重塑,且副作用在一定程度上限制了适用人群。工程化间充质干细胞衍生微囊泡具有促进血管新生,调节免疫平衡,改善机体局部微环境等功能,在心血管疾病的临床治疗中具有良好的应用前景。但传统工程化衍生微囊泡在制备过程中仍面临内容物损失严重,质膜结构易氧化,生物安全性风险以及递送效率低等挑战。针对上述问题,付晓玲教授团队构建了一种多功能的间充质干细胞衍生的杂化凝胶纳米囊泡,通过模块置换的方式将功能化修饰的巨噬细胞膜与干细胞内容物系统整合,以用于心肌梗死的靶向治疗。
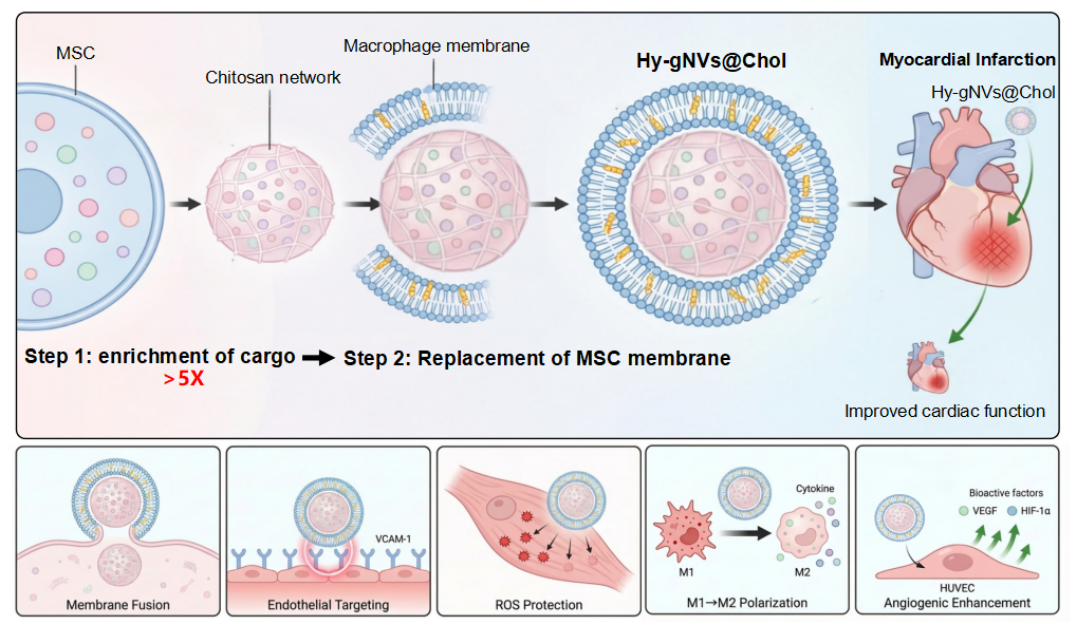
在本研究中,通过模块置换的方式对间充质干细胞纳米囊泡的膜结构进行了功能化修饰及替换,开发了一种兼具炎症靶向和高活性内容物含量的杂化间充质干细胞衍生纳米囊泡Hy-gNVs@chol。利用壳聚糖(CS)与带负电分子之间的静电吸附作用高效富集蛋白质等间充质干细胞活性物质并自组装形成蛋白凝胶颗粒,其有效成分的含量较常规制备方法得到的普通微囊泡提升了5倍以上。在颗粒表面包裹胆固醇修饰的巨噬细胞膜赋予其炎症靶向能力的同时克服了干细胞潜在的凝血风险。此外,胆固醇能够促进细胞内吞过程中膜融合的发生,从而进一步提升靶细胞摄取效率,并避免自身被溶酶体吞噬清除。通过尾静脉注射将Hy-gNVs@chol应用于心肌梗死模型中,纳米囊泡经长效血液循环后能够高效主动的积累在损伤心肌内,展现出良好的促血管生成和炎症抑制效果,减少了左心室壁变薄和纤维化的形成,显著恢复受损心脏的各项生理功能。
综上所述,Hy-gNVs@chol在心肌梗死的治疗中展现了突出的应用潜力,同时也为工程化干细胞衍生微囊泡的设计与优化提供了新思路。
该工作以“Fusogenic Hybrid Gelled Nanovesicles Combining Mesenchymal Stromal Cell Cargo with Cholesterol-Modified Macrophage Membranes for Targeted Myocardial Infarction Therapy”为题发表在《ACS Nano》上。文章第一作者为华南理工大学生物医学科学与工程学院2022级生物医学工程专业博士研究生刘闯,文章的通讯作者为华南理工大学国家人体组织功能重建工程技术研究中心付晓玲教授。
