国家人体组织功能重建工程技术研究中心边黎明教授课题组在 Nature Communications(IF=15.7)杂志上发表了一篇题为《Mechanically heterogeneous hydrogel with cell-programmed network restructuring promotes tissue regeneration by mechano-epigenetic modulation》的文章。

在骨修复过程中,细胞外基质(ECM)的生物物理信号对干细胞命运同样具有关键的调控作用:早期骨修复阶段,间充质干细胞所处的ECM呈现松散交联、力学均质的未成熟结构,支持细胞的快速增殖与团簇扩张,并为后续分化储备必要的细胞数量;随着发育进程推进,ECM因细胞分泌的酶(如碱性磷酸酶)介导的分子聚集与交联而逐渐成熟,形成包含刚性胶原纤维与柔软多糖基质的复杂异质结构,其局部刚度显著增加,诱导干细胞通过增强力学感知与粘附实现向成骨细胞谱系的分化,从而启动骨基质沉积与矿化。然而,如何在体外模型中复现上述阶段特异性的ECM动态演变仍面临挑战。传统预成型水凝胶支架因结构静态、无法响应细胞行为而难以模拟发育过程中ECM的时序性重塑;现有动态水凝胶虽可实现刚度调控,但缺乏与干细胞分化标志物的直接耦合,导致材料演变与细胞发育节奏脱节,限制了其对复杂组织再生的指导能力。
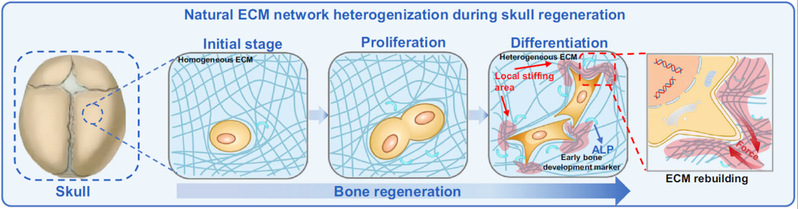
文章要点:基于细胞编程的力学异质性水凝胶设计与组织再生应用
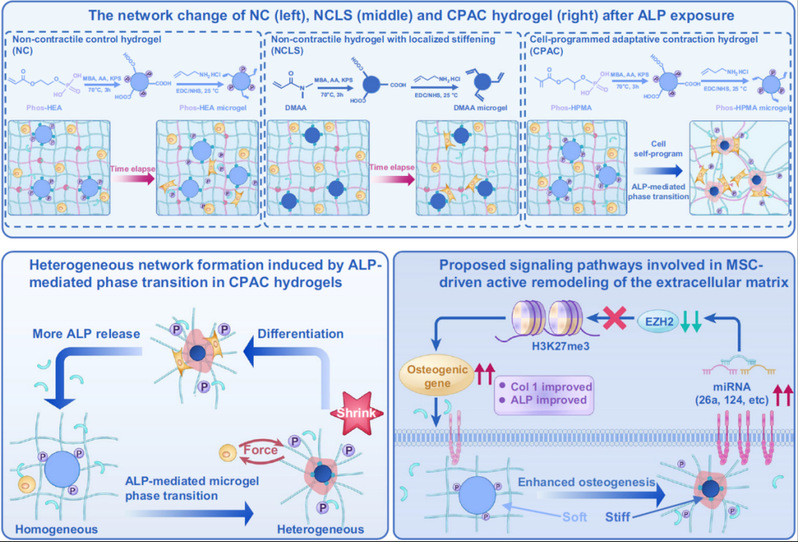
本研究开发了一种基于微凝胶复合的动态水凝胶系统(CPAC水凝胶),其通过细胞分泌的碱性磷酸酶(ALP)介导磷酸化微凝胶的亲水-疏水相变,实现细胞主动调控的局部网络收缩与硬化,从而模拟修复中细胞外基质(ECM)的力学异质性演化。该系统通过两种状态模拟骨修复不同阶段的ECM微环境:
初始均匀网络模拟早期未矿化骨ECM:通过动态主客体交联构建柔软均匀的水凝胶网络,支持间充质干细胞(MSC)的增殖与存活,维持初始干性。细胞驱动的异质性网络模拟发育中骨ECM:MSC分泌的ALP催化微凝胶中磷酸酯水解,触发微凝胶体积收缩,诱导局部基质致密硬化,形成软硬相间的力学异质结构。包裹其中的MSC感知这种异质性后,激活力学传导通路(pFAK、paxillin、pMyosin IIa上调),并通过miR-124-3-1/miR-214/miR-26a介导的表观遗传调控(抑制EZH2、降低H3K27me3)增强成骨基因(Runx2、ALP、Col1、OPN)表达。该水凝胶系统通过细胞自身分化标志物(ALP)驱动的相变与网络重塑,实现了对骨修复过程中ECM力学异质性的时序性模拟,并建立“细胞分泌ALP→基质硬化→促进成骨→更多ALP分泌”的正反馈循环,为干细胞命运调控及骨组织再生提供了智能化材料平台。
该工作以“Mechanically heterogeneous hydrogel with cell-programmed network restructuring promotes tissue regeneration by mechano-epigenetic modulation”为题发表在《Nature Communications》上。文章第一作者为2022级生物医学工程专业博士生凌强君(华南理工大学)和李昊医师(中山大学附属第一医院)。共同通讯作者为华南理工大学国家人体组织功能重建工程技术研究中心边黎明教授、张琨雨教授、赵剑阳副研究员以及广东省人民医院张余教授。边黎明教授2021年获聘教育部长江学者特聘教授,长期致力于发展动态生物材料与干细胞力学调控研究,课题组近期在《Nature Chemistry》、《Nature Communications》、《Journal of the American Chemical Society》等期刊发表多篇论文,更多信息可访问边教授实验室网站:https://www.x-mol.com/groups/bian_lab
