国家人体组织功能重建工程技术研究中心的张云娇教授、杨显珠教授与广东省人民医院温龙平教授合作,提出了基于多功能仿生纳米受体的NanoTAC技术,并在基于NanoTAC技术靶向降解突变p53的肿瘤精准治疗方面取得新进展。相关研究内容以“模拟选择性自噬受体的纳米受体用于靶向降解突变p53蛋白(Nanoreceptors promote mutant p53 protein degradation by mimicking selective autophagy receptors)”为题于2024年1月12日在《自然·纳米技术》(Nature Nanotechnology)上发表,论文的共同第一作者是华南理工大学的黄晓婉博士后、钱洁颖博士后和广州市第一人民医院(华南理工大学附属第二医院)的曹紫洋副研究员。

靶向蛋白降解技术(如PROTAC、LYTAC等)可以利用机体天然降解系统直接降解致病靶蛋白,不仅可以靶向酶,而且还可以靶向无活性位点或者不可成药的蛋白靶标,可针对多靶点进行一网打尽,给疾病治疗带来了巨大希望。然而,成药性差、有效性欠佳、代谢稳定性不良等缺陷和风险严重限制其发展。
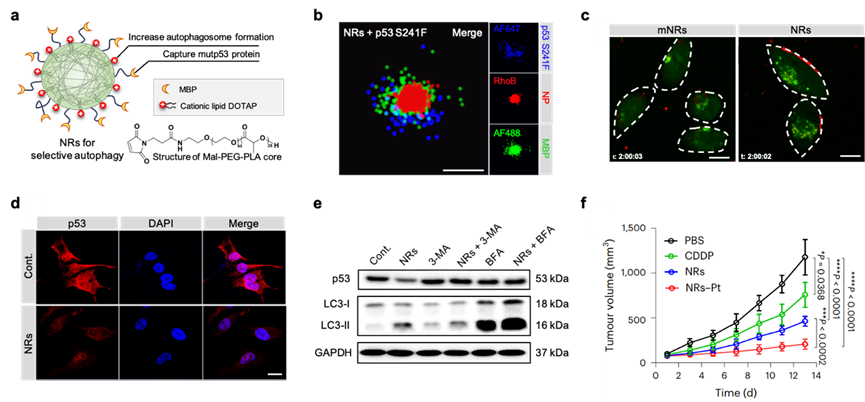
基于选择性自噬降解靶蛋白的生物学原理,研究团队利用FDA批准的纳米药物载体PEG-PLA,修饰MBP多肽和阳离子脂质,利用多肽捕获并识别待降解的突变蛋白、阳离子脂质诱导自噬靶向自噬体,来仿生模拟选择性自噬过程中的关键受体蛋白,实现肿瘤细胞中促癌突变p53蛋白的自噬性降解,在细胞和患者来源的肿瘤异种移植模型中均展现出了显著治疗效果。该NanoTAC技术作为一种全新的仿生纳米平台,在实现药物递送的同时,能够诱导自噬高效靶向降解致病蛋白,为肿瘤等重大疾病的精准治疗提供一个新思路新方向。