学院纳米医学和生物材料团队在国际期刊Cell Biomaterials发表最新研究成果
近日,华南理工大学纳米医学和生物材料团队在国际期刊Cell Biomaterials发表题为“A genetically programmable,conjugation-freenanomedicine platform for modularantibody-guided drug delivery”最新成果。华南理工大学生物医学科学与工程学院博士后田泰宇、赵东坤和2019级生物医学工程毕业生范亚楠博士(现为中国科学技术大学特聘副研究员)为论文共同第一作者,学院王均教授和沈松教授为通讯作者。
王均教授和沈松教授团队研发出一类基因可编程、无化学偶联的模块化抗体介导靶向纳米药物递送平台(T-CN),该平台突破了传统靶向纳米药物的技术瓶颈,实现靶向纳米药物的便捷制备,为靶向纳米药物的临床转化提供了全新解决方案。
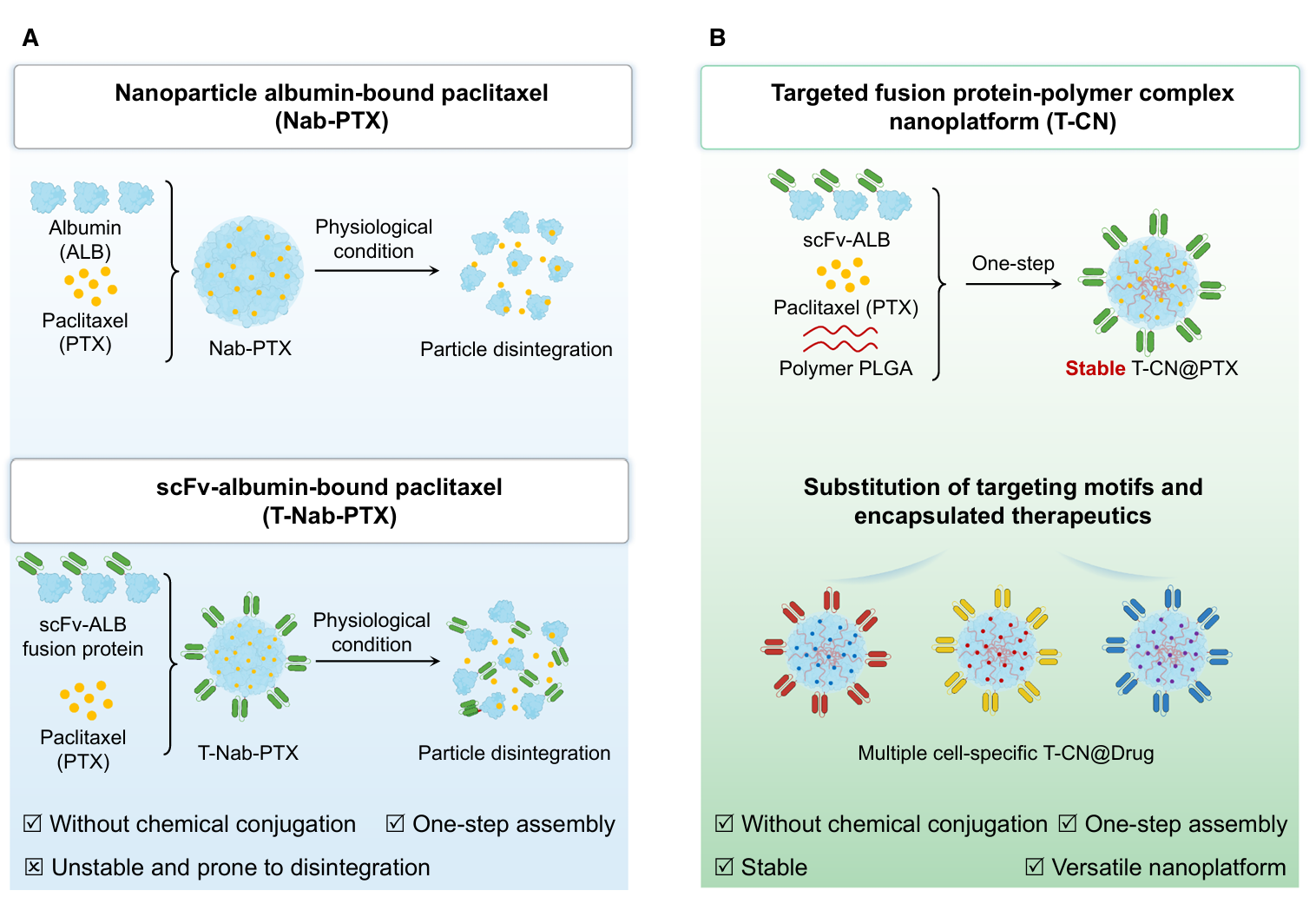
抗体修饰纳米药物凭借其精准靶向递药的优势,已成为纳米递药系统的重要研究方向。然而,这类体系的抗体修饰多依赖化学偶联策略,极大制约了制剂的重现性、规模化制备与临床转化潜力。白蛋白结合型纳米药物虽可规避化学偶联,实现无共价修饰的简易构筑,却存在生理环境下结构易解体、药物泄漏等缺陷,严重影响其体内治疗效果。
为此,团队提出了一种无需偶联步骤的纳米平台T-CN,该平台通过重组单链抗体-白蛋白融合蛋白(scFv-ALB)与聚乳酸-乙醇酸共聚物(PLGA)的一步共组装而成。以人表皮生长因子受体2(HER2)为模型靶点,以紫杉醇(PTX)为代表性载药,构建了T-CN@PTX。在该结构体系中,抗HER2 scFv-ALB融合蛋白同时发挥了引导纳米颗粒组装和实现肿瘤靶向的双重作用;而PLGA则负责增强结构的完整性,并确保药物的高效滞留。在多项体外和体内评估中,与临床应用的Nab-PTX及其靶向类似物相比,T-CN@PTX展现出了更为优越的稳定性、肿瘤蓄积能力以及抗肿瘤疗效。
这种模块化的设计允许便捷地替换靶向配体和治疗性载荷,从而确立了T-CN作为一个多功能平台,为开发具有可规模化生产潜力和细胞特异性的纳米药物提供了基础,并有望在多种疾病治疗场景中实现临床转化应用。(通讯员/王均教授、沈松教授课题组)
原文链接:https://www.cell.com/cell-biomaterials/fulltext/S3050-5623(26)00066-8
