学院边黎明、赵剑阳、赵鹏超、徐夏忆教授团队在Advanced Materials杂志上发表最新研究成果
2026年3月14日,国际学术期刊Advanced Materials在线发表了边黎明教授课题组以“Tissue-Conforming Organoselenium Hydrogel with Microphase-Controlled Acylhydrazone Crosslinking Kinetics Expedites Diabetic Wound Healing by Inhibiting AGE-RAGE Pathways”为题的研究成果。华南理工大学生物医学科学与工程学院副研究员赵剑阳、2024级生物医学工程专业博士生胡媛和材料与化工专业博士生刘财坤为共同第一作者,华南理工大学边黎明教授、赵鹏超教授、徐夏忆教授,斯坦福大学崔淼博士为共同通讯作者。该研究得到国家自然科学基金、国家重点研发项目、广东省自然科学基金等项目的支持。
糖尿病慢性伤口愈合一直是临床上的重大挑战。由于伤口微环境中存在持续的氧化应激和晚期糖基化终末产物(AGEs)的积累,导致炎症无法消退、血管新生受阻,常规敷料难以奏效。前者以过量的活性氧(ROS)为特征,直接造成细胞损伤并维持炎症状态;后者通过非酶糖基化形成,不仅交联细胞外基质(ECM)蛋白从而阻碍重塑,还结合晚期糖基化终末产物受体(RAGE),激发促炎信号级联反应。这些因素共同构成一个慢性炎症、巨噬细胞极化功能障碍和血管生成失败的恶性循环,使得通常仅针对这一复杂网络单一方面的传统治疗方法效果不佳。因此,这一关键空白凸显了迫切需要能够动态调节伤口微环境的集成解决方案,从而促进糖尿病伤口愈合。
自然界通过基于有机硒的氧化还原稳态提供了一种精巧的解决方案,其中谷胱甘肽过氧化物酶(GPx)等硒蛋白凭借其催化的有机硒分子等中间产物维持着生理平衡。这些系统通过一个精巧的两阶段机制运作:快速的活性氧(ROS)中和, 以及基于硒元素氧化还原反应活性的自我再生循环。另外还有证据表明,有机硒基团除了其经典的ROS清除作用外,还可以通过分解预先形成的晚期糖基化终末产物(AGEs)来充当有效的糖化抑制剂。这种内在的双功能特性使有机硒化学成为综合性伤口治疗极具潜力的基础。
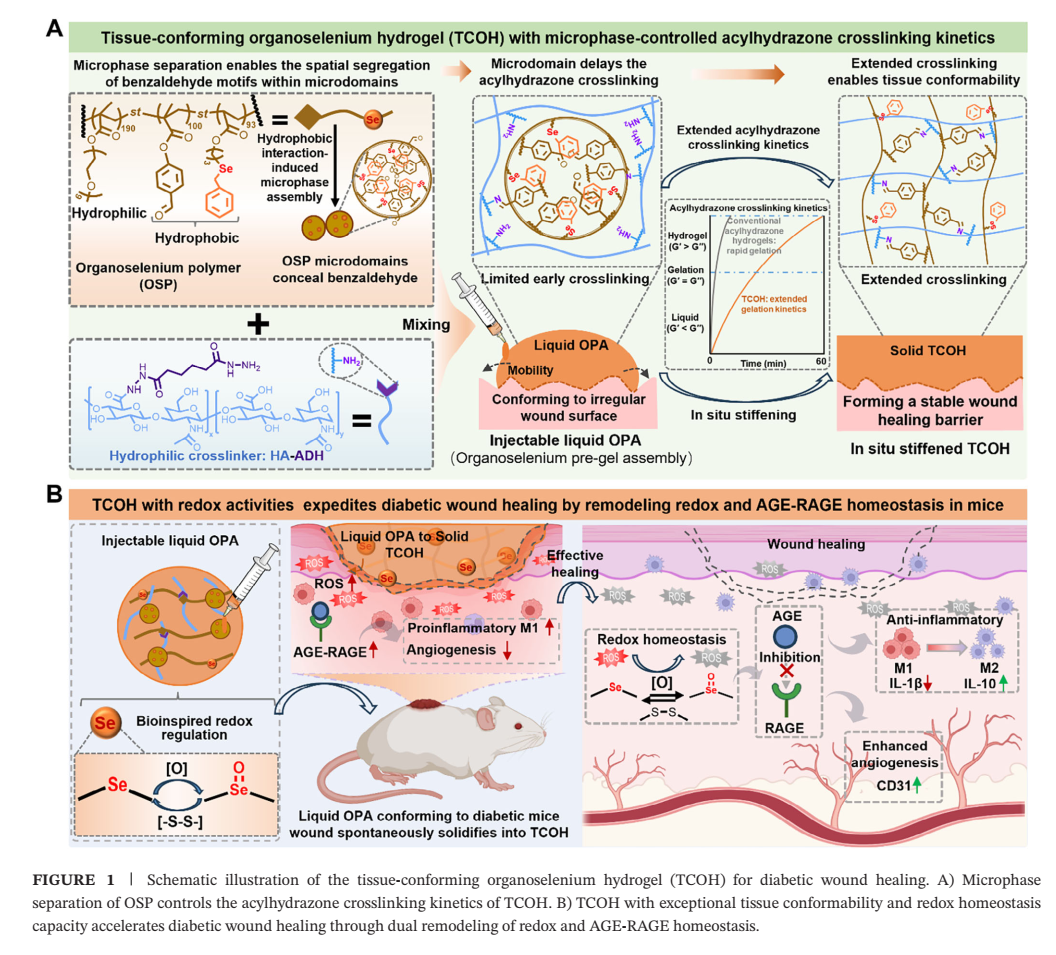
受此启发,华南理工大学边黎明教授和赵剑阳副研究员团队开发了一种名为“组织适形有机硒水凝胶”(TCOH)的新型材料,为糖尿病伤口治疗提供了全新思路 (图1)。具体而言,他们合成了一种能够发生微相分离的有机硒聚合物(OSP),以延长酰腙交联动力学,从而制备出一种组织适形的有机硒水凝胶(TCOH),该水凝胶能有效地将有机硒基团递送至病理性糖尿病伤口床。TCOH能够有效恢复氧化还原稳态,增强血管生成,并通过促进M2巨噬细胞极化来重编程免疫微环境。转录组学分析和蛋白质印迹分析共同证实了糖脂代谢的恢复以及AGE-RAGE和NF-κB信号通路的抑制。这种对促愈合微环境的多方面修复,加速了伤口闭合,增强了胶原沉积和功能性组织再生。这项研究打破了传统预先交联水凝胶不适用于复杂伤口形貌的束缚,通过整合动态材料适应性与有机硒多靶点病理调控功能,为慢性伤口管理建立了新范式,并为各种氧化还原调控和AGE相关的慢性疾病提供了一个有前景的治疗平台。(通讯单位/边黎明、赵剑阳、赵鹏超、徐夏忆教授团队)
论文链接:
https://advanced.onlinelibrary.wiley.com/doi/full/10.1002/adma.72776
