学院边黎明教授、赵鹏超教授团队在Science Advances期刊上发表最新研究成果
近期,华南理工大学生物医学科学与工程学院边黎明教授、赵鹏超教授团队在国际学术期刊Science Advances发表了以“Fluidic microgel assemblies with enhanced oral delivery of biologics alleviate colonic inflammation in murine and canine models”为题的论文。华南理工大学为论文的第一署名单位,生物医学科学与工程学院2024届博士毕业生谢清巧博士为论文的第一作者,华南理工大学边黎明教授、赵鹏超教授和广东省人民医院李勇主任医师为该文章的共同通讯作者。
炎症性肠病(IBD)已成为全球范围内高发且难治的慢性疾病。尽管抗TNF-α等生物制剂(Biologics)显著改善了中重度IBD患者的预后,但其必须依赖皮下或静脉注射,不仅造成较高的全身暴露和副作用,也大大降低患者依从性。口服给药被认为是最理想、直接的给药方式,但实现生物制剂的口服递送面临严峻挑战:胃肠道中的消化酶降解、剧烈的肠液流动、肠道蠕动以及IBD相关的严重腹泻,导致大分子生物药在胃肠道中极易被酶降解,同时难以在病灶区域实现“足够久、足够多”的缓释递送。
基于此,本研究提出了利用多重氢键驱动,将微凝胶颗粒组装成一种“流体状但不与水混溶”的流体微凝胶组装体(Fluidic Microgel Assemblies, FMGA)。这类材料含水量高达77%,既能像液体一样铺展、又不会被肠道液稀释冲散。口服后可在肠道表面形成大面积物理涂层,并实现至少48小时的超长滞留,既能保护生物制剂,又能最大限度地延长其在肠道表面的覆盖面积和时间,极大地增加了药物到达肠道病灶部位的可能性。
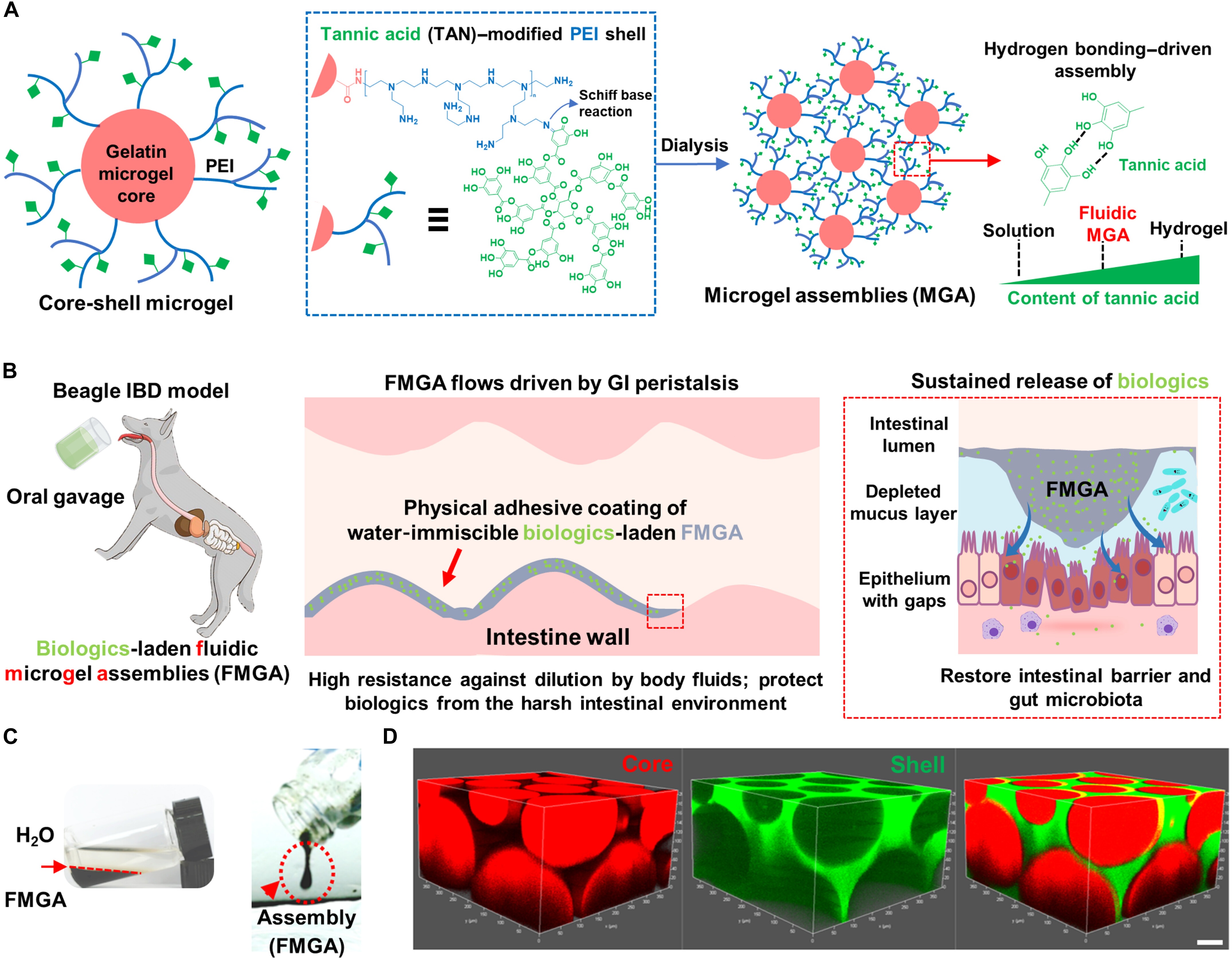
流体微凝胶组装体(FGMA)用于生物制剂口服递送治疗IBD示意图
研究使用外泌体(EXOs)和抗TNF-α抗体作为代表性大分子生物药,系统验证FMGA的递送能力。微凝胶间的微尺度孔隙可高效负载这些大分子药物,保护它们免受胃肠道恶劣环境的降解,并在肠道部位介导药物持续释放。相比直接口服大分子药物,药物负载的FMGA在小鼠和比格犬IBD模型中显著恢复肠屏障,改善了肠道菌群的多样性,并减轻了结肠组织病理炎症反应。这项研究提出了构建同时具备流动性和水不溶性的微凝胶组装体策略,成功克服了口服生物制剂递送在胃肠道中面临的滞留时间短、易降解等核心难题,为生物制剂的口服递送提供了一个简单、通用且高效的平台。(通讯员/边黎明、赵鹏超教授课题组)
文章链接:https://www.science.org/doi/10.1126/sciadv.adv6994
