华南理工大学边黎明教授、张琨雨副教授团队在Cell Biomaterials杂志上发表最新研究成果
在生物医学领域,超分子水凝胶因其独特的动态和可逆结构而备受关注,这些结构使其能够与生物分子进行特异性和可控的相互作用。这种水凝胶通过多种非共价相互作用(如氢键、π-π堆积、疏水相互作用等)组装而成,能够主动识别、捕获和释放生物分子,类似于细胞内外的生物结构。分子互变异构作为一种可逆的分子内原子或官能团迁移过程,能够响应环境刺激,改变分子间的氢键网络,从而调节超分子组装。这种特性使得分子互变异构成为构建响应性超分子水凝胶的有力工具,尤其是在需要对轻微pH变化等温和刺激做出响应的应用中。然而,目前基于分子互变异构的超分子水凝胶的报道还相对较少,且往往需要在极端条件下制备,限制了其在生物医学领域的应用。
2025年6月20日,华南理工大学生物医学科学与工程学院生物材料与再生医学团队设计开发了一种基于分子互变异构的超分子水凝胶,该水凝胶能够特异性地捕获和释放富含腺嘌呤的mRNA,并在动物模型中展示了其在骨关节炎治疗中的潜力。相关研究成果在Cell Biomaterials发表,华南理工大学为该论文的第一署名单位,2024届生物医学工程专业博士生吕远宁论文第一作者,学院边黎明教授、张琨雨副教授、许适当教授,以及中山六院中山大学王涛医生、瑞吉生物胡勇博士为通讯作者。

此种新型超分子水凝胶的形成基于氰尿酸(CYA)通过pH诱导(碱性条件下)的酮-烯醇互变异构(CYA到CYA*)增强分子间的氢键,CYA分子发生结构转变,形成具有更强氢键能力的CYA*,进而与透明质酸(HA)链结合,构建出稳定的三维水凝胶网络。
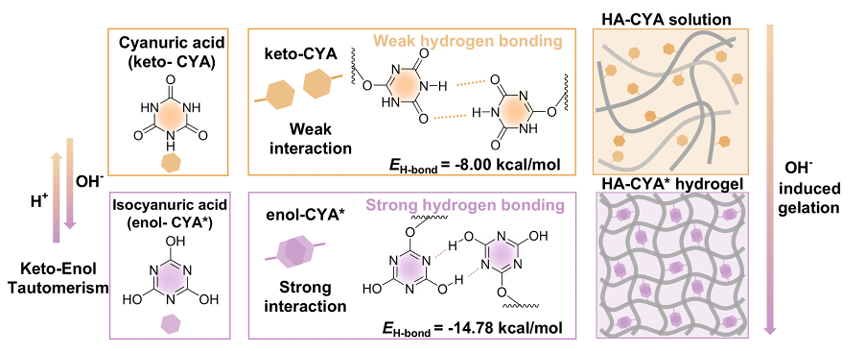
图1.描述 HA-CYA* 水凝胶形成机制的示意图
团队在该研究中创新性地提出了合成新型超分子水凝胶的新策略,不仅解决了在骨关节炎动物模型中的酸性关节微环境下释放治疗性mRNA,显著减轻主要症状,保护软骨和减少骨侵蚀,促进软骨细胞增殖,并增加软骨基质标记物的表达,更为重要的是,展示了CYA基超分子水凝胶在核酸药物递送中的巨大潜力,为以核酸为基础的再生治疗提供了一种新的可能性。(通讯员/边黎明、张琨雨教授课题组)
附文章链接:https://www.cell.com/cell-biomaterials/fulltext/S3050-5623(25)00115-1
