学院付晓玲教授团队在Advanced Science杂志上发表最新研究成果
2025年5月23日,国际学术期刊Advanced Science发表了付晓玲教授团队以“Inhibition and Rescue of Hyperglycemia-Induced Cellular Senescence by Mitochondrial Transfer From Enucleated Mesenchymal Stem Cell-Derived Microvesicles for Chronic Wound Healing”为题的论文。华南理工大学为论文的第一署名单位,生物医学科学与工程学院2021级博士研究生董子萱和2021级硕士研究生刘笑冰为共同第一作者,华南理工大学付晓玲教授为通讯作者。
慢性创面的修复仍然是一个具有挑战性的临床问题,阻碍愈合过程的一个关键因素是压力诱导(如高糖微环境)的衰老细胞异常积累。衰老细胞不仅无法分裂,而且无法对各种促修复信号(包括生长因子和细胞因子)产生有效反应。此外,这些细胞表现出衰老相关的分泌表型(SASP),分泌大量炎症因子并产生过量的活性氧(ROS),从而加剧创面微环境。大量证据表明,线粒体功能障碍在启动和维持细胞衰老中起着关键作用。因此,向创面局部递送线粒体有望恢复细胞线粒体功能,从而挽救细胞衰老表型。付晓玲教授团队开发了基于MSCs衍生微囊泡的线粒体递送策略,实现外源活性线粒体的高效负载及递送,抑制与挽救高糖导致的细胞衰老表型,促进慢性创面愈合。
该研究团队通过脂质体挤压技术,成功制备了包含有功能性线粒体的MSCs衍生微囊泡(Mito@euMVs)。通过将微泡的大小控制在1-4 μm以内,活性线粒体的包封效率被优化到67.2%。获得的Mito@euMVs能够抑制与挽救高血糖诱导的细胞衰老,改善衰老细胞的细胞功能,降低SASP。进一步鱼藤酮抑制实验表明,Mito@euMVs对细胞衰老的抑制与挽救作用主要是由递送的活性线粒体发挥功效。
在此基础上,该研究团队设计了可溶性聚乙烯醇(PVA)微针贴片,从而实现Mito@euMVs的经皮高效给药。借助带有压疮的糖尿病大鼠模型,在体内进一步验证了Mito@euMVs对慢性创面的促愈合效果。结果表明,经微针贴片递送的Mito@euMVs在促进糖尿病慢性创面愈合的同时,可以提升创面处组织的线粒体功能,并改善细胞衰老。同时,该研究团队通过蛋白组学阐明了相关机制,发现以上促进伤口愈合的积极效果可能是由于Mito@euMVs递送的线粒体改善了创面处细胞的线粒体功能、能量代谢与抗氧化能力,并且抑制了炎症发生和细胞衰老相关途径。
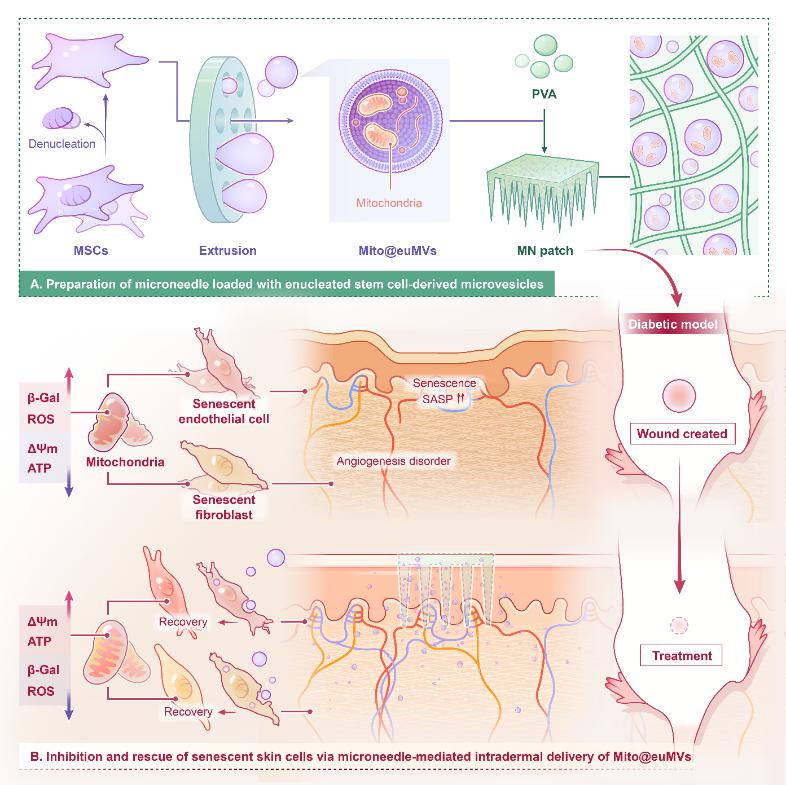
总体而言,这项研究高效制备了基于去核MSCs的微囊泡,用于递送线粒体以挽救细胞衰老。该研究验证了通过线粒体递送促进慢性伤口愈合的有效性。此外,作为多功能的线粒体递送载体,Mito@euMVs为与线粒体功能障碍或衰老相关的多种疾病提供了具有吸引力的治疗策略。(通讯员/付晓玲教授课题组)
原文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202501612
