学院纳米医学和生物材料团队在Cell Biomaterials期刊上发表最新研究成果
2025年3月11日,国际学术期刊Cell Biomaterials在线发表了纳米医学和生物材料团队的研究论文,题为“Leveraging T cell-specific fusogenicity of HIV for in vivo mRNA delivery to produce human CAR-T cells”。华南理工大学为论文的第一署名单位,学院2024届生物医学工程博士研究生王悦和2023级生物学博士研究生杨敏为论文的共同第一作者,华南理工大学王均教授和许从飞副教授为论文的通讯作者。
嵌合抗原受体(Chimeric Antigen Receptor, CAR)-T细胞疗法在治疗血液系统恶性肿瘤中展现出显著的疗效,但传统的CAR-T细胞疗法主要通过体外病毒感染实现CAR分子的持续表达,这一过程复杂、成本高,并且可能诱导细胞因子释放综合征(Cytokine Release Syndrome, CRS)和潜在的致瘤风险。相比之下,mRNA作为一种创新的药物,能够在细胞内快速表达功能性蛋白,且无基因随机整合的风险,但其递送效率受限于T细胞的摄取能力弱和内体逃逸效率低的挑战。面对这一挑战,王均教授和许从飞副教授团队提出了一种创新的体内靶向mRNA递送策略,通过模拟人类免疫缺陷病毒(HIV)的膜融合机制,开发出一种T细胞特异性膜融合型仿病毒颗粒(T-FVLPmCAR),实现了在体内高效、特异性地生产人的CAR-T细胞。
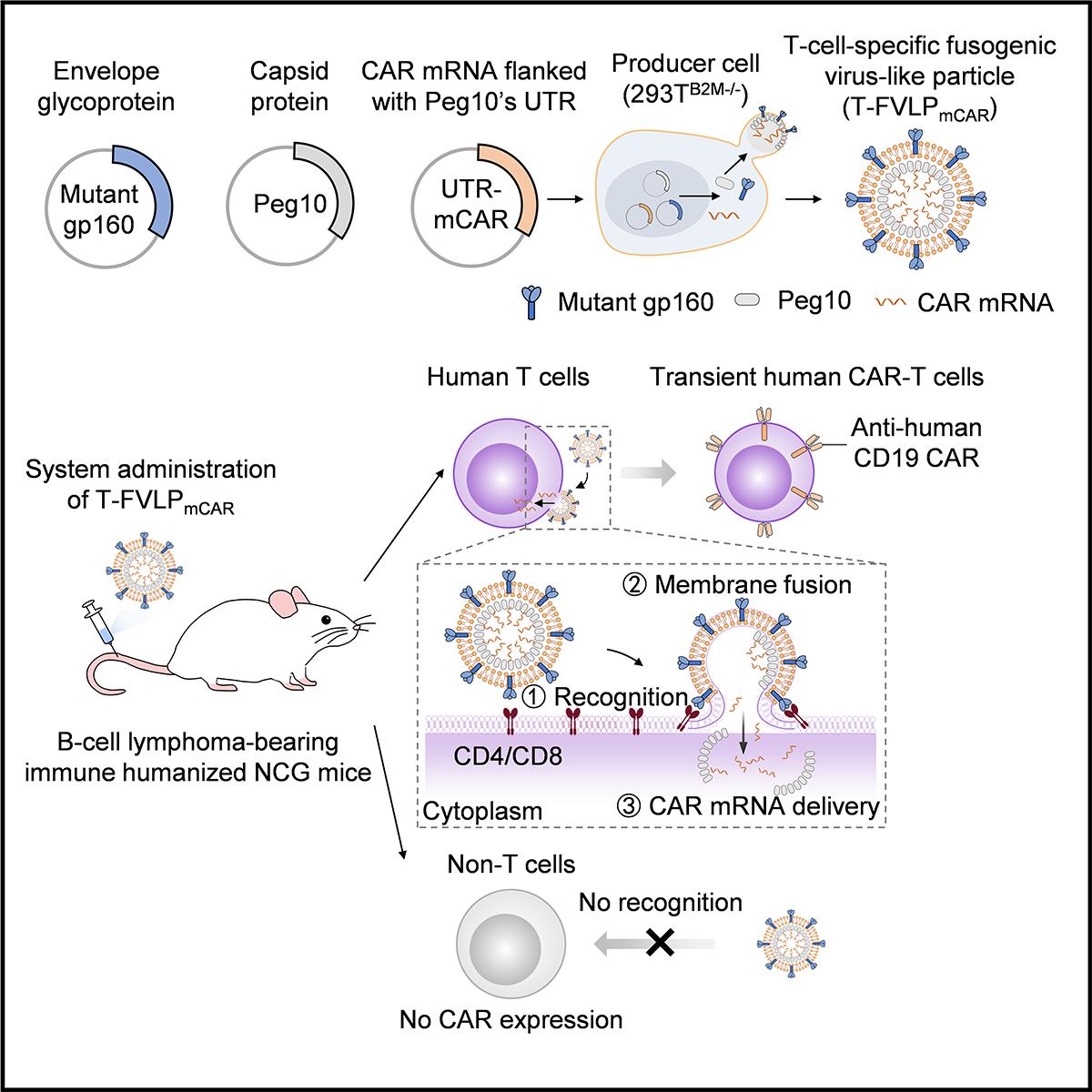
T-FVLPmCAR表面展示了突变型HIV包膜糖蛋白gp160,并通过衣壳蛋白Peg10装载CAR mRNA。该病毒样颗粒能够特异性识别人类T细胞,并通过膜融合机制将CAR mRNA直接递送至T细胞胞质中,从而在体内原位生成CAR-T细胞。实验结果表明,T-FVLPmCAR在免疫人源化小鼠模型中仅需不到1 μg的CAR mRNA即可高效生成CAR-T细胞,并在治疗B细胞淋巴瘤时展现出显著的抗肿瘤效果,且治疗效果呈剂量依赖性。该策略在治疗过程中未引起炎症因子升高或小鼠体重变化,显示出良好的生物相容性和安全性。
王均教授和许从飞副教授团队的研究提供了一种高效、特异的mRNA递送策略,为CAR-T细胞疗法的体内生产开辟了新路径。该策略不仅简化了CAR-T细胞的制备流程,还显著提高了其治疗的安全性,有望降低CAR-T细胞疗法的治疗成本,推动其广泛应用。
文章链接:
https://www.cell.com/cell-biomaterials/fulltext/S3050-5623(25)00002-9
