华南理工大学纳米医学和生物材料团队在Nano Letters杂志上发表最新研究成果
2024年7月2日,国际学术期刊Nano Letters在线发表了纳米医学和生物材料团队以“Ultrasound-Activated PROTAC Prodrugs Overcome Immunosuppression to Actuate Efficient Deep-Tissue Sono-Immunotherapy in Orthotopic Pancreatic Tumor Mouse Models”为题的论文。华南理工大学为论文的第一署名单位,刘晔和王海洋为论文的共同第一作者,袁友永教授为论文的通讯作者。
蛋白水解靶向嵌合体(PROTAC)介导的癌蛋白降解因其不可逆和可重复使用的作用方式成为癌症治疗的有效策略。然而,PROTACs的临床应用受到水溶性差、脱靶不良反应等限制。针对上述问题,华南理工大学袁友永教授团队提出了一种超声(US)可激活的PROTAC前药,该前药整合了靶向PROTAC前药的活性氧(ROS)可激活的含溴结构域蛋白4 (BRD4)和声敏剂Ce6,称为NPCe6+PRO,用于时空激活高效的声免疫治疗。具体来说,Ce6在US作用下产生ROS,促进声动力疗法(SDT),可以穿透深层组织,并诱导免疫原性细胞死亡(ICD)。同时,产生的ROS通过ROS响应机制切割硫代酮(TK)连接子,实现深部组织中PROTAC前体药物的按需激活。这种激活导致BRD4蛋白的降解,同时逆转了SDT过程中发生的PD-L1表达上调。在原位胰腺模型中,NPCe6+PRO能有效抑制超声刺激下的肿瘤生长。因此,本研究提出了一种精确且安全的US激活的PROTAC前药,不仅保证了精准的药物释放,而且防止了肿瘤免疫抑制通路的上调,从而实现对深部肿瘤的高效声动力-免疫治疗。实验结果表明,激活的前药会导致靶蛋白BRD4发生降解,并且能够同时逆转与SDT过程相关的PD-L1表达上调。在裸鼠原位胰腺癌模型中,NPCe6+PRO联合超声刺激可有效抑制肿瘤的生长。(图文/袁友永教授课题组)
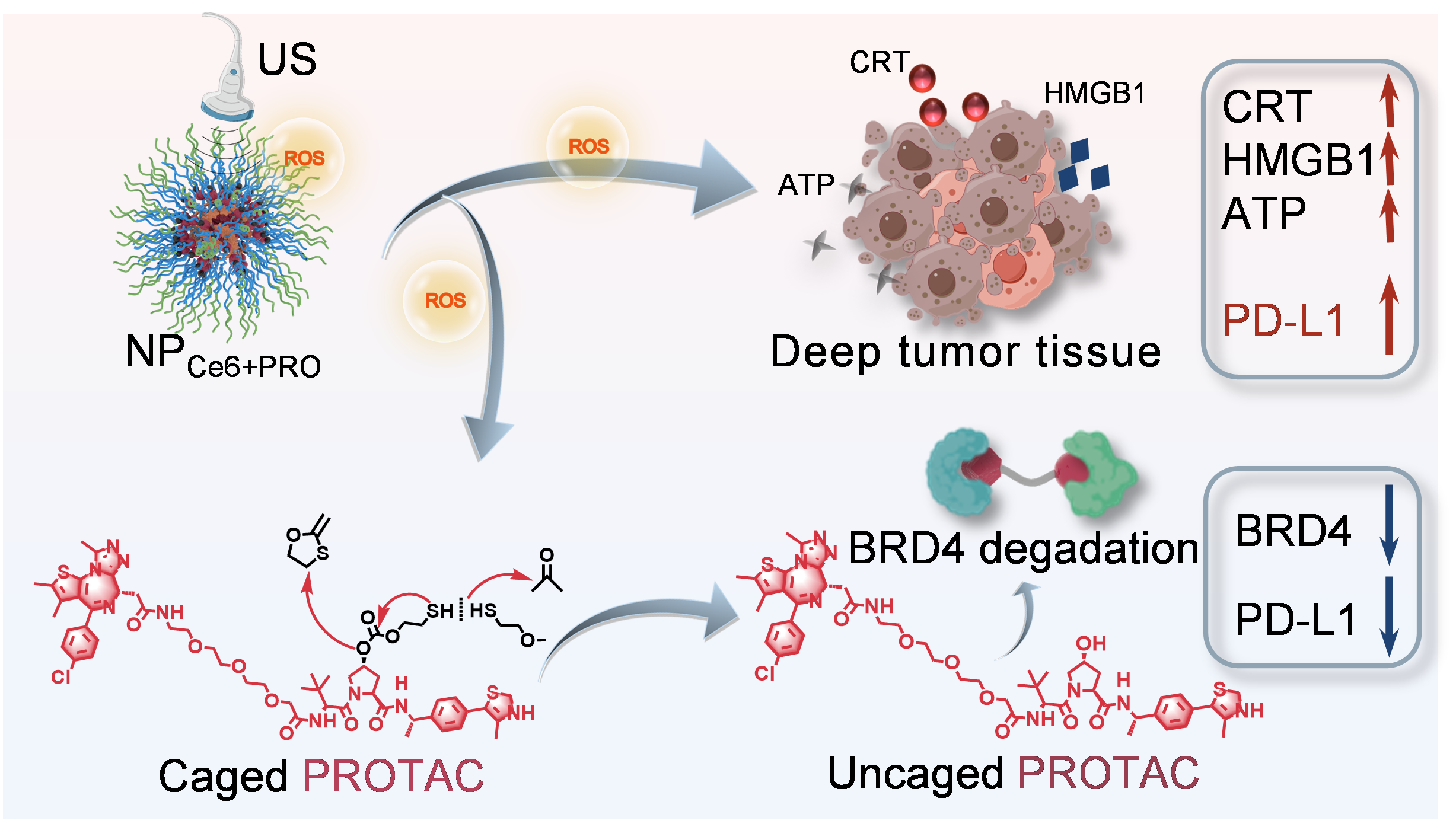
示意图:超声激活NPCe6+PRO用于免疫治疗的机制
附文章链接:https://pubs.acs.org/doi/10.1021/acs.nanolett.4c02287
