科研动态
- 华南理工大学吴钊课题组Nature Synthesis: 高张力环炔介导的羰基1,2-转位新策略 04-17
- 孔宪教授课题组本科生独立工作发表在Mol. Syst. Des. Eng.:电荷监督的等变架构实现数据高效的分子性质预测 02-04
- 华南理工大学孔宪教授团队 《Small》:不对称表面电荷修饰调控受限聚合物电解质中的溶剂化结构和离子电导率 01-28
- 华南理工王宇团队JACS: AI赋能确立“催组装三要素”新原理,开辟手性材料智能创制新范式 12-25
- 华南理工王辉副教授 Nature Communications :靶向线粒体的自发光氟化高分子纳米粒动脉粥样硬化治疗! 11-10
- 华南理工孔宪教授 AFM:PEO基聚合物电解质中氟化模式对溶剂化和离子传输性质的调控 11-10
耐药细菌的出现大大加剧了细菌感染对人类生命的全球威胁。开发能够消灭细菌、同时最大限度地降低宿主毒性并避免诱导耐药性的新型抗菌试剂是十分重要的。抗菌肽 (AMP) 和它们的聚合物模拟物,因其强大的抗菌活性且不易产生耐药性的优势已被开发为传统小分子抗生素的替代品,但由于宿主毒性以及体外评估与体内性能之间的差异,抗菌聚合物的临床转化仍然具有挑战性。大多数获准用于临床的抗菌肽都是具有2-5个带正电荷基团的环状寡肽,包括短杆菌肽S、杆菌肽、多粘菌素B、粘菌素和达托霉素等。环状寡肽/寡聚物的优点包括 (i) 环状拓扑结构具有更高的结合亲和力和特异性,蛋白水解稳定性和优于线性类似物的膜渗透性;(ii) 与聚合物相比,低聚物中阳离子电荷密度较低,可提高体内对抗革兰氏阳性菌的系统功效。然而,抗菌环状低聚物的开发仍然受到低效合成方法和高毒性的阻碍。因此,高效合成更类似于环状抗菌肽的生物相容性环状低聚物显得尤为重要。
近日,华南理工大学前沿软物质学院唐雯课题组提出了一种从硫辛酸衍生物制备阳离子环状寡聚物 (CCOs) 的有效方法。该类环状寡聚二硫化物采用阴离子开环聚合偶联环化解聚的一锅法级联反应获得。这种方法提供了许多临床批准的抗菌肽中具有的优选环状拓扑结构,产量高且易于纯化。同时,CCOs表现出广谱且强效的抗菌活性、高选择性和在还原环境中快速降解的能力(示意图1)。此项工作扩展了二硫化物基化合物的分子平台,为解决耐药性细菌感染危机提供了新的解决方案。
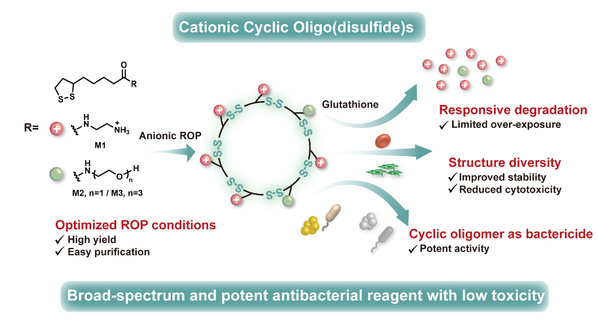
示意图1. 阳离子环状寡聚二硫化物的示意图。
作者通过阴离子开环聚合得到氨基官能化的环状寡聚物pre-CCO1,优化聚合反应条件可得到纯净的、高产率的环状寡聚二硫化物。脱保护后含有阳离子的环状寡聚物二硫化物CCO1,可通过多种结构表征手段,例如NMR、MALDI-ToF等证实最终产物中仅存在环状结构且重复单元个数为3-8,没有可检测到的线性聚合物(图1)。除此之外,通过细致研究单体初始浓度、反应时间以及反应溶剂等因素对聚合行为的影响,作者证实了其环状结构由开环聚合偶联环化解聚的一锅法级联反应获得,环状低聚物为热力学有利的产物(图2)。

图1. 环状寡聚二硫化物的合成与结构表征。

图2. 优化合成条件,得到转化率高、易纯化的CCO1。
中性亲水基团已被证明可通过减少溶血和不良蛋白质复合来降低毒性并在物理化学条件下保持抗菌聚合物的抗菌功效。为了调节 CCO1的细胞毒性,作者将带有不同链长亲水基团的单体与阳离子单体共聚,通过调节化学计量系统地调整 pre-CCO2s 和 pre-CCO3s 中的阳离子/亲水比。作者通过多种结构表征手段同样证实了共聚物均为环状结构,且重复单元个数与均聚物类似(仍为3-8个)(图3)。

图3. 含有亲水基团的环状寡聚二硫化物的合成与表征。
二硫键对生物体内的还原性和氧化性物质有响应性。谷胱甘肽 (GSH) 的浓度在细胞外环境中为微摩尔水平,而在细胞质中为毫摩尔水平。作者通过系统监测CCO1由GSH触发的降解行为,发现当重复单元的初始浓度 [RU]0 远高于 [GSH]0 时,CCO1的降解是总体伪一级反应,Rdp = kdp,app.[GSH],其中kdp,app.是表观降解反应常数(图4 A, B)。二硫键还可以被活性氧物质(例如 H2O2)进一步氧化,形成更亲水的亚砜(-SO-)和砜(-SO2-),使聚硫辛酸具有抗炎作用。因此,作者用类似的方法监测了CCO1被氧化的过程,发现CCO1的氧化是一个总体二级反应,Roxi. = koxi,app.[RU][H2O2],其中koxi,app.是表观氧化反应常数(图4 C, D)。CCO1的降解产物几乎无抗菌特性,溶血率与细胞毒性低于CCO1。共聚分子的降解产物也表现出良好的生物相容性(图4 E-G)。因此,GSH引发的降解确保了低细胞毒性并消除了药物在环境中的积累,有利于长期治疗。
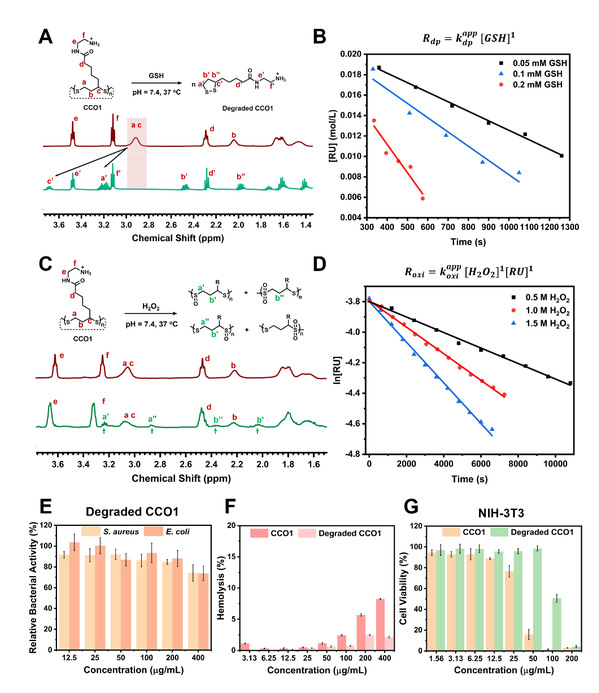
图4. 环状寡聚二硫化物的氧化还原响应性。
细菌实验的结果表明,CCO1对革兰氏阳性菌和革兰氏阴性菌表现出强效且广谱的抗菌活性,CCO1对金黄色葡萄球菌的最小抑菌浓度(MIC)为6.25 μg/mL,对大肠杆菌的MIC为12.5 μg/mL(图5A)。CCO1 在细菌杀菌动力学测定中表现出快速杀菌能力,4×MIC 下30分钟内杀死超过99.9%的金黄色葡萄球菌,2×MIC下仅 5 分钟即可杀死超过99.9%的大肠杆菌(图5B)。在亚MIC浓度的抗菌药物培养24代后,CCO1对金黄色葡萄球菌和铜绿假单胞菌均未产生耐药性,相比之下,金黄色葡萄球菌和铜绿假单胞菌对环丙沙星产生了明显的耐药性,MIC分别增加了512倍和32倍(图5 G-J)。共聚分子具有与CCO1类似的抗菌活性,而引入亲水基团提高了该类环状寡聚物在血清中的稳定性(图6)。
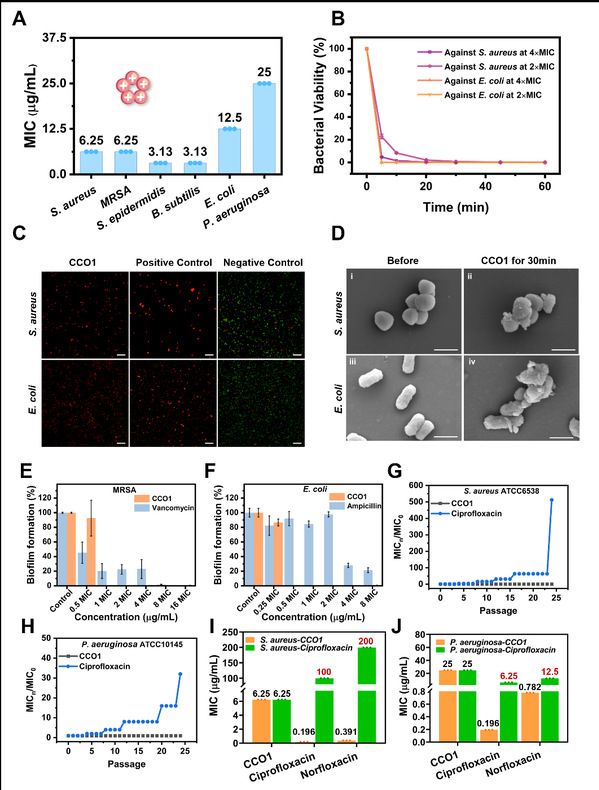
图5. CCO1的抗菌活性以及耐药性测试。

图6. 含亲水基团的CCOs的抗菌活性。
作者计算了CCOs对金黄色葡萄球菌的选择性指数 (SI1,等于 HC50/MIC),其中4种 CCOs的 SI 高于1280,这与之前报道的领先的 AMP 类似物相当,亲水基团的引入增强了血清中的抗菌稳定性并降低了体外细胞毒性,其中CCO2-64% 在该类低聚物中表现出最高的抗菌活性和最高的细胞存活率(图7)。
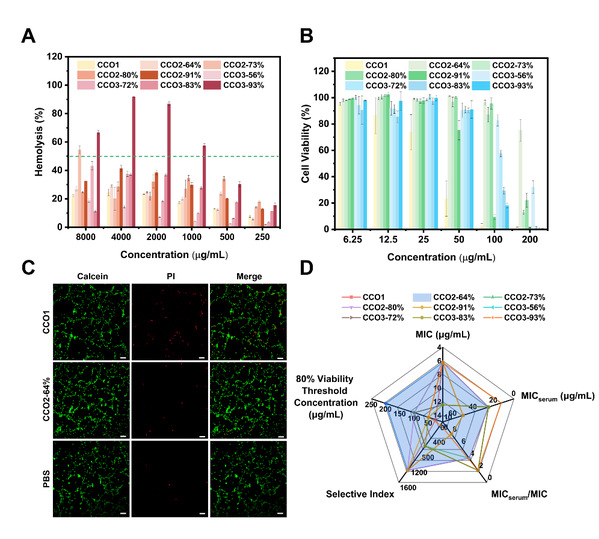
图7. CCOs的生物安全性。
作者通过小鼠背部伤口感染模型,验证了CCOs在体内的抗菌效果。与对照组相比,CCO1和 CCO2-64%的菌落形成单位 (CFU) 分别减少了1.44个对数和 2.30个对数,有效减少了感染伤口中的细菌,经过切片组织分析发现该类分子也可有利于伤口快速愈合(图8)。

图8. CCOs在小鼠全层伤口感染模型中的体内抗菌活性研究。
在该工作中,作者利用硫辛酸衍生物开环聚合的动态特性设计了氧化还原响应性阳离子环状寡聚二硫化物的有效合成路线。研究结果表明,环状寡聚二硫化物在体外和体内均表现出广谱和强效的抗菌活性,同时具有出色的生物相容性。同时,反应动力学的结果表现出该类寡聚物在谷胱甘肽浓度升高的情况下可快速降解以消除抗菌剂对正常组织和环境的不必要暴露,且能清除活性氧化物质,有助于发挥抗氧化和抗炎作用。总之,环状寡聚二硫化物的合成策略简单而有效,为治疗细菌感染以解决抗菌素耐药性难题提供了一种新工具。
该研究成果以“Synthesis of Cationic Cyclic Oligo(disulfide)s via Cyclo-depolymerization: A Redox-responsive and Potent Antibacterial Reagent”为题发表于国际知名学术期刊《Journal of the American Chemical Society》(JACS)。华南理工大学博士生郭佳为本文的第一作者,共同通讯作者是华南理工大学唐雯副教授和美国杜克大学Matthew L. Becker教授。
文章信息:
Guo, J.; Zhang, S.; Tao, Y.; Zheng, W.; Cheng, H.; Li, H.; Wang, Z.; Gou, Y.; Zhu, J.; Li, L.; Liu, Y.; Becker, M. L.*; Tang, W.*
Synthesis of Cationic Cyclic Oligo(disulfide)s via Cyclo-Depolymerization: A Redox-Responsive and Potent Antibacterial Reagent. J. Am. Chem. Soc. 2025, doi: 10.1021/jacs.4c16627.
文章链接:
https://pubs.acs.org/doi/10.1021/jacs.4c16627



