Achievement
刘阳教授等合作研究在Nature Communications发文揭示动脉调控造血干细胞首次进入胚胎骨髓
日期:2022-03-18
造血干细胞(Hematopoietic Stem Cell, HSC)具有分化为几乎所有血液细胞的多能分化潜能,因此在放化疗后进行造血干细胞移植,已广泛应用于多种恶性血液疾病的治疗。对造血干细胞植入骨髓机制的研究,有助于提高造血干细胞移植效率。
在成年哺乳动物体内,造血干细胞主要存在于骨髓中。造血干细胞的维持、静息和增殖等行为受到其微环境的调控。成年动物骨髓中造血干细胞和骨髓微环境的相互作用,已被较深入研究。但胚胎期骨髓微环境如何调控造血干细胞的行为仍不十分清楚。
近日,华南理工大学医学院等单位的合作研究发现,在造血干细胞发育过程中,动脉血管调控造血干细胞首次进入胚胎期骨髓。相关成果以“A specialized bone marrow microenvironment for fetal haematopoiesis”为题于2022年3月14日在线发表在Nature Communications杂志上。

这项研究通过单细胞测序对比分析发现,造血干细胞和骨髓微环境在胚胎期与成年期差异巨大。研究者利用遗传操作小鼠进行分析并发现,与成年期不同的是,胚胎期骨神经并不发挥HSC微环境的作用。缺少骨神经并不显著影响骨髓中造血干/祖细胞(Hematopoietic Stem and Progenitor Cell, HSPC)的数量。同时,成年重要的微环境Lepr+细胞在胚胎期几乎消失,因此也不发挥微环境功能。
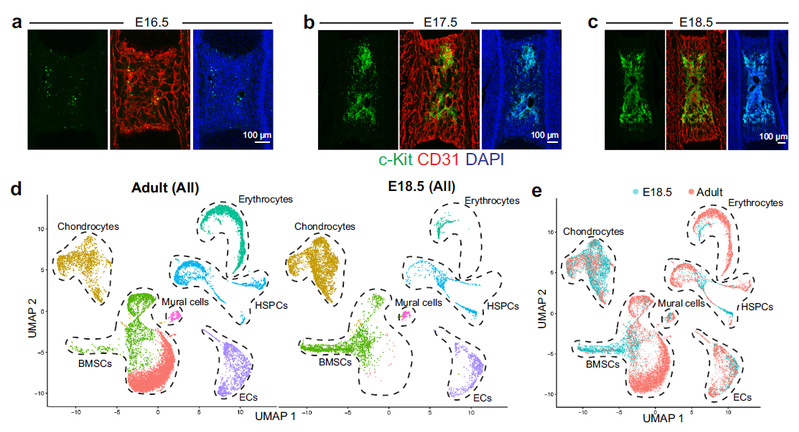
图1:造血干细胞和骨髓微环境在胚胎期与成年期的存在巨大差异
实验结果揭示,骨动脉是胚胎期关键的微环境细胞,在小鼠胚胎发育第16.5天,绝大多数造血干/祖细胞都位于动脉血管旁。此时的骨髓动脉可以释放Wnt2,动脉来源的Wnt信号影响造血干/祖细胞的扩增。而利用重组蛋白Wnt2在体外处理造血干/祖细胞,可以促进造血干/祖细胞的增殖、增强造血干/祖细胞形成体外克隆的能力。
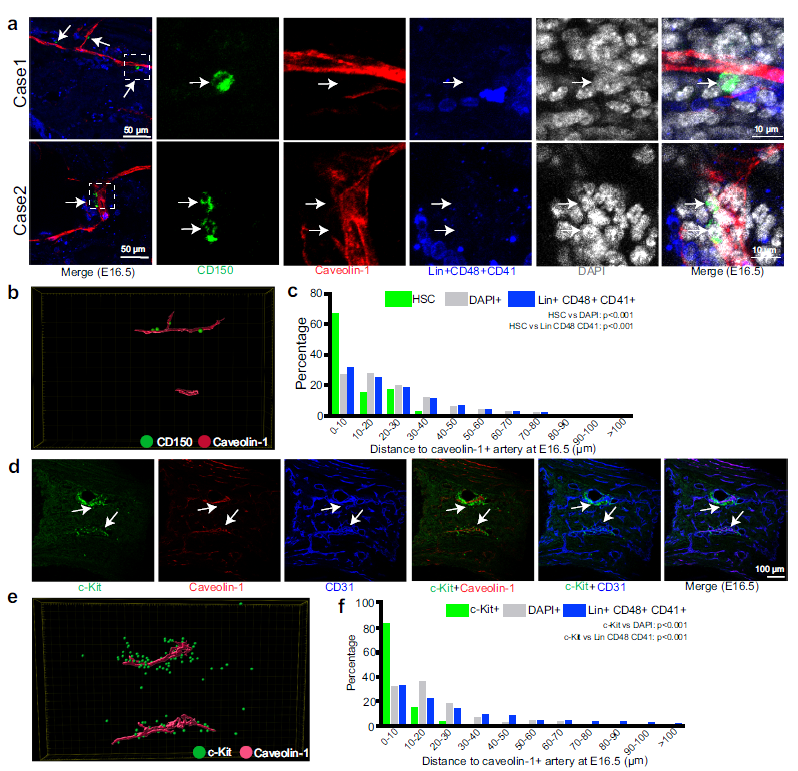
图2:胚胎期造血干细胞聚集于动脉血管旁
该工作首次通过高通量测序揭示骨髓微环境在胚胎期与成年期的细胞类群差异和基因差异,并鉴定了胚胎期特异的微环境因子Wnt2促进HSPC的体外增殖、提高移植早期的效率,从发育的角度为临床应用提供新的思路。
该工作由德国马克思普朗克分子生物医学研究所,与华南理工大学医学院和广州生物医药健康院合作完成。华南理工大学医学院刘阳教授是本项工作的共同第一作者兼通讯作者。
相关论文链接:https://www.nature.com/articles/s41467-022-28775-x

