科研动态
- 突破电子显微成像保真度瓶颈,韩宇教授合作成果发表于《Nature》 05-22
- 华南理工大学吴钊课题组Nature Synthesis: 高张力环炔介导的羰基1,2-转位新策略 04-17
- 孔宪教授课题组本科生独立工作发表在Mol. Syst. Des. Eng.:电荷监督的等变架构实现数据高效的分子性质预测 02-04
- 华南理工大学孔宪教授团队 《Small》:不对称表面电荷修饰调控受限聚合物电解质中的溶剂化结构和离子电导率 01-28
- 华南理工王宇团队JACS: AI赋能确立“催组装三要素”新原理,开辟手性材料智能创制新范式 12-25
- 华南理工王辉副教授 Nature Communications :靶向线粒体的自发光氟化高分子纳米粒动脉粥样硬化治疗! 11-10

动脉粥样硬化是一种慢性血管疾病,主要是由血液中的脂质、炎症细胞和纤维组织在动脉壁的积累形成的。其中,动脉部位的单核细胞在炎症环境中被诱导为巨噬细胞,识别并吞噬血液中过量的氧化低密度脂蛋白(oxLDL)。当oxLDL在胞内积累后,巨噬细胞将进一步转化为泡沫细胞,并产生更多的自由基和炎症因子,进而招募更多的免疫细胞。凋亡的泡沫细胞在动脉内壁的不断积累,形成不稳定斑块,最终导致动脉粥样硬化。近年来,大量证据表明,诱导细胞自噬对动脉粥样硬化治疗具有积极的影响。首先,自噬可以促进细胞内脂滴的降解和清除过程,抑制泡沫细胞的形成。其次,自噬可以通过减少促炎因子的释放来发挥抵抗炎症的作用,有助于控制动脉粥样硬化相关的炎症反应。此外,动脉粥样硬化是一种慢性炎症疾病,活性氧(ROS)水平与动脉粥样硬化的发展和进程密切相关。基于其特殊的病理微环境,将自噬诱导和ROS抑制结合起来,有望为动脉粥样硬化的治疗提供新的可能。
近日,华南理工大学王辉课题组联合华东师范大学程义云团队和上海交通大学第一人民医院王长平团队设计了一系列具有细胞自噬诱导功能的聚吡啶盐高分子递送载体,同时递送两种抗氧化酶(SOD和CAT),通过促进巨噬细胞的自噬能力以及降低细胞内的ROS水平,达到了对动脉粥样硬化的治疗作用。上述工作以“Polypyridiniumswith Inherent Autophagy-Inducing Activity for Atherosclerosis Treatment byIntracellularly Co-Delivering Two Antioxidant Enzymes”为题,发表在Advanced Materials上。论文第一作者为华南理工大学前沿软物质学院博士研究生梁梦晓和上海交通大学第九人民医院王谦。
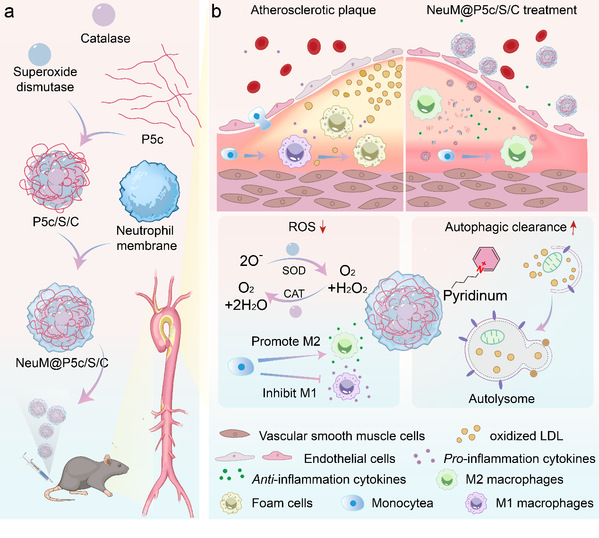
图1. 具有自噬诱导活性的P5c联合递送SOD和CAT治疗动脉粥样硬化
作者通过比较不同碳链长度和修饰比例的聚吡啶盐高分子库对蛋白质的递送能力,从结构与功能的关系上,揭示了聚吡啶盐高分子通过静电、疏水和cation-π相互作用与蛋白质结合形成稳定的蛋白质复合物,并筛选出蛋白递送效率最高的P5c(碳链长度为5,季胺化比例为70%)为主材料进行后续研究。通过肝素钠(heparin)、Tween-20以及10%血清的竞争释放实验表明,P5c主要通过疏水相互作用稳定结合蛋白质,并且具有一定的抗血清性能。
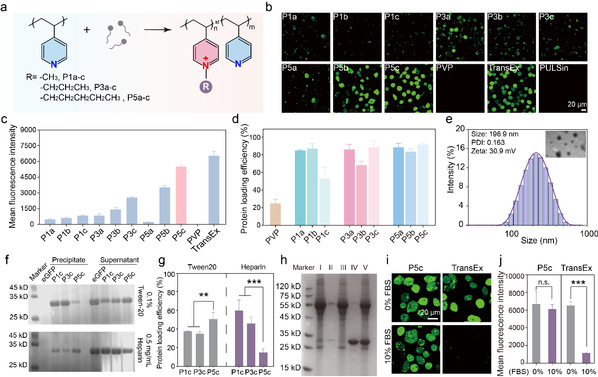
图2. 聚吡啶盐高分子材料的蛋白质胞内递送能力筛选
随后,作者又进一步研究了P5c递送蛋白质的入胞过程,通过对细胞内吞通路进行抑制以及与早期内涵体和溶酶体的共定位分析,发现P5c/eGFP不仅通过巨胞饮和脂筏作用等能量依赖方式进入细胞,还存在非能量依赖的入胞方式。接着钙黄绿素的泄露和入胞实验结合巨型单层囊泡(GUVs)的内含物泄露实验,表明了该非能量依赖方式为膜打孔。
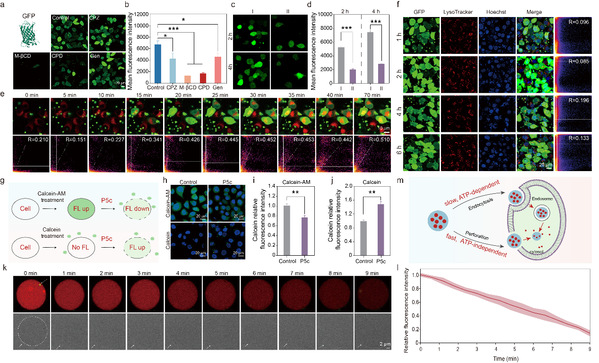
图3.P5c递送蛋白质入胞的机理
在充分研究了P5c递送蛋白质的性能和机理后,作者利用P5c联合递送SOD和CAT进入巨噬细胞。结果表明,该策略可以成功的将两种抗氧化酶递送进巨噬细胞内,并且降低LPS刺激的炎症型巨噬细胞内的ROS水平,并能有效调节巨噬细胞的极化以及炎症因子的分泌。
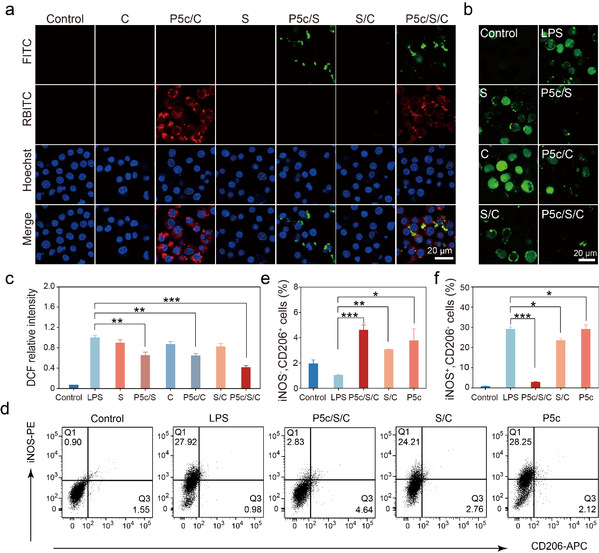
图4. P5c将SOD和CAT递送到巨噬细胞中以清除细胞内ROS并调节巨噬细胞极化
随后,作者详细的验证了P5c以及P5c/S/C复合物对细胞的自噬诱导能力。作者构建了稳定表达mCherry-GFP-LC3B蛋白的143B细胞系,通过对LC3B蛋白的招募情况进行表征,表明了P5c具有诱导细胞自噬的功能。接着,作者对泡沫细胞内的脂滴情况以及LC3和p62等自噬相关蛋白的表达情况进行了检测,结果表明,P5c和 P5c/S/C复合物可以通过激活泡沫细胞的自噬水平,促进泡沫细胞对脂滴的降解,减缓泡沫细胞的生成。
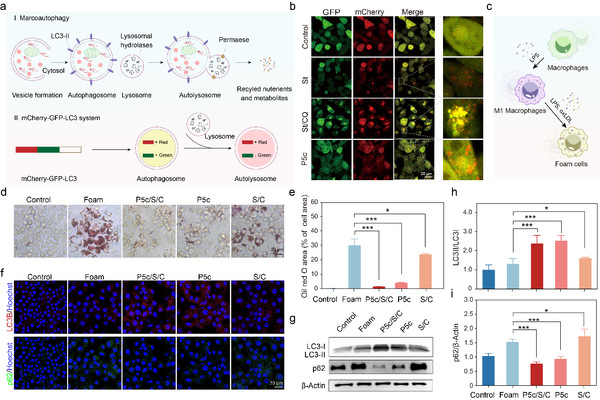
图5.P5c及P5c/S/C复合物通过诱导细胞自噬以抑制泡沫细胞的形成
最后,作者利用中性粒细胞膜对P5c/S/C复合物进行包被,实现复合物对动脉炎症环境的靶向作用。在AopE-/-动脉粥样硬化小鼠模型中,NeuM@P5c/S/C展现出优异的治疗效果。对小鼠动脉部位的切片分析结果表明,该纳米材料不仅能够显著清除斑块部位的ROS水平,还能有效激活该部位细胞的自噬水平,从而抑制动脉粥样硬化的发展。
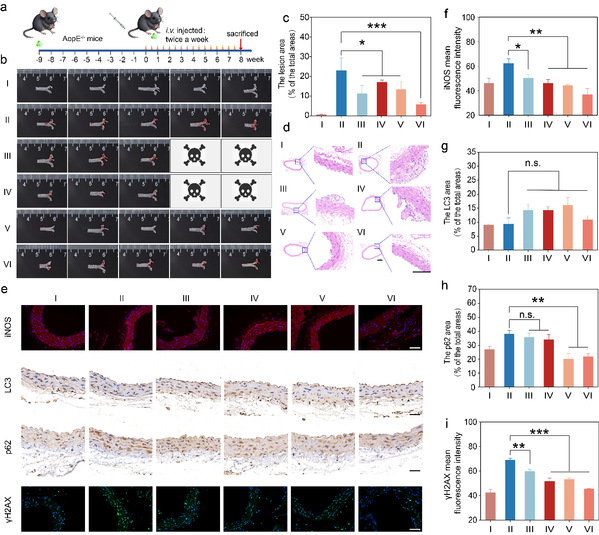
图6.NeuM@P5c/S/C在治疗动脉粥样硬化方面显示出优异的治疗效果
文章信息:
Liang M, Wang Q, Zhang S, Lan Q, Wang R,Tan E, Zhou L, Wang C*, Wang H*, Cheng Y*.Polypyridiniums with Inherent Autophagy-Inducing Activity for AtherosclerosisTreatment by Intracellularly Co-Delivering Two Antioxidant Enzymes. Adv Mater.2024, e2409015. doi: 10.1002/adma.202409015.
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/adma.202409015
图文:前沿软物质学院
编辑:余锦婷
初审:王辉
复审:康德飞
终审:王林格



