华南理工大学生物科学与工程学院朱伟教授团队,近日在国际知名期刊《Small》(IF=12.1)上发表题为《具备长期储存稳定性的可编程生物杂交益生菌,用于增强肠道微生物群调控和溃疡性结肠炎治疗》的研究论文。论文共同第一作者为华南理工大学博士生江佳妮和华南理工大学硕士生董江燕,通讯作者为朱伟教授、深圳市人民医院刘凯胜研究员和李趣欢副教授。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/smll.202512736
在溃疡性结肠炎(UC)治疗中,传统药物始终难以摆脱复发率高、副作用明显和局部疗效不足等痛点。活体益生菌治疗虽然被视为下一代精准干预策略,但其临床应用仍面临三大瓶颈:活性难维持、疗效较单一、药物难精准到达炎症病灶。如何让益生菌“活着到达、精准释放、持续发挥作用”,成为该领域亟待突破的关键科学问题。
利用功能元件对生物体进行外源调控从而强化其结构和功能是一种新兴的生物体改造策略。前期,朱伟教授课题组围绕这一策略开展了大量研究工作(Adv. Mater. 2025, 37, 2417050; Adv. Mater. 2024, 2407831; PNAS 2024, 121, e2408273121; PNAS 2024, 121, e2322418121; Angew. Chem. Int. Ed. 2024, 63, e20240611)。近期,朱伟教授团队联合刘凯胜研究员创新性地构建了一种可编程生物杂化益生菌平台(Bif@FCSM(A)),以双歧杆菌为核心载体,通过多层模块化组装策略,首次实现了“结构强化—功能定制—响应释放”的一体化设计,赋予益生菌更强的环境适应性与精准治疗能力。该平台有效突破了厌氧益生菌(如长双歧杆菌)在临床应用中的关键瓶颈,显著改善了其储存稳定性差、口服递送效率低以及治疗模式单一等问题,为活体益生菌的临床转化提供了新的技术路径。
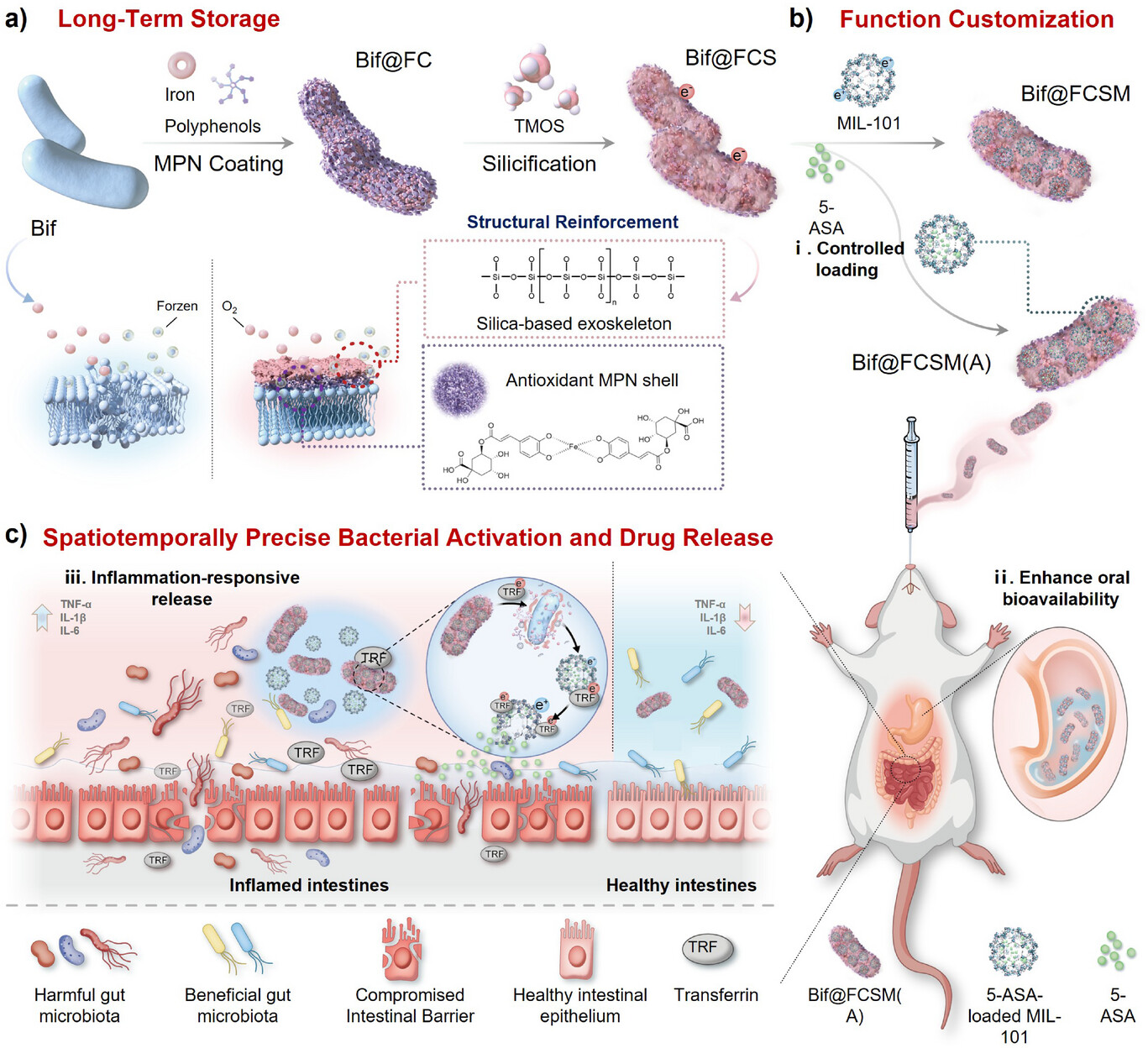
图1. 可编程生物杂化益生菌平台缓解溃疡性结肠炎示意图。 a) 长效储存性能;b) 功能可定制;c)时空精准的细菌激活与药物释放。
该研究的亮点包括:
(1)结构强化:多层“纳米护甲”显著提升稳定性
构建 MPN 氧气屏蔽层+SiO₂ 结构强化层 的多层模块化封装体系,有效抵御氧化损伤与胃酸侵袭。益生菌在有氧储存条件下活性提升41倍,胃液存活能力提升871倍,显著突破传统活菌递送稳定性瓶颈。
(2)功能定制:模块化负载药物,实现益生菌精准功能化
利用 MIL-101-Fe 的高比表面积和大孔容实现治疗药物高效负载,赋予细菌可编程功能化治疗能力,使其不再局限于单一菌群调节功能,而是升级为兼具活菌治疗与药物递送双重作用的智能治疗载体。
(3)响应释放:病灶微环境触发,实现精准激活治疗
炎症组织高表达转铁蛋白竞争性螯合 Fe³⁺,触发外层结构解离,实现药物与益生菌在病灶部位的精准释放与同步激活,推动治疗模式由被动递送升级为病灶驱动的智能响应,显著提升局部治疗效率
该工作首次将长效储存稳定性、炎症响应释放和菌群精准调控有机整合于同一益生菌平台中,为下一代智能活菌治疗系统提供了新的设计范式。
此研究得到深圳市科技计划项目、广东省自然资源厅海洋经济发展专项资金项目、国家自然科学基金、深圳市人民医院“五三”计划、国家自然科学基金、 广东省科技计划项目、广州市科技计划项目以及中央高校基本科研业务费等项目的支持。