黄黎珍与杜红丽团队联合在 Nucleic Acids Research 发文:IPGRM技术揭示CRISPR/Cas9编辑中全基因组DNA修复网络
华南理工大学生物科学与工程学院黄黎珍副教授与杜红丽教授联合团队在核酸研究领域权威期刊 Nucleic Acids Research 在线发表题为“Indel pattern-guided repair mapping reveals genome-wide DNA repair networks in CRISPR/Cas9 editing”的研究论文。学院2025级博士研究生万延斌、2021级硕士研究生黄冬超、2023级硕士研究生赵炫烨、林锡定为论文共同完成人,黄黎珍副教授、杜红丽教授为共同通讯作者,华南理工大学生物科学与工程学院为第一通讯单位。论文链接:https://doi.org/10.1093/nar/gkag260

CRISPR/Cas9技术通过诱导DNA双链断裂实现基因编辑,其最终编辑结果高度依赖细胞内DNA修复通路。然而,不同修复结果产生的分子机制及其调控网络长期以来尚未被系统解析,这在一定程度上限制了基因编辑的可预测性和精确控制能力。
本研究首先通过对Cas9基因编辑结局进行高通量测序及系统数据分析,在看似随机的编辑结果中发现了高度规律性的修复模式:从序列特征来看,插入修复中1 bp模板化插入占绝对主导地位,删除修复中微同源介导的删除修复呈现明显优势,据此将Cas9修复结局归纳总结为七种规律性修复结局;从修复动力学来看,这七种规律性结局同样表现出特征性的时间动态特点,其中1 bp插入通常在编辑早期迅速完成,体现NHEJ快速修复特征,微同源介导的缺失则在后期逐渐累积,反映MMEJ通路的延迟激活,而大插入和突变则呈现持续发生的趋势。这些结果共同表明,DNA修复并非随机过程,而是具有稳定时间程序性的动态过程,不同修复通路之间存在明显的竞争与协同关系。
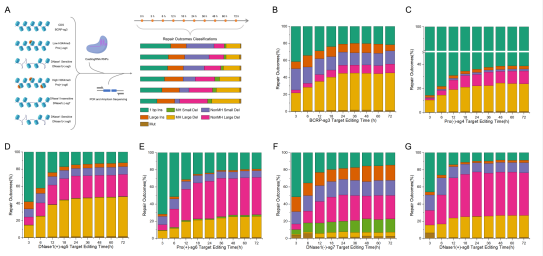
图1 Cas9 诱导的多个基因组位点修复模式的时间动态
基于前述修复规律性探索,本团队创新性构建了基于规律性修复结局导向的IPGRM(Indel Pattern-Guided Repair Mapping)筛选技术。该技术的核心突破在于:首次将1 bp插入(1 bp Ins)、大片段插入(Large Ins)、无微同源小缺失(NonMH small Del)、无微同源大缺失(NonMH Large Del)、微同源介导小缺失(MH small Del)、微同源介导大缺失(MH Large Del)以及复杂突变(Mut)等七类具有明确分子特征的修复结局,编码为可自动化识别的序列算法模型,实现对单个靶点数百万编辑产物的秒级模式识别与结局分类。这一方法论突破,使本研究首次具备了对不同编辑结局背后的各种修复通路调控因子进行全基因组、无偏倚系统性筛选的能力。与以往传统方法相比,以往大量数据仅能完成中通量基因组筛选,或仅能解析少数具体修复结局;而IPGRM技术在相同测序数据要求的前提下,即可完成全基因组水平的大规模筛选,同时实现对七类修复结局的同步解析,显著提升了筛选通量与解析广度。
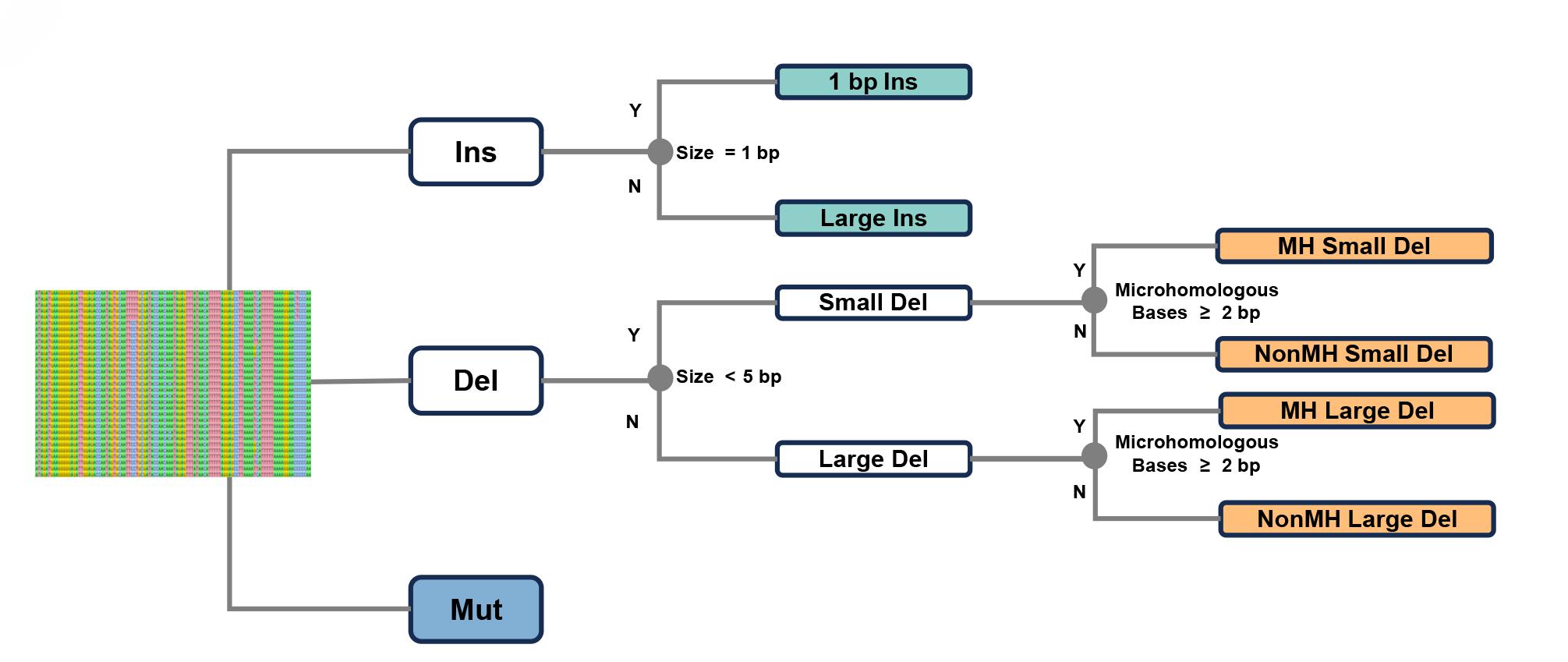
图2 IPGRM分类流程示意图
依托IPGRM高通量筛选平台,研究团队完成了覆盖全基因组约19,050个编码基因及1,864个miRNA基因的CRISPR筛选文库构建与repair-seq解析,系统鉴定了参与不同修复模式的关键调控因子。功能聚类分析揭示了修复调控的三类核心模块:微同源介导末端连接(MMEJ)驱动的MH缺失形成一个由蛋白编码基因和miRNA共同定义的协同调控模块,而非仅由核心修复酶本身决定;非同源末端连接(NHEJ)协调1 bp插入和非MH缺失,其中RFC4/5通过稳定修复模板来抑制大缺失的发生;非常规修复结果则呈现独特的遗传特征——大插入与聚合酶相关调控因子相关联,而复杂突变则富集染色质相关调控因子。值得注意的是,S100A8通过与PARP1直接互作,被鉴定为一个强效的MMEJ抑制因子,揭示了炎症信号与DSB修复通路选择之间未被充分认识的交叉对话。
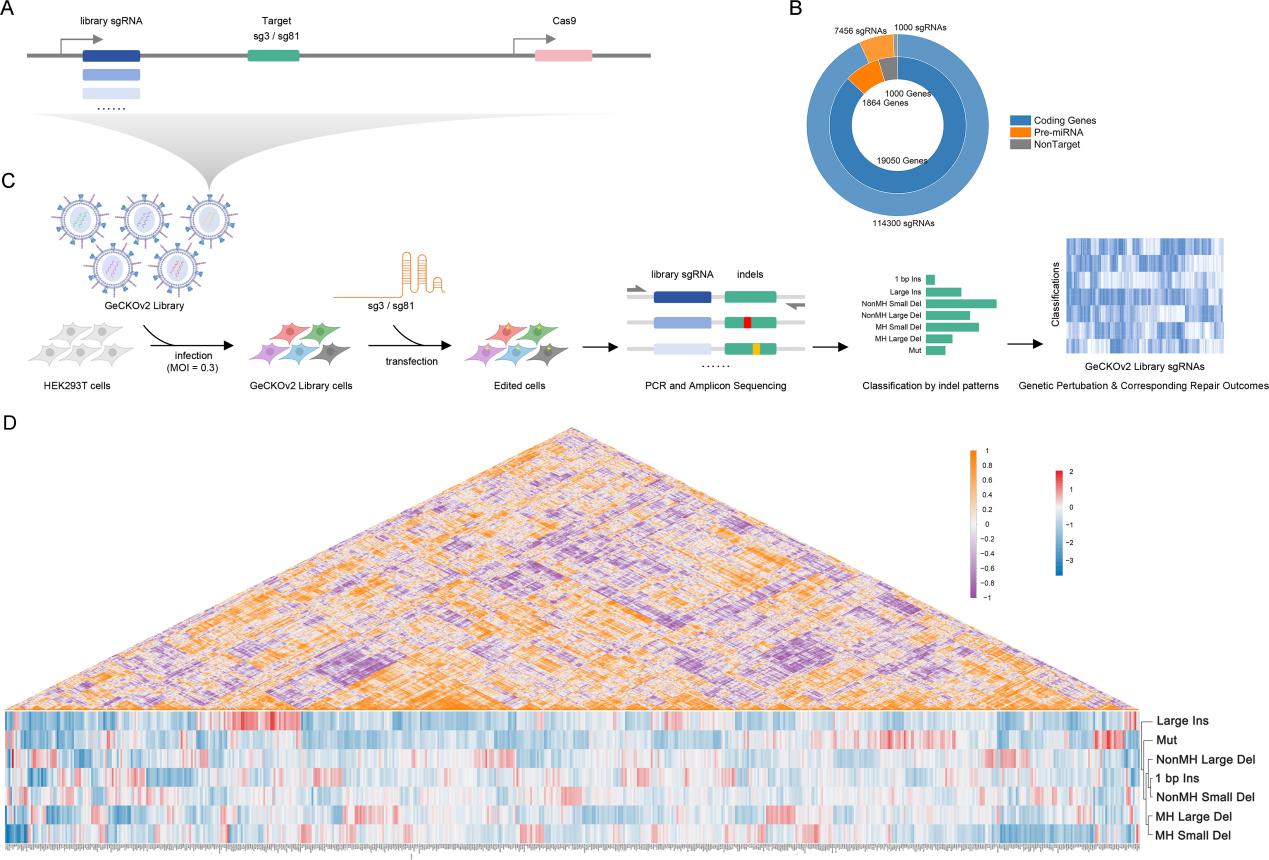
图3 IPGRM鉴定参与不同修复模式的关键调控因子
研究首次发现大量miRNA的缺失可显著改变Cas9编辑产物谱特征,且不同miRNA呈现鲜明的修复结局调控偏好性:部分miRNA选择性调控微同源介导缺失(MH small Del和/或MH Large Del),部分特异性影响1 bp插入事件,另有若干miRNA可同时重塑多种修复结局的竞争平衡。这一发现不仅将DNA修复的调控维度从蛋白质编码基因拓展至非编码RNA层面,更揭示了转录后调控在DNA修复中的重要作用,为精准基因编辑的调控策略开辟了新的方向。
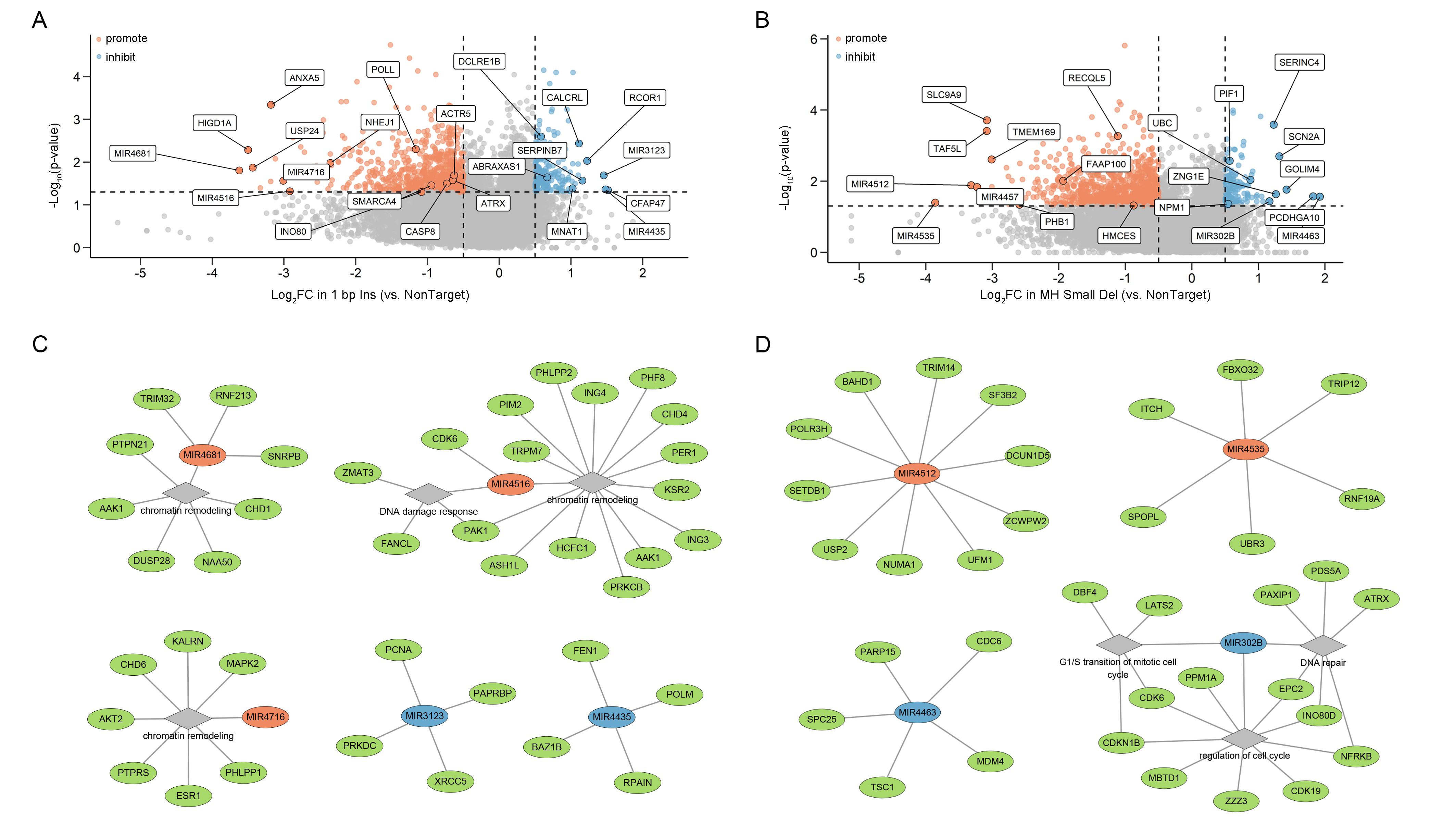
图4 IPGRM揭示编码基因和miRNA对DSB修复的多层次调控
综上,该研究建立了基于编辑结果模式的IPGRM分析框架,系统揭示了CRISPR/Cas9编辑过程中DNA修复的时间动态特征及其全基因组调控网络,拓展了对DNA修复机制的理解,并为提升基因编辑精确性及开发相关治疗策略提供了重要理论依据。
该研究得到广东省自然科学基金(2022A1515011733、2025A1515010459)、广东省药品监督管理局科技创新计划(2024ZDZ07)、广州市重点研发计划(202206010073、2023A03J0542)等资助。