朱伟教授团队在ACS Nano期刊发表前瞻性论文:生物层级间的生物硅化作用
近日,华南理工大学生物科学与工程学院朱伟教授在纳米科学顶级期刊ACS Nano(IF=16.5)上在线发表题目为“Biosilicification across biological hierarchies”的论文,系统阐述了生物硅化技术从分子到宏观生物全层级的研究进展、核心体系与转化前景,为生物无机工程、生物资源保存、肿瘤免疫治疗等交叉领域开辟了全新发展方向。华南理工大学生物科学与工程学院硕士生林沐雨阳、博士生郭思诗、博士后周亮为共同第一作者,朱伟教授与美国新墨西哥大学C. Jeffrey Brinker院士为共同通讯作者。
论文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c22206
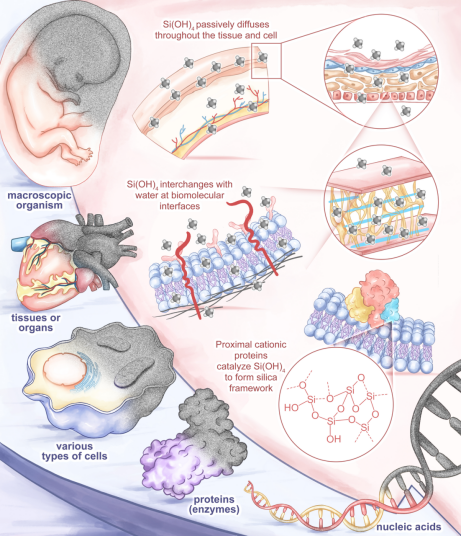
图1. 在不同层级尺度上稳定或功能性演化生物样本的生物硅化技术示意图
生物样本与生物活性物质的长期稳定保存、功能强化,一直是生命科学、生物医药领域的核心难题。传统超低温冷冻、化学固定等方法,存在成本高昂、高度依赖冷链、易造成生物结构与遗传信息不可逆损伤等诸多瓶颈。而海洋中的硅藻等硅质生物,历经亿万年进化形成了精密的生物硅化调控通路,能在温和生理条件下构建出机械性能极强、结构高度有序的二氧化硅生物骨架,这为人工生物硅化技术的发展提供了天然的仿生蓝图。近年来,随着合成生物学、材料科学与生物无机化学的深度交叉融合,生物硅化技术实现了跨越式发展,成为突破传统生物保存与功能强化技术瓶颈的核心方向
什么是 “生物硅化”?
生物硅化指由生物调控的硅元素摄取、转运与沉积过程,可通过蛋白催化的溶胶-凝胶反应,在生命体系内部或表面原位形成硅基生物矿物结构,是一类有机-无机杂化界面工程。相比传统“体外制备-体内递送”的材料应用模式,生物硅化具有不可替代的核心优势:反应条件温和,全程可在常温常压水相环境中进行,无剧烈理化刺激;跨尺度普适性强,可覆盖从核酸、蛋白等生物大分子到完整器官、多细胞生物的全层级样本;可实现自限性沉积,精准调控硅层厚度与孔隙率,兼顾保护效果与物质交换;生物相容性优异,硅化产物可在体内可控降解并经肾脏安全清除,无长期蓄积毒性。
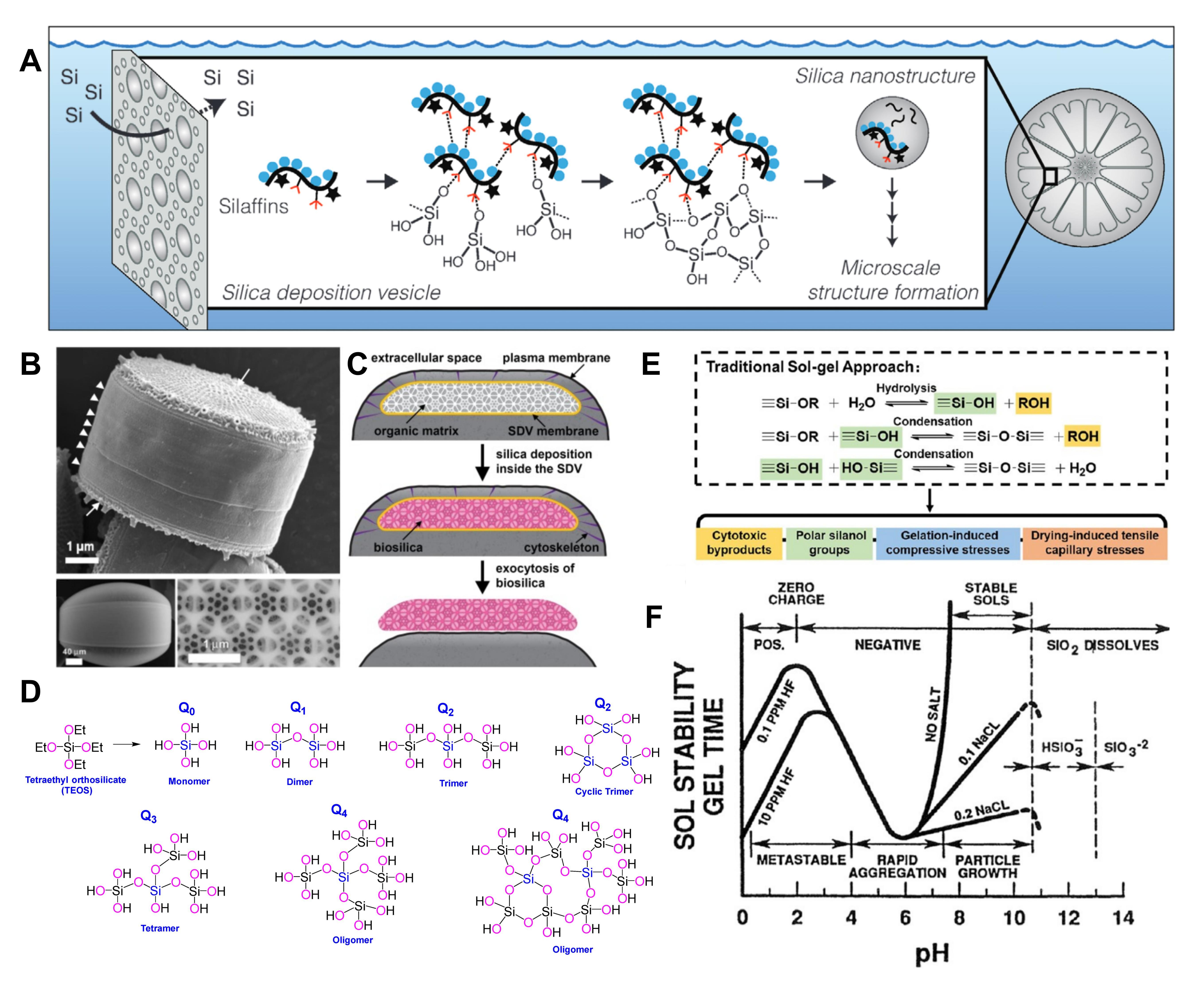
图2. 自然界生物硅化与人工定制化仿生硅化技术
从核酸分子到整体生物:四大核心应用层级
1.核酸尺度硅化
核酸作为遗传信息的核心载体,其稳定保存是维持生物遗传连续性与多样性的关键,而天然DNA结构脆弱,极易受温度、酶解、氧化等因素影响发生降解。核酸尺度的生物硅化,核心是通过冷冻硅化、深度硅化等技术,实现基因组DNA的原位封装与高保真保护。通过优化的硅前体递送策略,正硅酸分子可高效渗透进入细胞与细胞核,在蛋白催化下形成均匀的二氧化硅网络,对全基因组实现360°包裹保护。例如,冷冻硅化技术可将常温环境下基因组DNA的半衰期延长至1208年,是未保护样本的167倍,同时保持极低的基因突变率,甚至低于PCR扩增中Taq酶的错误率;深度硅化技术则实现了从微生物到多细胞生物的跨尺度基因组保存,70℃加速老化3周后,目标基因片段回收率仍超50%,为生物种质资源库、法医样本保存、古基因组研究提供了颠覆性方案。
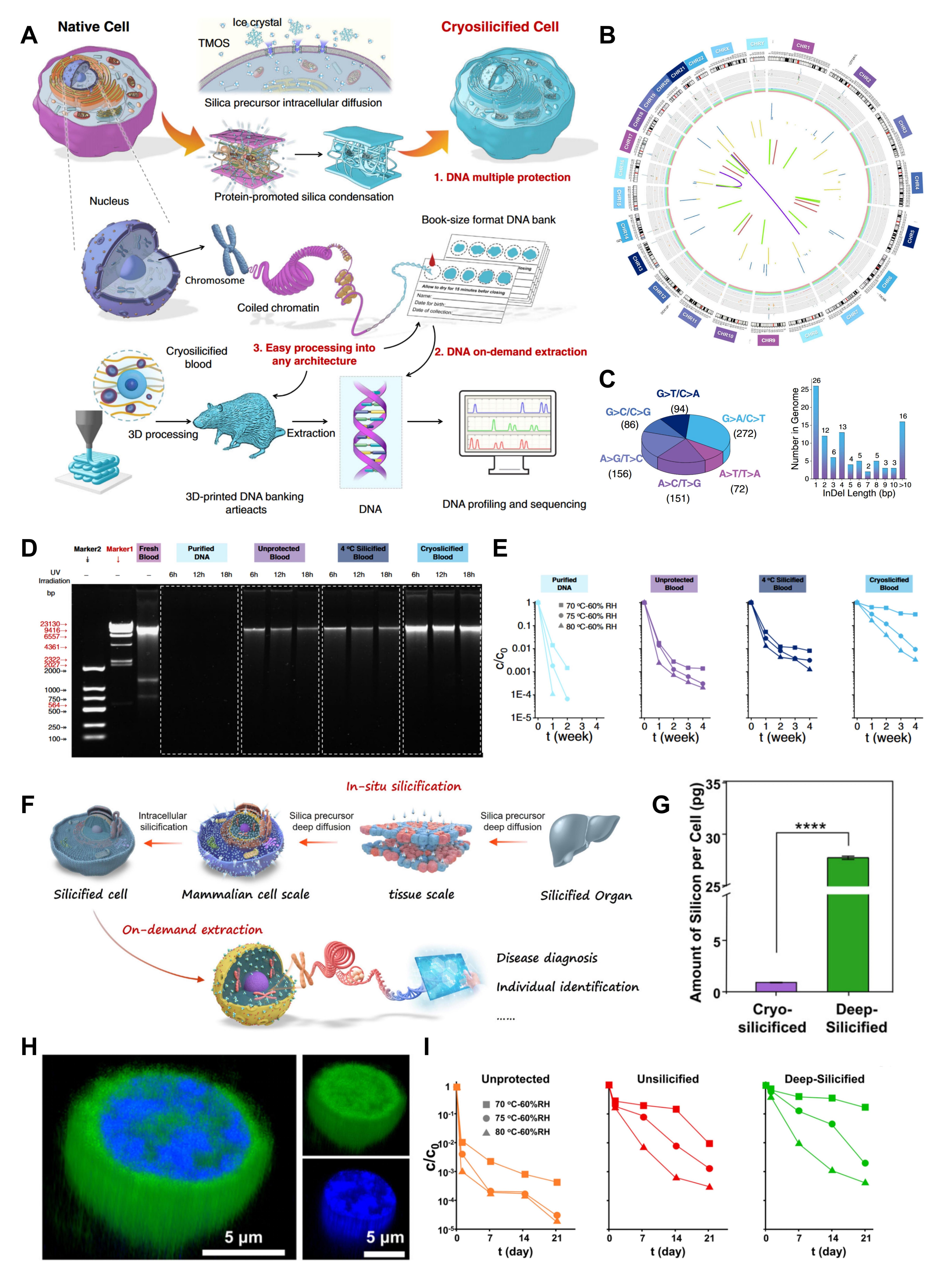
图3. 核酸尺度的生物硅化
2.蛋白(酶)尺度硅化
蛋白与酶是生命活动的核心执行者,但其天然结构极不稳定,易在环境胁迫下发生变性失活,长期以来高度依赖冷链系统保存与运输。蛋白尺度的生物硅化,从胞外单酶分子到胞内蛋白组实现了全维度保护与功能增强。在单酶水平,创新开发的“硅酶”技术,通过多组分硅前体在单酶分子上的精准修饰,打破了传统酶固定化“活性-稳定性不可兼得”的零和困境,不仅使脂肪酶、葡萄糖氧化酶等工业酶的催化活性提升1.26-1.95倍,还大幅增强了其耐温、耐有机溶剂、耐极端pH的能力;针对胞内蛋白,自限性硅化技术可在细胞内形成纳米级半透硅壳,室温储存1年后,胞内多种关键酶的活性仍能保留80%以上,而传统固定方法的保留率不足3%,彻底摆脱了生物酶制剂对冷链系统的依赖。
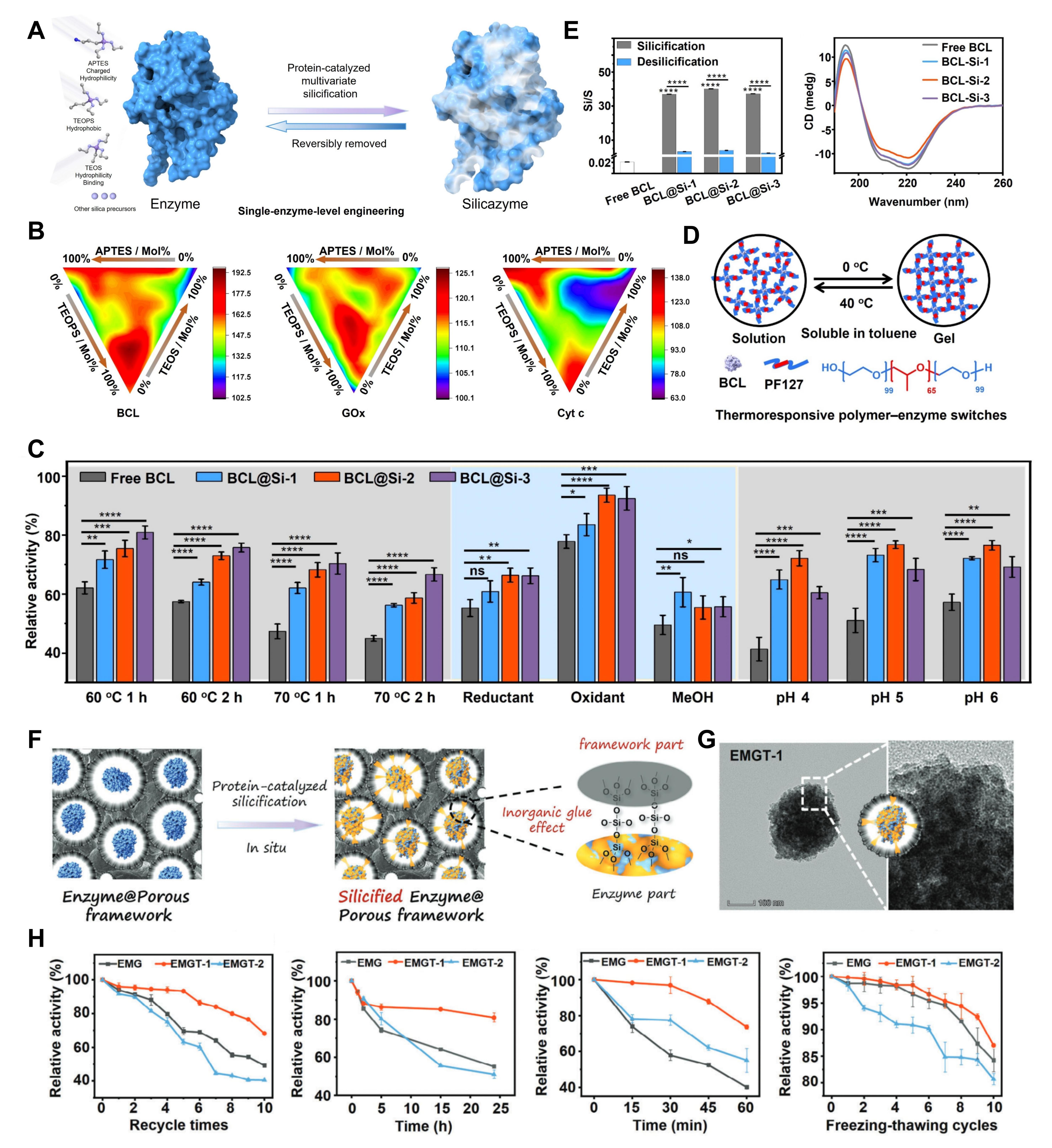
图4. 蛋白质尺度的生物硅化
3.细胞尺度硅化
细胞是生命结构与功能的基本单位,也是细胞治疗、再生医学、疫苗开发的核心载体,细胞尺度硅化是生物硅化技术最核心的应用场景。通过细胞膜表面或胞内的可控硅化,既能为细胞构建一层“无机铠甲”增强环境耐受性,又能精准调控细胞生理功能与命运走向,适配多元化的生物医药应用。例如,在肿瘤免疫治疗领域,基于硅化技术开发的全细胞肿瘤疫苗,可在室温干燥条件下长期稳定保存肿瘤全抗原,功能化修饰后在小鼠卵巢癌模型中实现了100%的治愈率,单次预防性免疫即可为机体提供完全的肿瘤攻击保护;在输血医学领域,红细胞表面的仿生硅化可有效屏蔽血型抗原,构建出具备通用输注潜力的新型红细胞制品,同时完整保留其携氧能力与体内循环特性;此外,细胞尺度硅化还能实现肿瘤细胞靶向凋亡诱导、间充质干细胞成骨分化定向调控,为再生医学与精准肿瘤治疗提供了全新策略。
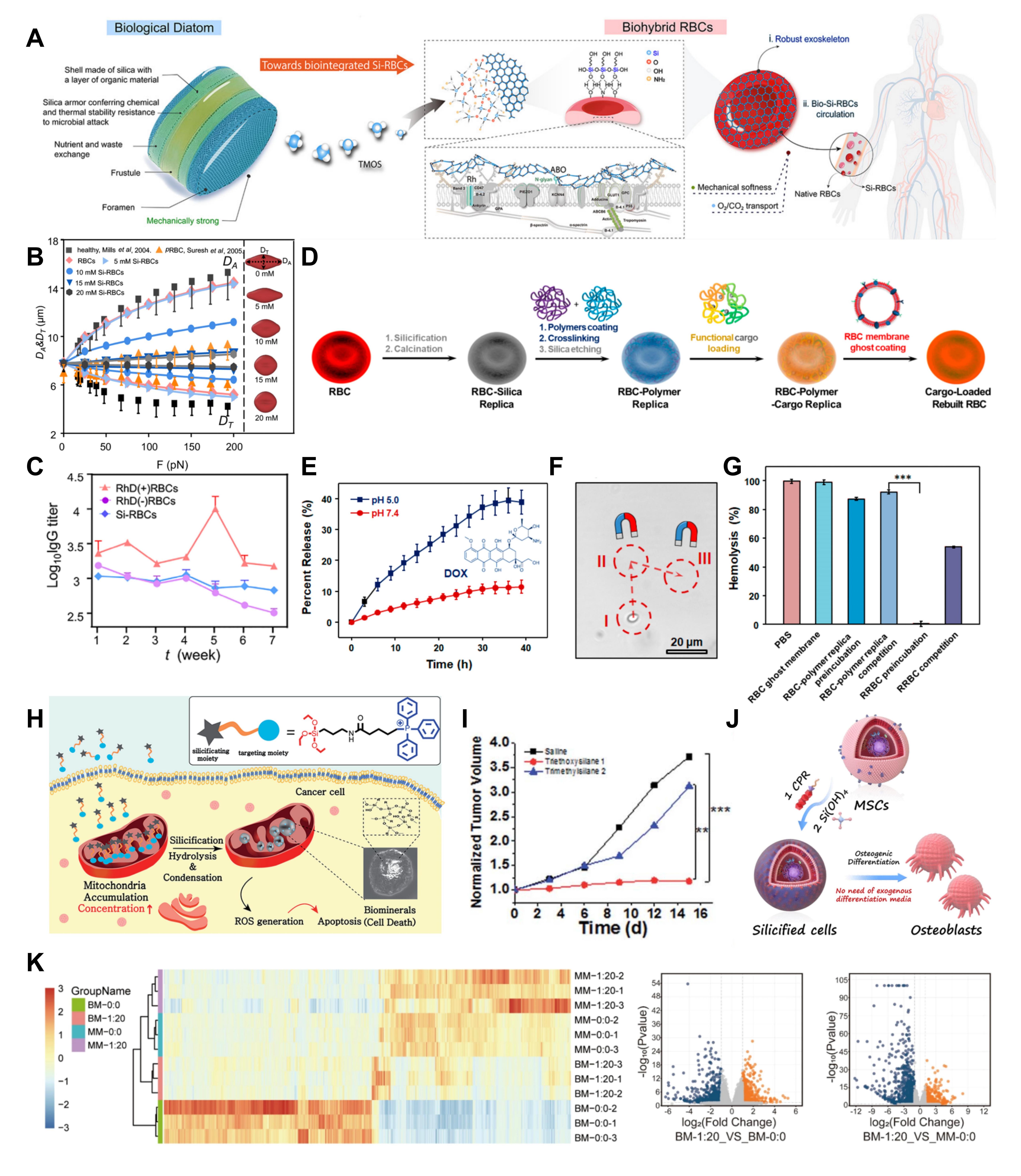
图5. 细胞尺度的生物硅化
4.宏观生物/组织尺度硅化
软组织、完整器官与整体生物样本的高保真长期保存,一直是临床病理、生物多样性保护领域的重大挑战,传统固定方法易造成样本结构变形、生物信息丢失、成像伪影等问题。宏观尺度的生物硅化技术,突破了硅前体的组织渗透瓶颈,实现了从离体软组织、完整器官到多细胞模式生物的全结构高保真保存。硅生物复制技术可在鸡胚胎等完整生物样本上形成纳米级均匀硅层,高保真保留从亚细胞超微结构到器官整体形态的全层级生物特征;深度硅化技术则进一步实现了小鼠完整器官、蚯蚓等宏观生物的同步结构与基因组信息保存,常温下样本预计保存寿命近千年,模拟近百年储存后仍能保留96.36%的完整基因组信息,为临床生物样本库、生物种质资源库、博物馆标本保藏提供了全新的技术方案。
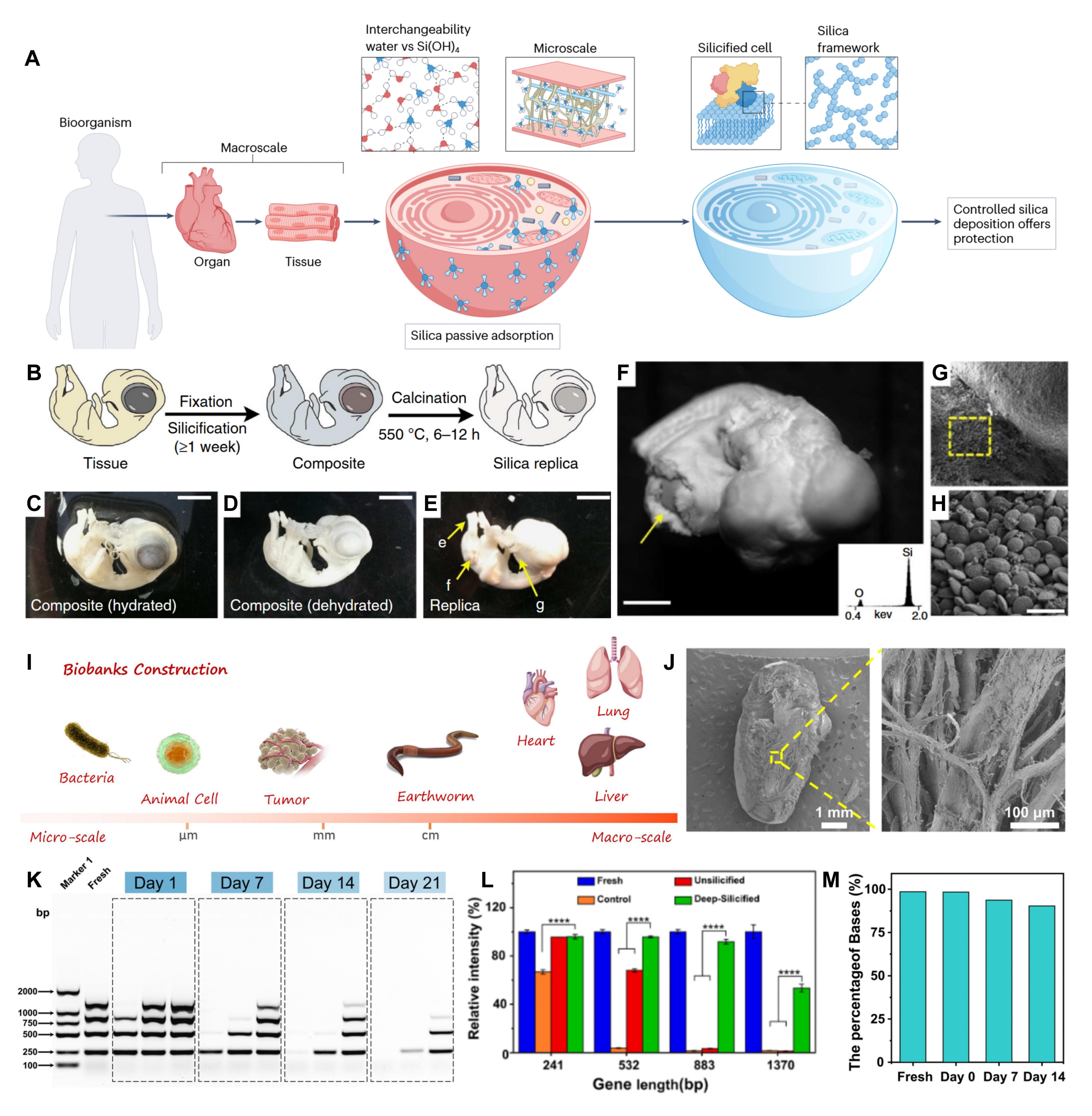
图6. 器官、组织及个体的宏观尺度的生物硅化
前景与挑战并存
尽管跨生物层级生物硅化技术在生物保存、生物医药、再生医学等领域展现出极为广阔的应用前景,但在临床转化与规模化应用的推进过程中,仍面临诸多核心挑战:硅前体在复杂生物组织中的渗透效率与沉积均匀性仍需进一步优化;不同层级硅化产物的体内降解动力学与长期代谢归宿有待更系统的阐明;硅化反应的时空精准控制与生物体内生理窗口的匹配度尚不完善;面向临床应用的标准化制备流程与质量控制体系仍未建立。
针对上述挑战,文章也提出了四个未来值得重点关注的发展方向:结合合成生物学定向进化与AI蛋白设计技术,开发催化效率更高、靶向性更强的硅化调控元件,实现硅化过程从分子到组织尺度的可编程精准调控;拓展生物硅化在NK细胞、巨噬细胞等更多免疫细胞治疗平台中的应用,开发新型通用型细胞治疗产品;联合免疫检查点抑制剂、STING激动剂等免疫调控分子,构建基于硅化技术的协同抗肿瘤免疫治疗策略;开发可逆、动态响应型生物硅化体系,实现对生命体系功能的精准、可逆调控,推动从“静态结构保存”向“动态功能调控”的范式升级。
“跨生物层级生物硅化”并非单纯的材料合成技术,而是聚合化学、材料科学、合成生物学与免疫生物学深度交叉融合的创新成果。它打破了无机材料与生命系统之间的传统边界,为生物资源保藏、生物医药开发、再生医学研究注入了全新的可能,推动相关领域迈向精准化、高效化、普适化的全新阶段。未来,这一技术必将在多学科的协同发展中,走出一条兼具科学创新价值与产业转化潜力的广阔道路。
本研究得到了国家自然科学基金(项目编号:22372061、22572061)、广东省科技计划项目(项目编号:2024B1111130002)、广州市科技计划项目(项目编号:2024A03J0163)以及中央高校基本科研业务费专项资金的资助。