朱伟教授课题组在Advanced Science发表论文:基于红细胞和MOF-级联酶的生物功能复合体用于高尿酸血症治疗
近日,华南理工大学生物科学与工程学院朱伟教授课题组在国际著名期刊Advanced Science(IF=17.52)杂志上在线发表题目为“Synthetic Biohybrids of Red Blood Cells and Cascaded-Enzymes@ Metal–Organic Frameworks for Hyperuricemia Treatment”的研究论文。博士研究生李泽宇和硕士研究生薛烈聪为该文共同第一作者,华南理工大学生物科学与工程学院为第一单位。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202305126
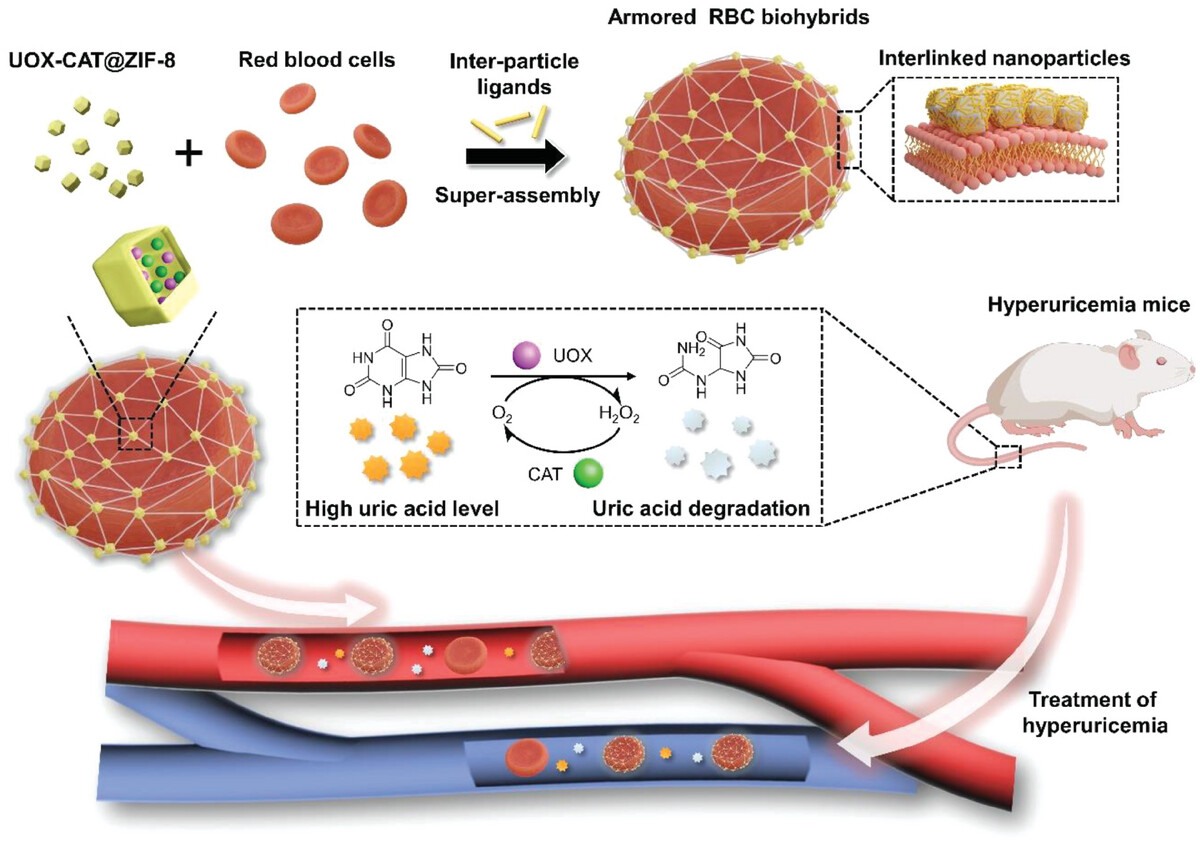
图1. 基于红细胞和MOF-级联酶的人造生物杂合体用于高尿酸血症的治疗示意图
近年来,随着人们生活水平的不断提高,饮食结构也发生了翻天覆地的变化。随之而来的是,高尿酸血症的发病率逐年攀升,且呈年轻化趋势。长期高尿酸血症可能导致痛风,并增加心脑血管疾病、代谢综合征、肾脏疾病患者的死亡率。
高尿酸血症是指机体嘌呤代谢紊乱,尿酸(UA)分泌过多或肾脏排泄功能障碍,使尿酸在血液中积聚的状态。目前主流的治疗策略侧重于平衡尿酸的产生和排出,但是所用的药物可能产生副作用,包括药物不良反应和累积的肝脏毒性。采用尿酸酶(UOX)策略,将尿酸转化为水溶性更高且更易排出的尿囊素是另一种有效策略,然而基于UOX的治疗疗效受到多种因素制约,包括酶的低催化活性、酶的可及性、副产物(H2O2)如何快速去除、UOX的循环时间以及在体内的稳定性等,这些制约因素限制了其被进一步应用。
近日,朱伟教授课题组基于纳米粒子模块化组装的思想,开发了全新的血红细胞和MOF-级联酶(UOX-CAT)的生物功能复合体用于高尿酸血症的治疗。以功能纳米颗粒作为构筑基元,通过模块化组装方式将其可控组装于血红细胞表面形成全新血红细胞超组装体。该组装体兼顾血红细胞的结构和功能(载氧和长循环能力),同时颗粒的模块化引入可赋予其多功能集成效应,包括颗粒在血红细胞表面的“搭便车”效应可显著提升其循环半衰期,血红细胞提供氧气分子可辅助尿酸向尿囊素的加速转化,UOX在纳米颗粒内的负载可提升其催化活性、稳定性和降低酶降解风险,而尿酸降解产生的H2O2可被进一步被CAT酶清除避免积累。新型血红细胞基药物载体的构建为高尿酸血症的治疗提供了全新的思路。
为了实现最佳的级联催化活性,对两种酶(UOX 和 CAT)的负载比进行了优化。 体外实验结果显示,当UOX与CAT的摩尔比≤4:1时,副产物H2O2可以被完全降解,而在4:1的摩尔比下可观察到最快的UA降解速率。由于提高外源酶的稳定性对于体内应用至关重要,进一步考察了pH、温度、胰蛋白酶处理等几种环境对治疗性酶活性的影响。结果发现,封装在 ZIF-8框架中的UOX与游离状态相比,其对环境的抗力明显增强,包括:1)即使在70℃高温条件,封装的UOX的活性仍然留有60%,是游离UOX活性的2倍;2)在宽的pH测试范围内,包封的UOX 的残留活性高于游离UOX;3)在胰蛋白酶处理下,在ZIF-8内封装的UOX酶活性下降缓慢,在 40 分钟内仍能保持在 80% 以上活性。
受益于红细胞的“搭便车效应”,封装的 UOX 可以避免体内酶的快速降解和系统清除,从而有效保持其内在酶促活性,实现持久催化。体内实验结果表明,所获得的血红细胞功能复合体可以在2小时内使急性高尿酸血症模型小鼠的UA水平正常化,并且清除半衰期为49.7±4.9小时,比游离UOX的清除半衰期(14.2 ± 1.7 小时)提升了3倍以上。
总而言之,与之前报道的基于纳米材料的 UOX 制剂不同,“血红细胞功能复合体”中的固定化 UOX 可以避免体内的快速酶促降解和系统清除,并通过其搭在红细胞上的方式确保 UOX 与 UA 的可及性,从而有效地维持其酶促活性。 此外,血红细胞功能复合体的制
方法简单、快速,并且方法具有普适性和可拓展性。同时,CAT介导的H2O2消除进一步避免了WBC、LDH水平的升高以及主要器官的病理变化。该工作通过在活细胞载体上组装功能纳米材料展示了人工生物增强的力量,为创新药物输送系统的研发带来了全新的思路。
该研究得到了国家自然科学基金及广东省自然科学基金等项目的支持。