杜红丽教授课题组在mBio上发表论文:人宿主体内SARS-CoV-2突变多样性揭示其体内进化特征及免疫逃逸模式
近日,华南理工大学生物科学与工程学院杜红丽教授课题组在美国微生物学会期刊mBio(中科院top期刊)上在线发表题为“SARS-CoV-2 within-host diversity of human hosts and its implications for viral immune evasion”的研究论文。硕士研究生席彬彬为论文第一作者,杜红丽教授为通讯作者(https://journals.asm.org/doi/full/10.1128/mbio.00679-23)。据悉,席彬彬为华南理工大学生物科学与工程学院2021届生物技术专业毕业生,目前已完成4项关于新冠病毒的研究。
SARS-CoV-2持续进化,部分突变极大的增强了SARS-CoV-2的感染能力、传播能力和免疫逃逸能力。从源头上看,这些突变应该产生于病毒感染宿主后的体内进化过程。杜红丽课题组(Bai et al., IJID. 2020;Xi et al., CSBJ. 2021a;Xi et al., CSBJ. 2021b;Xi et al., Virues 2022)及国内外之前的基于组装基因组的宏观进化分析很难揭示SARS-CoV-2体内进化特征及免疫逃逸机制,因此该课题组重新利用近20万SARS-CoV-2全基因组高深度测序数据,揭示了SARS-CoV-2在人类宿主体内的突变多样性、突变的主要模式、潜在的突变驱动因素和序列偏好性以及突变的选择过程等。
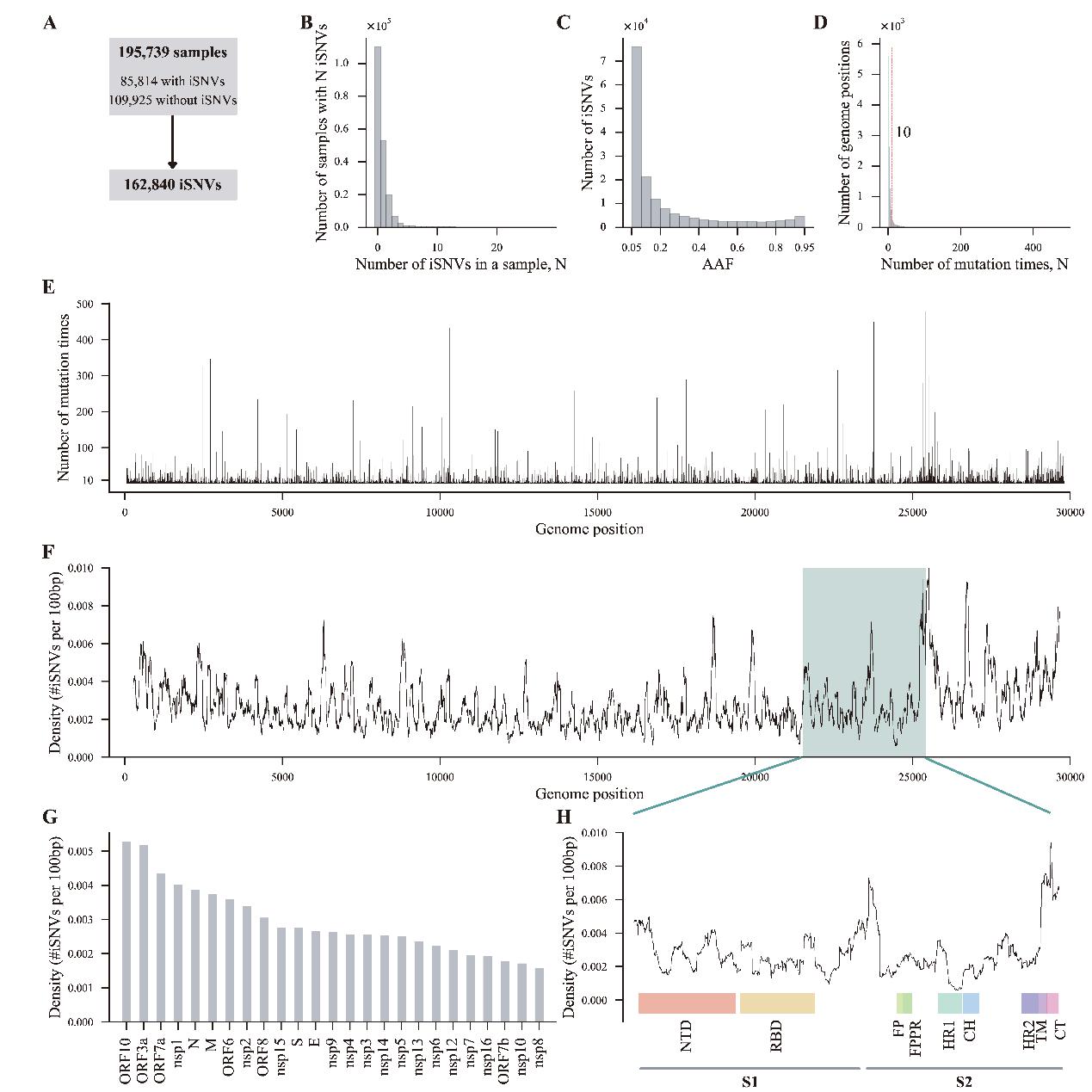
图一:SARS-CoV-2宿主内多样性及体内突变在基因组上的分布
ZAP蛋白是先天性免疫的重要组成部分。它能够识别单链RNA病毒CpG二核苷酸,并招募相关蛋白降解病毒RNA,从而起到抗病毒的作用。先前研究发现,由于对人类宿主的适应性进化,SARS-CoV-2基因组的CpG含量逐渐降低。通过分析体内突变对基因组CpG含量的影响,该研究发现CpG获得性体内突变经受了更强的选择作用,因而丢失的更快。结合SARS-CoV-2传播瓶颈较窄的特征,该研究对SARS-CoV-2基因组CpG含量随时间逐渐降低的原因进行了阐述。

图四:体内突变对SARS-CoV-2基因组序列CpG含量的影响
S蛋白作为人体适应性免疫的主要靶点,其表位的变化会降低先前感染或注射疫苗诱导产生的抗体的中和能力。该研究发现,S蛋白上非同义体内突变构成了一个免疫逃逸突变库。如果这些突变在病毒群体中固定,SARS-CoV-2的免疫逃逸能力将进一步增强。
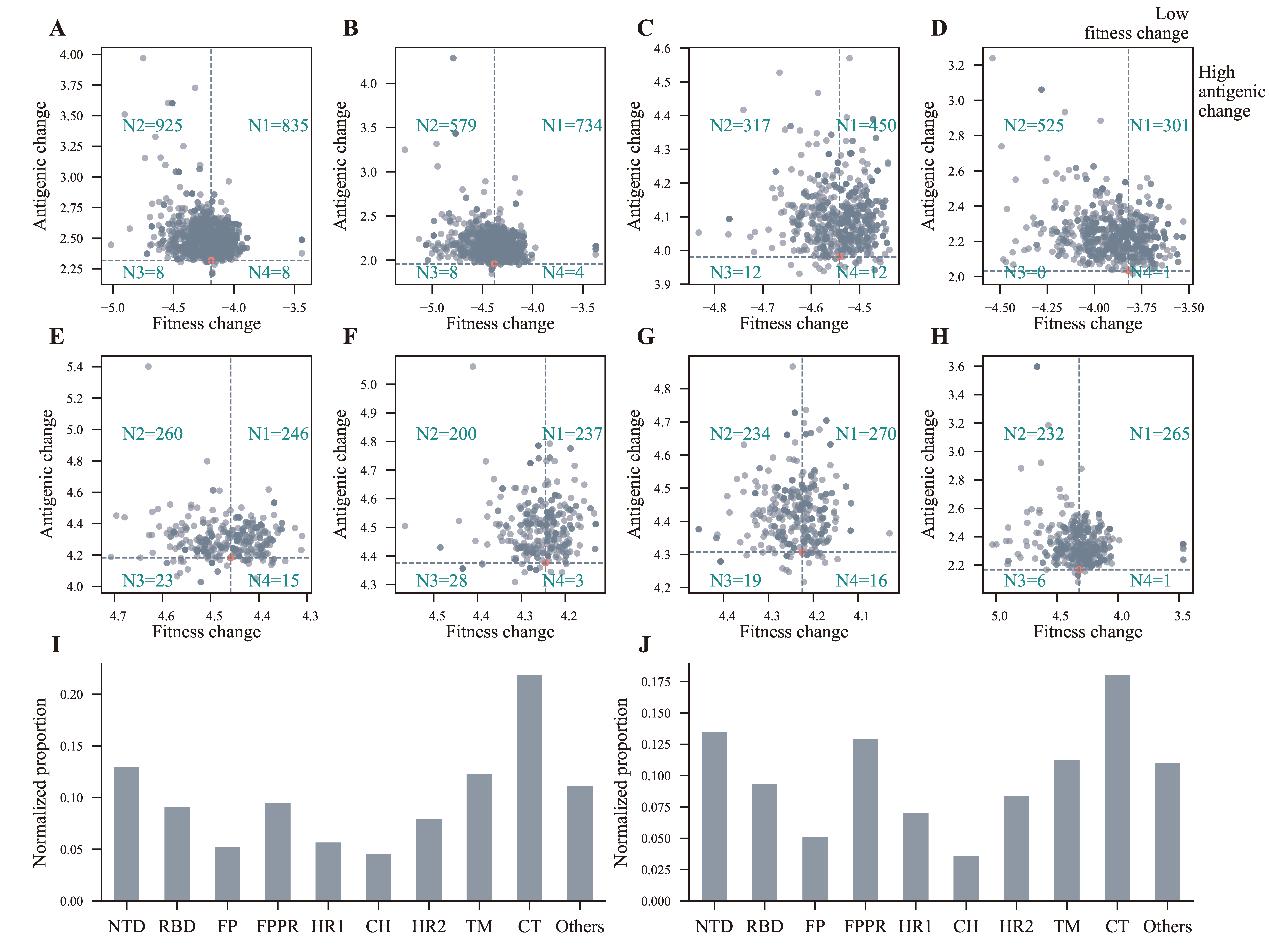
图五:S蛋白非同义突变对病毒适应性及S蛋白抗原性的影响
总之,该研究对SARS-CoV-2体内突变多样性特征进行了系统性描述,并发现SARS-CoV-2采取不同的进化策略来逃避先天性和适应性免疫。
该项工作得到了广东省重点研发计划(2019B020226001) 和国家重点研发计划(2018YFC0910201)的资助。
课题组其他相关论文链接:
https://doi.org/10.1016/j.ijid.2020.08.066
https://doi.org/10.1016/j.csbj.2021.04.002
https://doi.org/10.1016/j.csbj.2021.09.002
https://doi.org/10.3390/v14030454