朱伟教授课题组受邀在Matter发表评述:自体肿瘤全细胞疫苗:低温硅化疫苗
近日,华南理工大学生物科学与工程学院朱伟教授受邀在Matter (IF=19.967)上撰写Preview文章“Autologous whole-cell cancer vaccination: Cryogenic silicified vaccines”。文章介绍了最近发表在Nature Biomedical Engineering上新开发的低温硅化癌症疫苗。该疫苗可以结合病原体相关分子模式,为个性化免疫治疗提供保护和治疗效果。同时该方法有望在脱水和复水后长期储存而不丧失功效,并且可能适用于多种肿瘤类型。华南理工大学生物科学与工程学院博士后陈韵为第一作者,2021级硕士生郭思诗参与其中,朱伟教授为通讯作者,华南理工大学为第一单位。论文链接:https://doi.org/10.1016/j.matt.2022.05.025
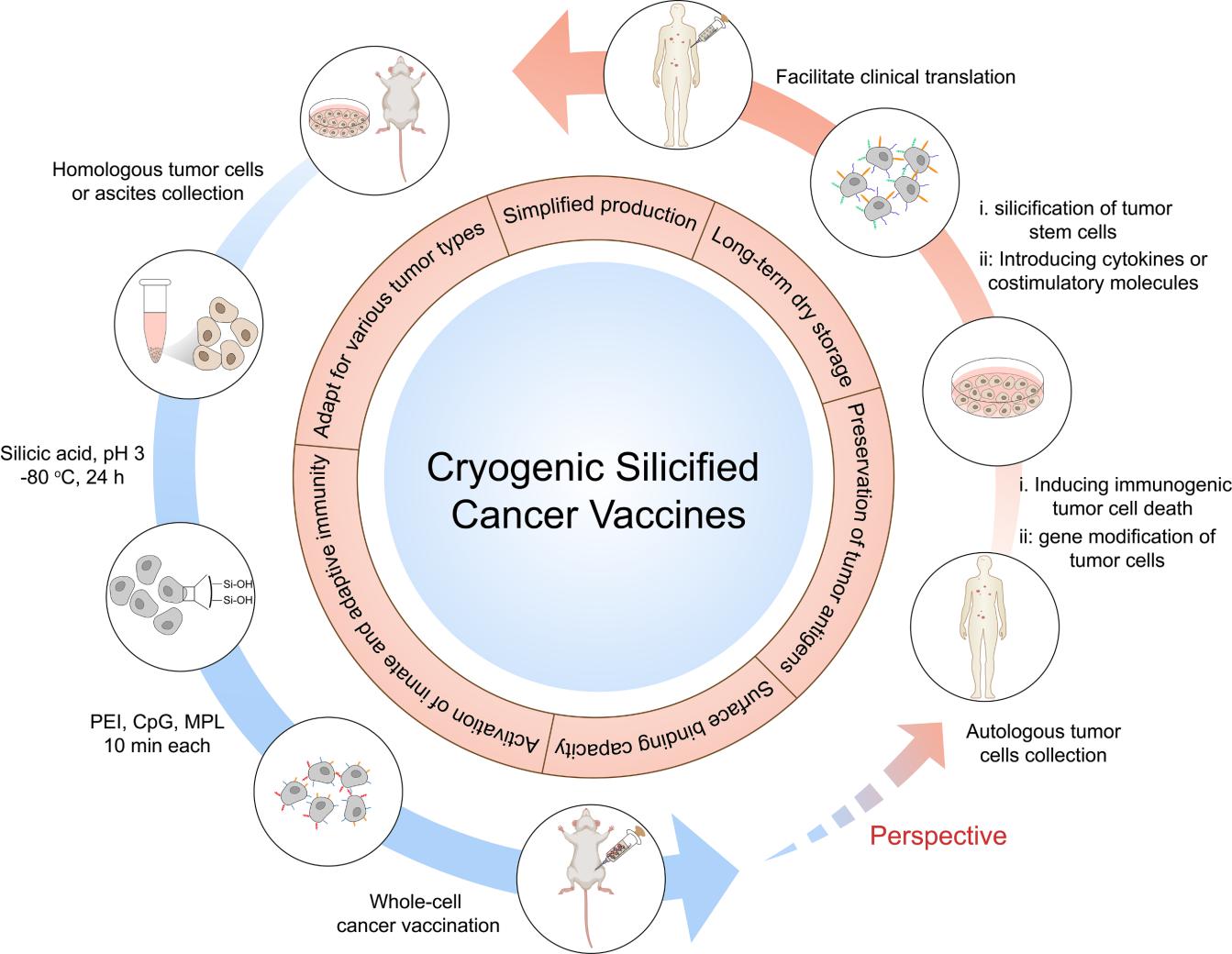
图1. 低温硅化技术制备自体全细胞肿瘤疫苗
肿瘤细胞疫苗,是指通过从患者自体或同种异体的肿瘤组织中提取肿瘤细胞作为免疫原,经灭活处理后使瘤细胞丧失致瘤性,但仍保留其免疫原性。在肿瘤治疗,抑制肿瘤转移和防止肿瘤复发上能够引发有效持久的抗肿瘤特异性反应,展现出良好的应用前景,被认为是一种可靠和有效的肿瘤免疫治疗手段。文章介绍了Guo等人最近在Nature Biomedical Engineering上新报导的低温硅化癌症疫苗的工作,其通过低温硅化肿瘤细胞实现个体化肿瘤免疫治疗。该策略可在短时间内(24小时之内)简单高效地制
出癌症疫苗。同时,该疫苗在脱水和和复水后仍能在室温中保持等价的效力。相比之下,临床试验的辐照全细胞疫苗(IR-Vac)在复水后具有聚集等问题。来自患者自体肿瘤细胞的全细胞疫苗具有一整套肿瘤特异性抗原及肿瘤相关抗原,可引起特异性免疫反应。此外,该研究通过修饰硅化肿瘤细胞表面的病原体相关分子模式(pathogen-associated molecular patterns, PAMPs),即toll样受体(Toll-like receptor, TLR)配体,能够促进树突状细胞的活化及T细胞加工和呈递肿瘤抗原。
尽管该研究取得了一定的突破,但安全有效的癌症疫苗的开发还面临着肿瘤细胞免疫原性不足、肿瘤异质性高等挑战。在评述中,作者提出未来低温硅化癌症疫苗可通过进一步改进,以解决其局限性,如以免疫原性的方式诱导肿瘤细胞死亡或对肿瘤细胞进行基因修饰,以增加其免疫原性;在硅化表面引入细胞因子或共刺激分子以增强免疫反应等。与此同时,作者认为,低温硅化的肿瘤细胞疫苗具有在临床应用上应用的潜力。