团队杜金志教授等在Science Bulletin期刊上发表最新研究成果
近日,华南理工大学杜金志、王领联合中山大学附属第一医院林润等研究人员,在肿瘤免疫治疗领域取得新进展。团队开发了一种名为“药效转录组学特征富集分析(PSEA)”的全新高通量药物组合预测平台,并结合可注射水凝胶药物递送系统,成功实现了对肿瘤相关巨噬细胞的精准重编程,显著抑制了肿瘤生长、复发与转移,为实体瘤治疗提供了极具潜力的新策略。相关成果以“Pharmacotranscriptomics-based discovery and hydrogel-mediated delivery of drug combinations for potentiated cancer immunotherapy”为题,发表于 Science Bulletin。
研究亮点
1. 组学指导新药发现:本研究开发的PSEA方法,通过整合药物扰动的大规模转录组数据库(LINCS),能够高效、精准地从海量化合物中预测出能与已知免疫激动剂(R848)协同增效的潜在药物伴侣,将传统的药物组合筛选从“大海捞针”转变为“按图索骥”。
2. 局部精准递送:团队设计了基于PLGA-PEG-PLGA聚合物的温敏水凝胶用于递送药物组合(MIT/R848@Gel)。该制剂在室温下为可注射的液体,注射到肿瘤周边后,在体温下迅速转变为固体凝胶,形成长效药物储库,实现药物的局部、可控、缓释递送,极大提高了药效并降低了全身毒性。
3. 疗效全面且持久:在多种高度恶性肿瘤模型(包括小鼠原位乳腺癌、转基因自发性乳腺癌及兔VX2肝癌术后模型)中,MIT/R848@Gel局部治疗不仅可以高效抑制原发肿瘤,更展现出强大的预防术后复发、抑制远端转移的能力,并能诱导产生持久的免疫记忆,实现肿瘤长期缓解甚至“治愈”。
4. 机制清晰明确:该组合疗法能有效将肿瘤内免疫抑制性的M2型巨噬细胞重编程为具有抗肿瘤活性的M1型,进而激活并招募大量的细胞毒性T细胞进入肿瘤,逆转肿瘤免疫抑制微环境,从根源上激发系统性抗肿瘤免疫反应。
研究背景
近年来,以免疫检查点抑制剂为代表的癌症免疫疗法取得了革命性进展。然而,对包括三阴性乳腺癌、肝癌在内的诸多“冷肿瘤”,其响应率仍然有限。肿瘤微环境中大量存在的、具有免疫抑制功能的肿瘤相关巨噬细胞(TAMs)是导致免疫疗法失效的关键“帮凶”之一。因此,将TAMs从“助纣为虐”的M2型逆转为“除暴安良”的M1型,是改善免疫治疗的热点方向。尽管已有R848等药物可激活巨噬细胞,但单药疗效欠佳。如何找到更高效的药物或药物组合,并解决药物体内递送效率低、副作用大的难题,是当前领域面临的巨大挑战。
成果简介
研究团队以R848为模型药物,建立了PSEA预测平台。该平台通过分析R848处理细胞后的核心转录特征,并与LINCS数据库中数十万种化合物扰动细胞的基因表达谱进行比对和富集分析,精准预测出化疗药物米托蒽醌(MIT)是与R848协同作用的最佳候选。随后,团队构建了可共同负载MIT和R848的温敏水凝胶MIT/R848@Gel。在多种临床前模型中,该凝胶显示出卓越疗效:1)在原位4T1乳腺癌模型中,MIT/R848@Gel实现了近90%的肿瘤抑制率,并显著延长小鼠生存期;2)在模拟人乳腺癌自发成瘤与转移的MMTV-PyMT转基因小鼠模型中,MIT/R848@Gel在术后103天仍保持100%存活率,并可强效抑制远端肿瘤生长和肺转移;3)在更恶性的兔VX2肝癌术后模型中,应用MIT/R848@Gel后,术后三周CT监测未发现任何肿瘤复发迹象,而对照组已出现明显复发。
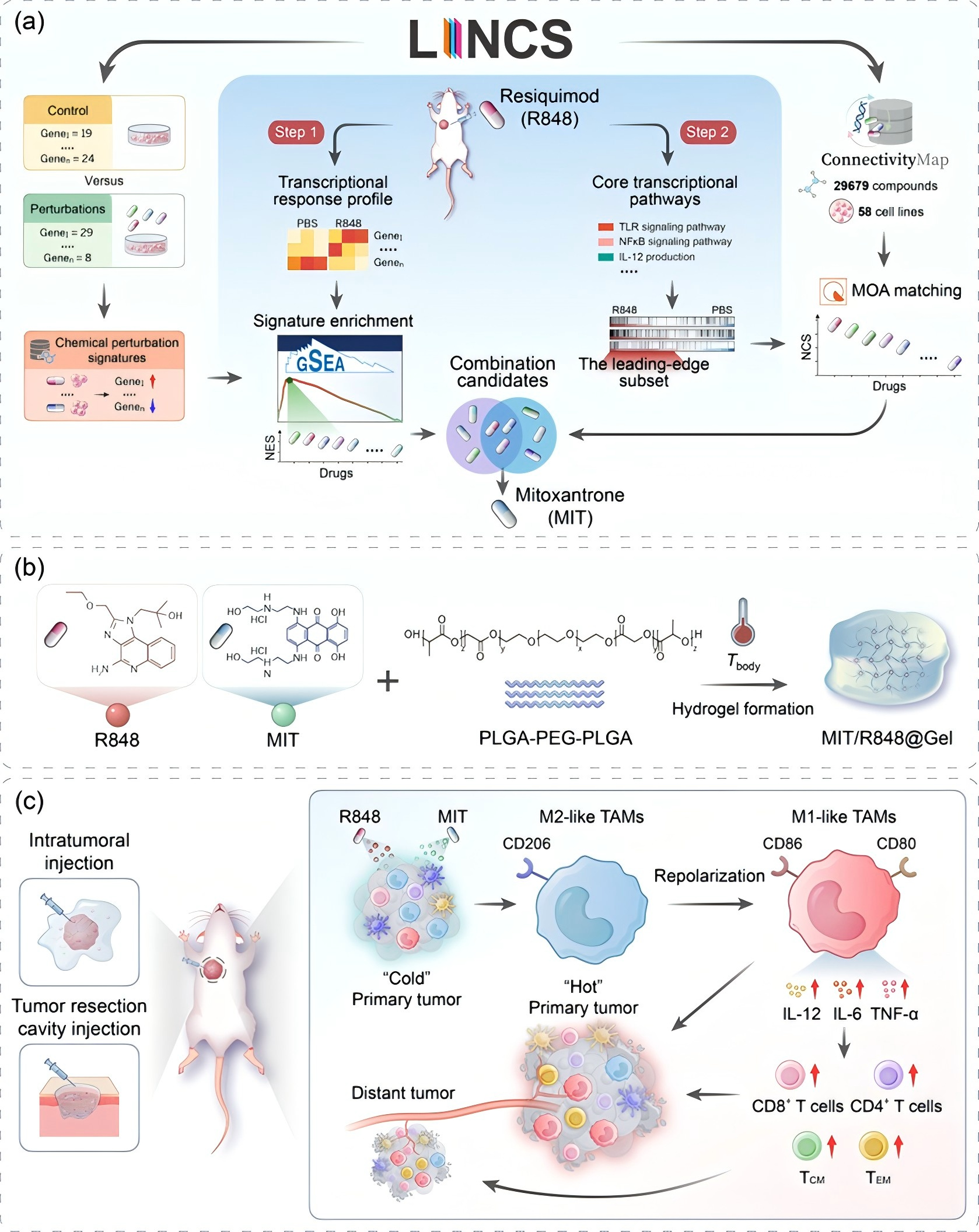
基于PSEA的药物发现与水凝胶递送用于肿瘤免疫治疗的示意图。(a)PSEA方法筛选MIT作为R848组合搭档的流程图;(b)温敏水凝胶共载MIT和R848;(c)作用机制:水凝胶重编程巨噬细胞并激活全身性抗肿瘤免疫。
文章信息
Rong Liu, Hui-Han Yu, Wei-Rong Li, Jia-Si Wu, Jing-Yang Zhang, Jia-Qi Luo, Yu Pang, Ying Chen, Yan-Dan Yao, Run Lin, Ling Wang, Jin-Zhi Du, Jun Wang. Pharmacotranscriptomics-based discovery and hydrogel-mediated delivery of drug combinations for potentiated cancer immunotherapy. Science Bulletin, 2026 doi: 10.1016/j.scib.2026.01.022
