熊梦华教授团队在Nano Research期刊上发表最新研究成果
近日,华南理工大学生物医学科学与工程学院熊梦华教授团队在国际学术期刊Nano Research发表了以“Tailoring pH-ultra-sensitive oncolytic polyesters via a manageable polymer blending strategy”为题的研究成果,中山大学孙逸仙纪念医院2023级博士生苏婵娟、学院2023级药学专业硕士生曾雨萱、中山大学孙逸仙纪念医院2023级硕士生张世华、中山大学孙逸仙纪念医院博士后袁月玲为本文共同第一作者,中山大学孙逸仙纪念医院鲍燕研究员、熊梦华教授、博士后汪吉红为本文共同通讯作者。
溶瘤材料通过裂解细胞膜高效杀伤肿瘤细胞,在克服耐药性与肿瘤异质性方面展现出独特优势,但如何实现对肿瘤细胞的选择性裂解、同时避免损伤正常组织细胞,仍是该领域的关键挑战。针对肿瘤酸度存在的个体差异与区域异质性,研究团队前期基于肿瘤组织(pH 6.5–7.0)与正常生理环境(~ pH 7.4)之间微小的pH差异,发展了pH超敏溶瘤高分子,可在0.1–0.2 pH差异下实现活性的“开/关”控制。然而,传统化学合成方法在调节溶瘤材料响应pH阈值时存在合成繁琐、调控精度受限等难题。
为解决上述问题,团队合成了两种结构明确、具有不同响应pH阈值的交替聚酯,并通过简便可控的聚合物共混策略,使二者在水溶液中自组装成杂化聚酯纳米颗粒。通过改变两种聚合物的质量比,杂化纳米颗粒的pKa值可在6.37至7.04之间实现连续精准调控。在肿瘤微酸环境下,该材料被激活后能与肿瘤细胞膜阴离子磷脂发生强烈的特异性结合,30分钟内导致细胞膜破裂及内含物泄露,实现不依赖于内吞作用或细胞凋亡通路的“物理性”死亡。静脉注射下,该系列材料最大耐受剂量高、无明显脏器毒性,其中最优配方在胰腺癌、结肠癌、乳腺癌等多种小鼠模型中均疗效显著,部分小鼠实现肿瘤完全消退。
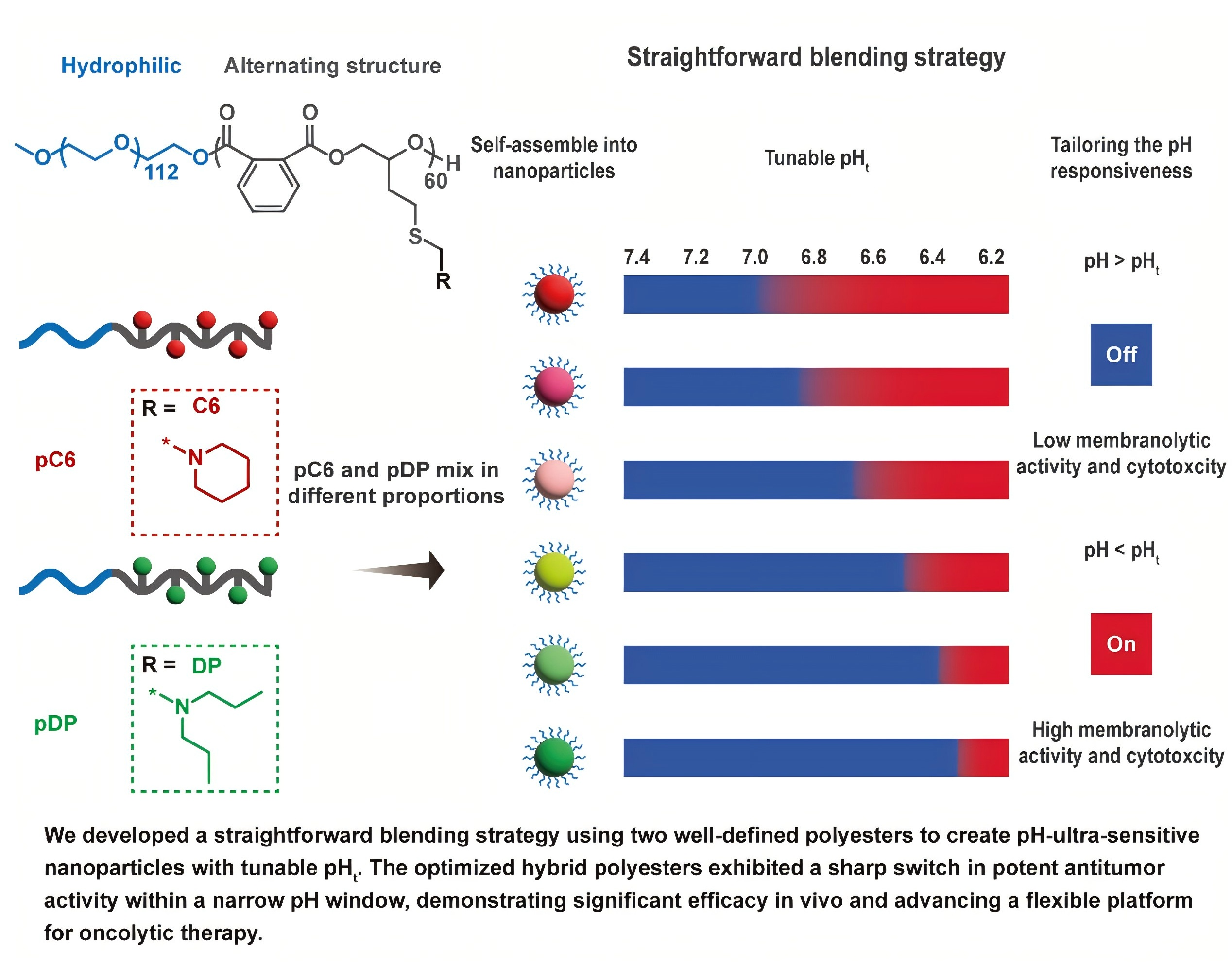
该研究以简单的物理共混策略替代复杂的化学合成,在保持聚合物精确结构的基础上,实现了溶瘤材料响应pH阈值的简便、灵活调控,为应对肿瘤微环境的异质性提供了新思路,也为推动安全高效的靶向溶瘤药物走向临床提供了极具潜力的通用策略。
附原文链接:https://doi.org/10.26599/NR.2026.94908441
