王均教授、杨显珠教授、苏苗博士等在Science Advances期刊上发表肿瘤纳米疫苗最新研究成果
近日,华南理工大学生物医学科学与工程学院王均教授、杨显珠教授研究团队在肿瘤纳米疫苗研发领域取得重要突破,相关研究成果以“TLR9-activating cholesterol azetidine derivative–assisted therapeutic vaccines for cancer immunotherapy”为题发表于《Science Advances》。华南理工大学生物医学科学与工程学院博士后陈俊彬和苏苗为论文共同第一作者,王均教授、杨显珠教授、苏苗博士为共同通讯作者。
治疗性肿瘤疫苗在诱导内源性抗原特异性T细胞反应以对抗肿瘤方面展现出巨大潜力,是当前肿瘤免疫治疗的前沿方向。如何有效协同先天免疫的激活与抗原的精准递送,一直是限制肿瘤疫苗临床疗效的重大障碍。肿瘤抗原与免疫佐剂的协同联合是癌症疫苗诱导高效抗肿瘤免疫的关键;利用纳米技术与载体材料制备的纳米载体,能够解决癌症疫苗制剂在体内的递送难题,已成为癌症疫苗开发的前沿方向。
传统策略集中在利用纳米载体将肿瘤抗原和佐剂共同封装于同一纳米载体,但由于不同成分(如亲水性和电荷)的理化性质差异,共同递送策略往往面临着兼容性差、共封装效率低、释放同步性控制差、亚细胞时空定位协调不足等瓶颈。基于此,开发本身就具备免疫佐剂活性的纳米载体材料,可有效简化疫苗组分和制备工艺,提供了一种极具吸引力的替代方案。
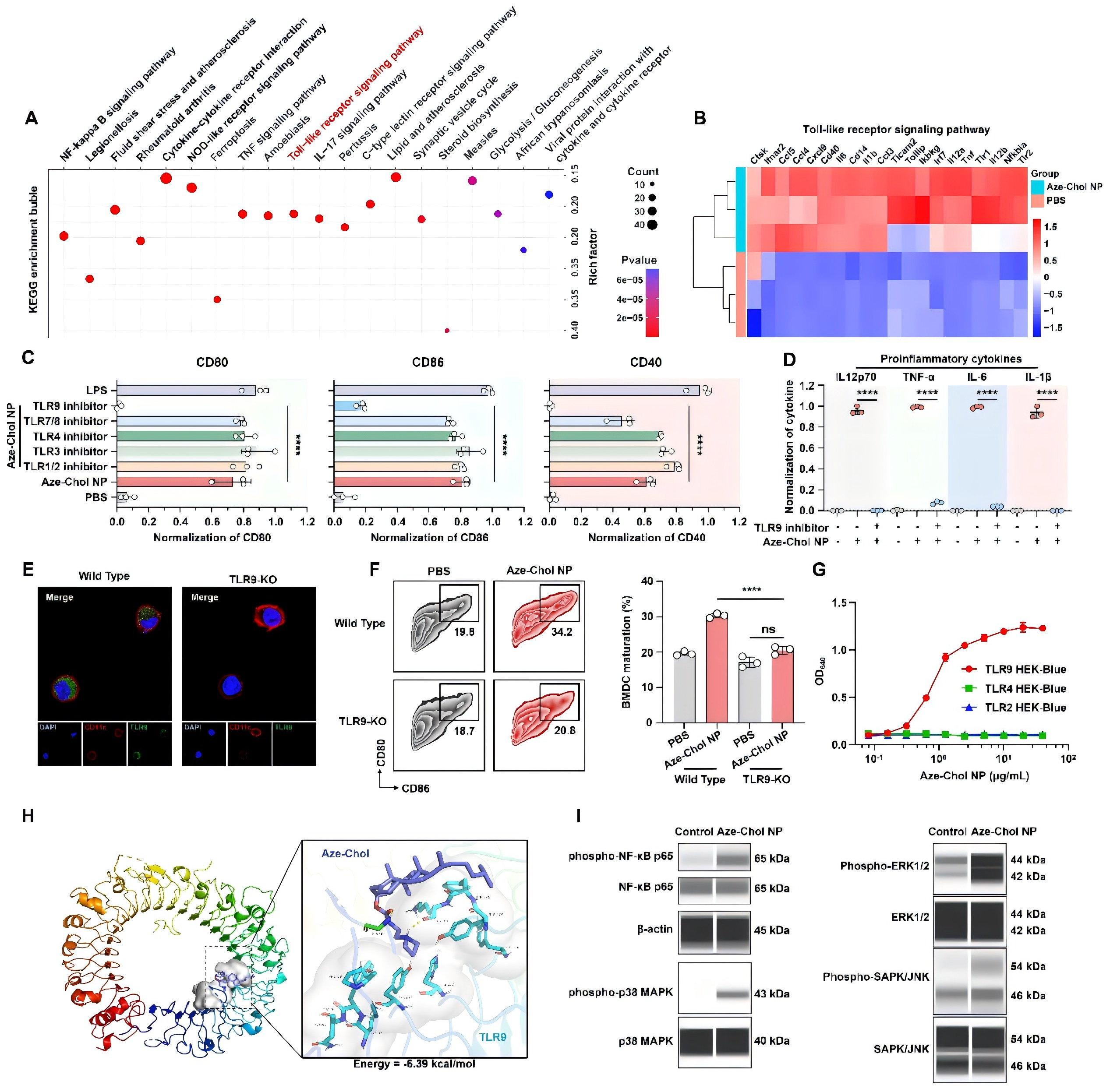
为此,研究团队创新性地开发了一种具有内源性先天免疫佐剂活性的纳米载体平台(Aze-Chol NP)。该研究通过系统筛选带有不同叔胺杂环头部基团的胆固醇衍生物,发现带有氮杂环丁烷(azetidine)头部的胆固醇衍生物能够作为Toll样受体9(TLR9)的特异性强效激动剂。基于此构建的聚合物纳米载体Aze-Chol NP,在无需额外添加佐剂的情况下,能够直接通过TLR9信号通路诱导树突状细胞(DCs)的成熟与激活,并高效地将蛋白质或多肽抗原递送至淋巴结,显著提高抗原交叉呈递与特异性细胞毒性T细胞反应。
本研究开发了兼具抗原递送与免疫激活双重功能的Aze-Chol NP纳米载体,为癌症疫苗提供了一种结构明确的新型自佐剂活性递送平台,同时为TLR9免疫激动剂的设计提供了全新的作用机制范式;不仅为设计更简单、更强效的癌症疫苗提供了全新思路,也为个性化免疫治疗提供了创新平台。
文章链接:https://www.science.org/doi/10.1126/sciadv.aeb2465
