王均教授、沈松副教授合作在Nature Communications上发表最新研究成果
自然杀伤(NK)细胞和T细胞对先天免疫系统和适应性免疫系统至关重要,在肿瘤识别和清除中发挥着互补和协调的作用。协同NK和T细胞的免疫疗法有望进一步增强抗肿瘤疗效。已有研究表明,靶向NK和T细胞表面共表达的免疫检查点分子(如NKG2A、TIGIT)可以同时激活先天性和适应性免疫反应。然而,由于肿瘤发生机制的复杂性,单一使用相应的单克隆抗体疗法在临床试验中并未取得预期疗效,突显出与其他免疫检查点抑制剂联合使用的必要性。双/多特异性抗体由于能同时靶向两个或多个靶点,具备联合治疗潜能,其中三特异性抗体能够促进三种免疫调节分子协同,是该领域最前沿的进展之一,然而目前尚无针对NK细胞和T细胞的三特异性抗体报道。
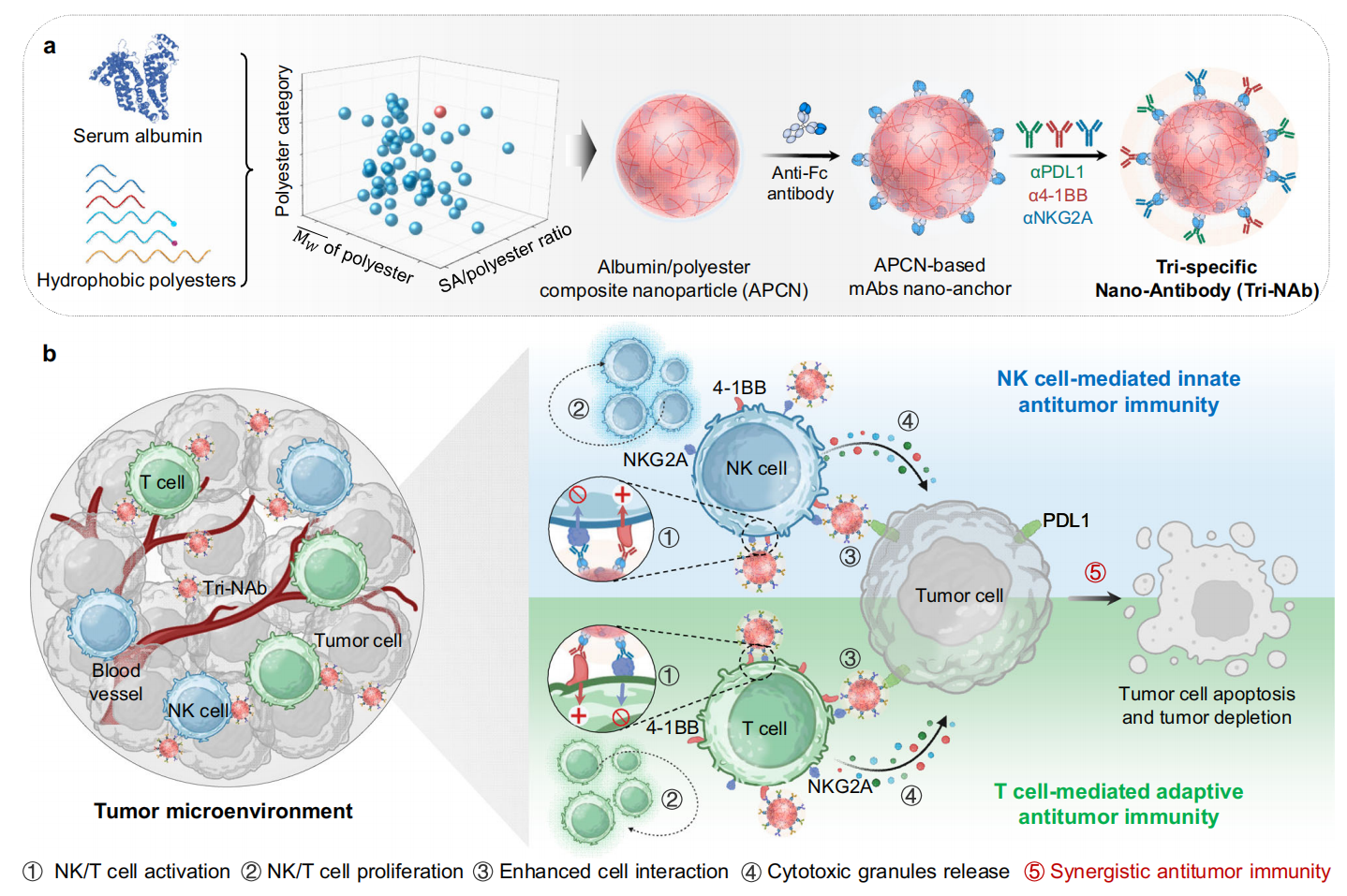
图:Tri-NAb的构建及其增强先天性和适应性抗肿瘤免疫反应的作用机制示意图。
尽管已有部分三特异性抗体被成功开发出来,但其在生产和研发上仍面临技术壁垒和成本较高、副产物多、纯化工艺复杂等问题。将多个单抗固定在纳米载体表面是构建多特异性纳米抗体(nano-antibodies, NAbs)一种有前景的策略。在之前的研究中,研究团队通过将抗IgG(Fc)抗体(αFc)偶联到氨基修饰的聚苯乙烯纳米粒上构建了一种通用型的抗体固定平台,模拟了双特异性抗体的功能,有效激活了免疫反应(Nat. Commun. 2021, 12, 1359)。然而,聚苯乙烯内核载体较差的生物相容性极大阻碍了该平台的未来应用。
在该项研究中,研究团队利用血清白蛋白和生物可降解疏水性聚酯材料发展了一种生物相容性良好的白蛋白/聚酯复合纳米粒(APCN),成功取代原有聚苯乙烯内核,解决了生物安全性问题。进一步通过在其表面固定抗PDL1、4-1BB和NKG2A(或TIGIT)抗体成功构筑了能协同NK和CD8+ T细胞的类三特异性抗体(Tri-NAb)。研究证实Tri-NAb能够有效结合NK和CD8+ T细胞,触发其激活和增殖,同时促进其与肿瘤细胞相互作用,从而引发高效的肿瘤杀伤效果。在多种小鼠肿瘤、患者来源结肠癌类器官和人源化小鼠模型中,均证实Tri-NAb通过协同NK和CD8+ T细胞显著增强抗肿瘤疗效,显示NK细胞和T细胞协同抗肿瘤免疫治疗的临床应用潜能。
该成果以“Orchestrating NK and T cells via tri-specific nano-antibodies for synergistic antitumor immunity”为题发表在国际高水平学术期刊Nature Communications上,华南理工大学生物医学科学与工程学院博士研究生叶倩妮为论文第一作者,王均教授和沈松副教授为论文的通讯作者。
文章DOI号: https://doi.org/10.1038/s41467-024-50474-y.
