团队在肿瘤特异性基因激活纳米药物方向取得研究进展
肿瘤免疫疗法近年来取得了巨大突破,有10余款免疫检查点抗体和8款CAR-T细胞疗法获批上市。然而,大多数实体瘤缺乏效应T细胞浸润,导致免疫检查点抗体无法在大多数实体瘤患者中诱导有效的抗肿瘤反应。CAR-T疗法在实体瘤治疗中效果欠佳,其中的一个重要原因是CAR-T细胞无法有效浸润至实体瘤。如何促进T细胞或CAR-T细胞高效、特异性地迁移到实体瘤中对于改善当前的免疫疗法至关重要。
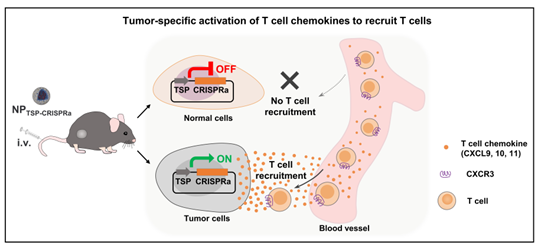
鉴于此,华南理工大学王均/许从飞团队提出了一种基于CRISPR的转录激活(CRISPRa)纳米药物,通过激活肿瘤细胞自身表达T细胞趋化因子,募集T细胞迁移浸润至肿瘤内。结果显示,瘤内注射CRISPRa基因激活纳米药物可以抑制不同实体瘤的生长,包括黑色素瘤、胰腺癌、结直肠癌和乳腺癌。此外,团队构建了肿瘤特异性的CRISPRa基因激活纳米药物,可以实现仅上调肿瘤中T细胞趋化因子的表达,而对正常组织没有影响。全身注射肿瘤特异性基因激活纳米药物可以特异性地将T细胞或CAR-T细胞招募到实体瘤中,提高免疫检查点抗体(PD-L1抗体或CTLA-4抗体)以及CAR-T细胞的抗肿瘤效果。该研究开发的特异性基因激活纳米药物为增强T细胞浸润改善实体瘤免疫治疗疗效提供了一种有前景的策略。
这项研究成果以“Gene-activating nanomedicine for the tumor-oriented infiltration of T cells to enhance immunotherapy against solid tumors”为题发表在国际学术期刊Nano Today, 2023, 52, 101992。论文的第一作者是张玥博士和赵贵博士,通讯作者是许从飞副教授和王均教授,华南理工大学为论文的第一署名单位。