团队在Aggregate杂志发表最新研究成果
肿瘤坏死因子受体超家族(TNFR)参与细胞存活、凋亡、炎症反应和细胞分化等相关信号转导,是潜在的肿瘤治疗靶点。比如,激活T细胞表面的OX40可以促进效应T细胞增殖,抑制调节性T细胞生成;激活DR5可比较特异性地诱导肿瘤细胞凋亡而不损伤正常细胞。目前有多个靶向TNFR家族成员的药物正在开展用于肿瘤治疗的临床试验,然而这些药物的临床治疗效果不一。进一步研究发现,能够诱导TNFR聚集交联的药物能更有效地激活下游信号,产生更好的疗效。
在这项研究中,华南理工大学纳米医学和生物材料研究团队在开发靶向TNFR的多价强效激动剂方向取得研究进展。该研究基于一种多聚蛋白支架,通过融合OX40L、TRAIL等靶向TNFR的配体,制备可以聚集交联TNFR的多价强效激动剂。与抗体或配体的单体相比,经过蛋白支架多聚的配体可以触发强大的TNFR下游激活信号。纳米簇状多价MV-OX40L和MV-TRAIL可以分别有效促进T细胞活化和诱导肿瘤细胞凋亡。此外,团队通过将可以结合抗体的FcR与多聚蛋白支架融合表达,开发一种通用的纳米适配子MV-FcR,用于快速制备不同的多价抗体药物。该MV-FcR可以多聚商业化的TNFR抗体激动剂,将αOX40抗体与MV-FcR直接孵育可得到多价的MV-αOX40,有效增强αOX40的抗肿瘤作用。此外,MV-FcR还可以多聚其它治疗性抗体,例如αPD-L1抗体,增强其效价。该研究为多价抗肿瘤蛋白药物的工程化提供了一种有前景的策略。
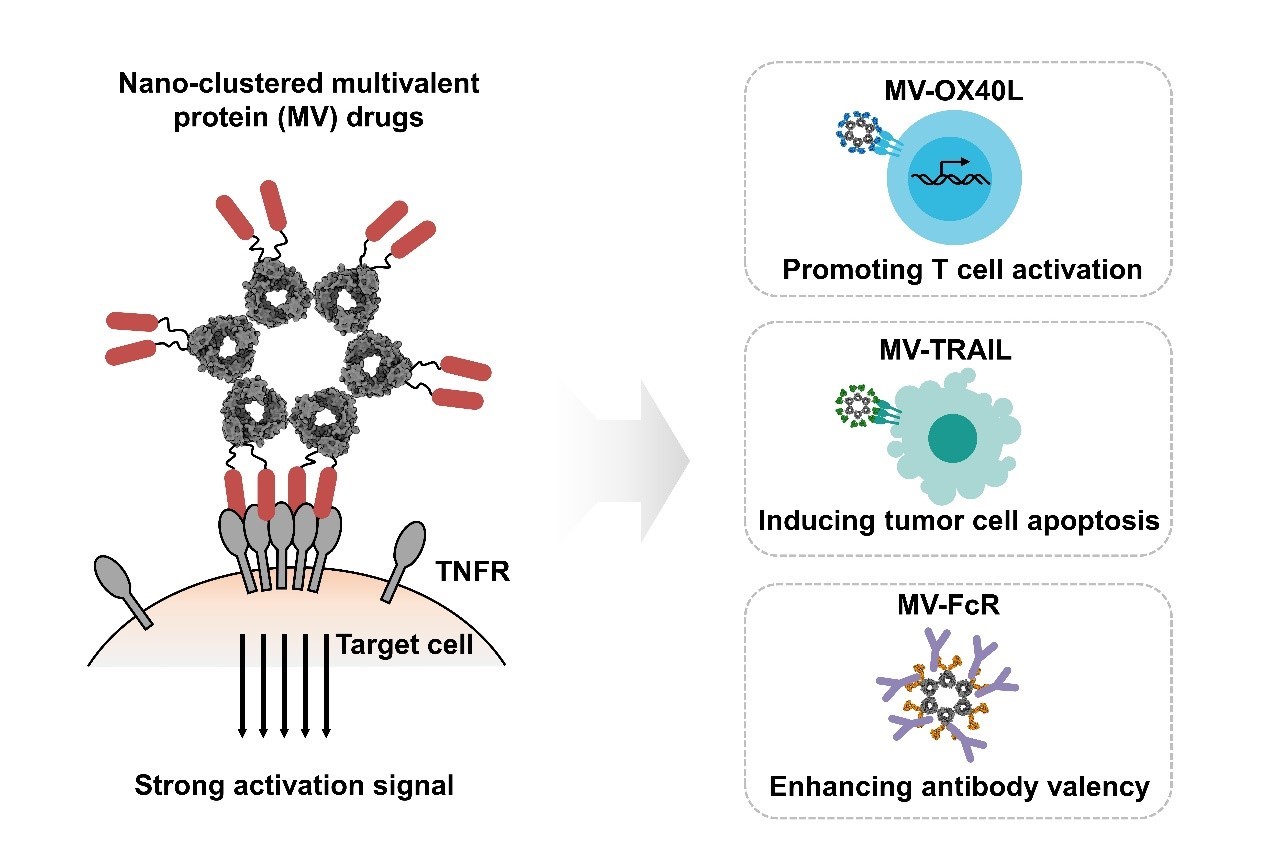
这项研究成果以“Engineering nano-clustered multivalent agonists to cross-link TNF receptors for cancer therapy”为题发表在国际学术期刊Aggregate,全文链接https://onlinelibrary.wiley.com/doi/10.1002/agt2.393。论文的通讯作者是王均教授和许从飞副教授,第一作者是张玥博士和赵贵博士,华南理工大学为论文的第一署名单位。
