团队在抗炎纳米药物方向取得研究进展
活化中性粒细胞过度浸润被认为是中性粒细胞炎症中组织损伤的主要原因。尽管程序性细胞死亡如凋亡等维持了活化中性粒细胞的稳态,但这一过程常常会被异常炎症反应破坏。与细胞凋亡过程中暴露的内源性钙网蛋白不同,外源性钙网蛋白作为“老化”信号,可启动巨噬细胞介导的程序化清除(PrCR),此过程可脱离细胞凋亡而独立存在。
鉴于此,华南理工大学王均教授和中国科学技术大学王育才教授研究团队在国际权威学术期刊ACS Nano上报道了一种纳米介导的策略,以人工老化信号刺激启动活化中性粒细胞的精准清除,并在多种炎症模型抑制炎症反应和组织损伤。
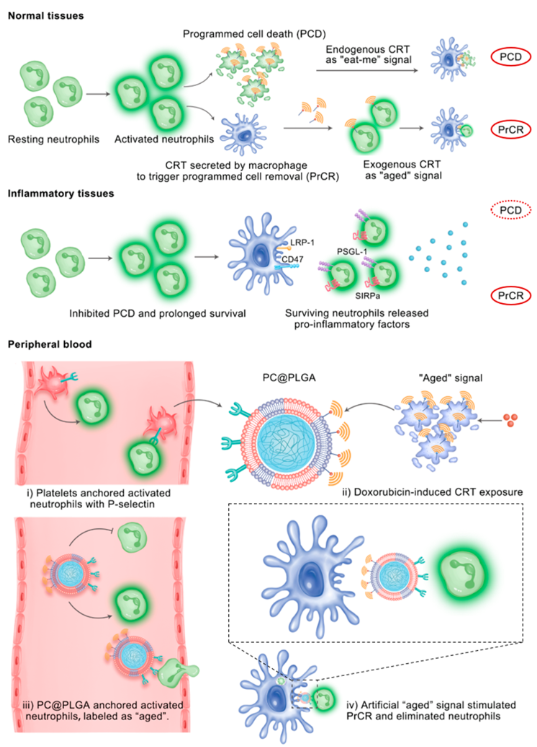
利用来源于血小板衍生细胞外囊泡(PEVs,用P表示)和来源于阿霉素处理细胞钙网织蛋白表达膜(用C表示)的杂化膜包被PLGA,以制备聚合物纳米颗粒PC@PLGA。该系统实现纳米颗粒表面“靶向”信号和“衰老”信号的双重展示,可特异性靶向活化中性粒细胞,并引发巨噬细胞对其的程序化清除。在急性肺损伤和严重急性胰腺炎的小鼠模型中,PC@PLGA可特异性靶向活化的中性粒细胞并误导巨噬细胞将其识别为“老化”中性粒细胞,然后启动PrCR以有效缓解炎症反应和组织损伤。该策略提供了一种利用纳米技术精准调控中性粒细胞命运的新思路,也为调控其他重要免疫细胞功能提供一定参考。
该成果以“Aged-Signal-Eliciting Nanoparticles Stimulated Macrophage-Mediated Programmed Removal of Inflammatory Neutrophils”为题发表在国际著名学术期刊ACS Nano。
全文链接:https://pubs.acs.org/doi/10.1021/acsnano.3c03815。
