团队在HSP70启动子驱动的基因编辑以增强巨噬细胞抗肿瘤免疫治疗方面取得研究进展
作为先天免疫细胞和抗原提呈细胞,巨噬细胞是机体的第一线防御之一,通过吞噬癌细胞并将其抗原肽呈递给T淋巴细胞(T cells),进一步激活全身的抗肿瘤免疫反应。因此,巨噬细胞介导的抗肿瘤治疗被广泛探索。不幸的是,肿瘤细胞通过表达CD47与信号调节蛋白-α (SIRPα)结合,提供“不要吃我”信号来抑制巨噬细胞的吞噬。因此,通过阻断CD47-SIRPα通路可以打破巨噬细胞的免疫抑制,增强巨噬细胞对肿瘤细胞的吞噬。然而研究表明,仅阻断CD47-SIRPα通路可能不能引起充分的吞噬作用,需要提高肿瘤细胞CRT的表面暴露为巨噬细胞提供“吃我”的信号才能进一步促进巨噬细胞的吞噬作用。
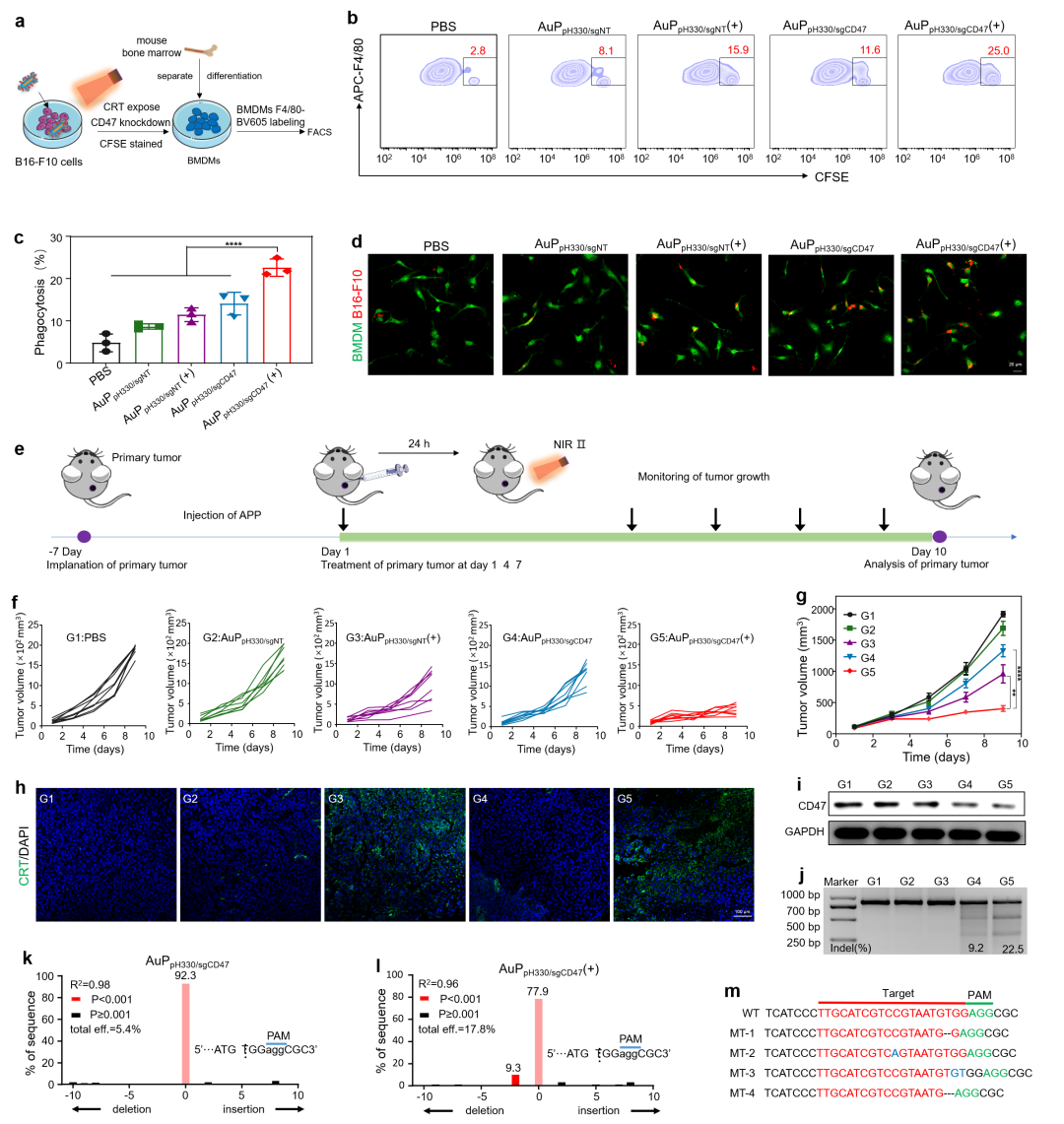
因此,为了重新唤醒巨噬细胞的识别和吞噬功能,我们设计了一种HSP70启动子驱动的基因编辑系统AuPpH330/sgCD47,该系统由PEI修饰的Au纳米棒和HSP70启动子驱动的CRISPR/Cas9质粒编辑靶向CD47, pH330/sgCD47组成。该系统在1046 nm激光下增强了肿瘤细胞CD47的敲除,阻断了“不要吃我”信号,恢复了巨噬细胞识别肿瘤细胞的能力。同时,AuPpH330/sgCD47(+)可以增强固有的CRT暴露,为巨噬细胞提供“吃我”信号,协同促进肿瘤细胞的巨噬细胞识别和吞噬,并显著增加M2-to-M1巨噬细胞复极化,最终表现出优异的肿瘤治疗效果。更重要的是,它还刺激了免疫记忆反应,以抑制远端肿瘤的生长和肺转移肿瘤的发生。由于这些优势,该策略在原发、远处和肺转移性肿瘤模型中取得了抗癌效果。因此,这种基于CRISPR/ Cas9辅助组装策略的双增强巨噬细胞吞噬的方法可以为癌症免疫治疗提供一种新的途径。
研究成果以“NIR-II Light-Driven Genetically Edited Nanoparticles with Inherent CRT-Inducing Capability for Macrophage-Mediated Immunotherapy”为题发表在国际著名学术期刊Nano Today上,黄巧仪,苏苗,赵亮为文章的共同一作。
全文链接:https://doi.org/10.1016/j.nantod.2023.101857
