团队在肿瘤特异性基因纳米药物方向取得研究进展
PD-1/PD-L1免疫检查点阻断疗法可以增强T细胞的活化杀伤功能,是有效的肿瘤免疫治疗策略。虽然目前已有多款靶向PD-1或PD-L1的抗体药物获批上市,但是大多数的癌症患者对此类药物的响应率低,约为10%—30%,无法获得满意的治疗效果。这主要由下面两方面的因素引起:一、肿瘤组织中缺乏足够的T细胞浸润;二、抗体药物静脉注射的给药方式导致药物在肿瘤中富集不足,且非特异的作用会引发一些不良反应。
针对PD-1/PD-L1阻断疗法以上两方面的不足,近日,华南理工大学王均/许从飞研究团队在国际权威学术期刊Nature Communications上发表了最新研究成果。该研究设计了一种肿瘤特异性基因纳米药物,可以有效提升肿瘤中T细胞趋化因子和PD-L1拮抗剂的水平,增强肿瘤免疫治疗效果。
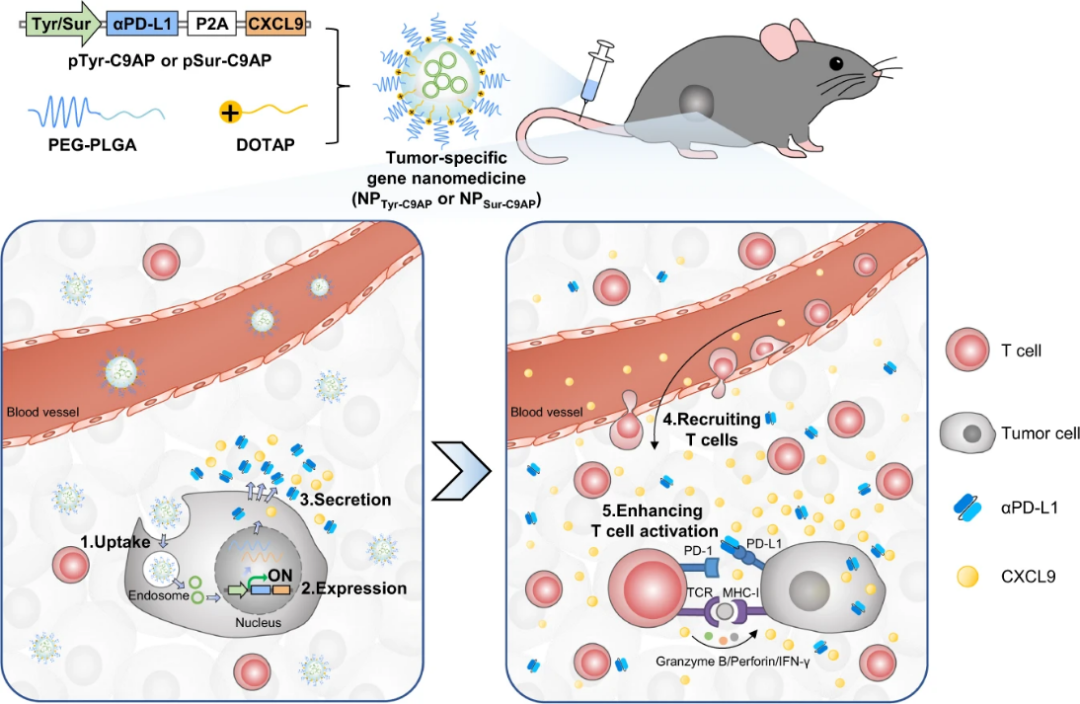
研究团队构建了肿瘤特异性启动子—酪氨酸酶启动子(Tyr)或生存素启动子(Sur)驱动的趋化因子9(CXCL9)与PD-L1单链片段抗体(αPD-L1)的共表达质粒。然后,将此肿瘤特异性基因表达质粒包载在阳离子脂质辅助的聚合物纳米颗粒CLAN中,制备成了肿瘤特异性的基因纳米药物。此基因药物经系统给药后,可以特异性地驱动黑色素瘤细胞或多种肿瘤细胞同时分泌大量的CXCL9与αPD-L1,一方面能够在肿瘤组织与外周组织之间形成显著的CXCL9浓度梯度,促进T细胞在肿瘤中的募集与浸润;另一方面,肿瘤中高浓度的αPD-L1可以有效增强浸润T细胞的活化与杀伤作用。在多种肿瘤模型的体内治疗实验中,均显示出强大的肿瘤免疫治疗效果。另外,与系统注射靶向PD-L1的抗体相比,此纳米药物在疗效和安全性方面均具有一定的优势。这种利用纳米药物将肿瘤细胞设计成T细胞趋化因子和αPD-L1抑制剂生产者的策略,巧妙地解决了αPD-L1治疗中响应率低的问题。
该成果以“Engineering tumor-specific gene nanomedicine to recruit and activate T cells for enhanced immunotherapy”为题发表在国际权威学术期刊Nature Communications, 2023, 14, 1993。
全文链接:https://www.nature.com/articles/s41467-023-37656-w。
