团队在利用锰离子配位纳米载体实现抗原和佐剂的胞质协同递送方面取得研究进展
癌症疫苗由于能够诱导肿瘤特异性和持久性的免疫反应,近年来受到了极大的关注。但肿瘤疫苗在临床上的表现并不令人满意。抗原提呈细胞(APCs)加工呈递抗原能力不足以及抗原和佐剂时空协同效率不高被认为是肿瘤疫苗面临的两大挑战。纳米疫苗在实现抗原和佐剂的时空协同递送方面显示出巨大的优势。在细胞水平上,已经开发了实现抗原胞质递送和抗原佐剂共递送的策略。但是,在亚细胞水平实现抗原和佐剂的时空协同递送仍面临挑战。
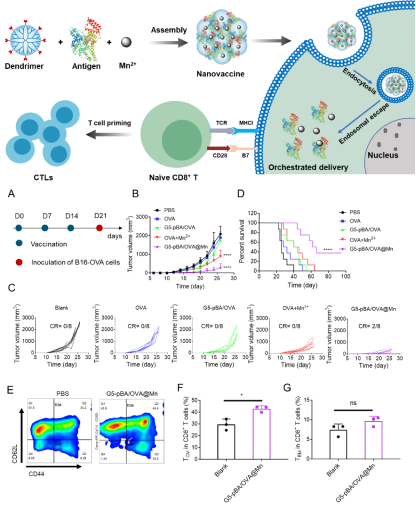
因此,研究团队开发了一种基于锰离子(Mn2+)配位作用以实现抗原和佐剂胞质协同递送的纳米疫苗(G5-pBA/OVA@Mn)。该疫苗体系将Mn2+的生物学功能和结构功能相结合,其不仅能够作为cGAS-STING信号通路的激动剂发挥佐剂功能,而且通过与载体和蛋白抗原发挥配位作用增加抗原的包载,辅助纳米体系的形成。纳米疫苗经内吞途径进入细胞内涵体后,在内涵体酸性条件刺激下,Mn2+配位作用减弱,增强了载体破坏内涵体膜的能力,从而实现抗原和佐剂的内涵体逃逸和胞质协同释放。在体内小鼠模型中,接种G5-pBA/OVA@Mn纳米疫苗诱导产生了强大抗原特异性免疫反应,具有作为预防性疫苗、治疗性疫苗以及联合免疫检查点抑制剂(如α-PD-1)治疗的巨大潜力,为实现抗原和佐剂的时空协同递送提供了一种新策略。
论文信息:该成果以“Orchestrated Cytosolic Delivery of Antigen and Adjuvant by Manganese Ion-Coordinated Nanovaccine for Enhanced Cancer Immunotherapy.” 为题发表在国际著名学术期刊Nano Lett. 2023上,全文链接:https://pubs.acs.org/doi/10.1021/acs.nanolett.2c04970
