近日,华南理工大学生物医学科学与工程学院、生命科学研究院、医学院王均教授和杜金志特聘研究员受邀在美国化学会创办的化学类国际顶级期刊Accounts of Chemical Research(影响因子20.955)发表题为《Tumor-Acidity-Cleavable Maleic Acid Amide (TACMAA): A Powerful Tool for Designing Smart Nanoparticles To Overcome Delivery Barriers in Cancer Nanomedicine》的综述论文(DOI: 10.1021/acs.accounts.8b00195),系统回顾了研究团队从提出肿瘤酸度敏感纳米药物设计理念,到构建载体材料克服体内药物递送屏障,提高肿瘤治疗效果的研究进展。华南理工大学是论文唯一署名单位,王均教授和杜金志特聘研究员为通讯作者。
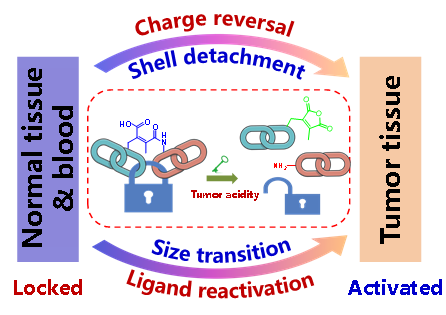
纳米药物递送系统是王均教授研究团队重点研究方向之一。纳米颗粒作为药物递送系统,可增强药物治疗效果,提高候选药物成药性。然而,抗肿瘤纳米药物经静脉注射后需经历血液环境、肿瘤组织微环境、细胞内微环境等性质和特征不同的药物递送屏障,具体包括血液循环、血管渗出、肿瘤组织富集和渗透、肿瘤细胞内吞及胞内药物释放等多个方面。上述生理屏障严重降低纳米药物进入肿瘤及肿瘤细胞的效率,降低了抗肿瘤效果。针对上述问题,王均教授领导的科研团队经过近十年的不懈努力,提出了肿瘤酸度敏感纳米载体设计理念,构建了一系列基于2,3-二甲基马来酸酰胺及其衍生物的肿瘤酸度响应纳米药物载体,其在正常生理条件下具有“生物惰性”,可延长纳米颗粒血液循环,增加肿瘤富集,而在肿瘤部位则发生特异性性能变化,如电荷反转、尺寸转变、PEG脱壳、配体重激活等,有效克服药物递送的生理屏障,提高药物递送效率和肿瘤治疗效果。研究成果发表了系列高水平论文,如Angew. Chem. Int. Ed. 2010, 49, 3621;J. Am. Chem. Soc. 2011, 133, 17560;ACS Nano 2012, 6, 771;Adv. Mater. 2012, 24, 5476;Adv. Mater. 2014, 26, 931;J. Am. Chem. Soc. 2015, 137, 15217;Proc. Natl. Acad. Sci. U. S. A. 2016, 113, 4164;Angew. Chem. Int. Ed. 2016, 128, 1010等。所提出的研究策略受到国内外同行的广泛关注和采纳,上述系列论文总引用近2000次,其中有5篇论文入围ESI高被引榜单。
论文全文链接:https://pubs.acs.org/doi/10.1021/acs.accounts.8b00195
