文章简介
NLRP3炎性小体与多种炎性疾病有关,其过度激活会引发相关疾病的发生和发展,因此其激活需要严格控制。过量产生的活性氧 (ROS) 被认为是NLRP3炎性体激活的关键因素。因此,具有ROS清除能力的纳米酶是NLRP3激活的潜在抑制剂,也是相关炎症疾病的有希望的治疗药物。然而,通过靶向NLRP3炎症小体,直接抑制NLRP3炎症小体活化从而防治炎性疾病的纳米酶却鲜有报道。

近期,华南理工大学张云娇教授团队报道了二维羟基氧化钴纳米片(2D Co NSs),其具有包括过氧化物酶(POD)、过氧化氢酶(CAT)和超氧化物歧化酶(SOD)在内的多种类酶催化活性和羟基自由基(•OH)清除能力,可以对应清除多种生物相关的ROS,如H2O2,•O2⁻和•OH。作者进一步通过密度泛函理论(DFT)计算阐明了Co NSs多种ROS清除活性的潜在机制以及它们之间的相对活性强弱:在生理条件下这些消除ROS的催化反应是自发的,且CAT在其中占主导地位。除了作为广谱的ROS清除剂,Co NSs还是NLRP3炎症小体和焦亡的抑制剂,可以通过阻止NLRP3炎症小体组装过程关键蛋白的寡聚化和焦亡相关蛋白的剪切,直接抑制NLRP3炎症小体的活化及其激活后介导的焦亡。体内的实验表明,Co NSs处理可以缓解LPS诱导的系统性炎症和DSS诱导的肠炎的症状。这项工作以“2D Cobalt Oxyhydroxide Nanozymes Inhibit Inflammation by Targeting the NLRP3 Inflammasome”为题发表在Advanced Functional Materials上。文章的第一作者是华南理工大学博士研究生陈梓莹,中山大学陈品博士为共同第一作者,华南理工大学张云娇教授为通讯作者。
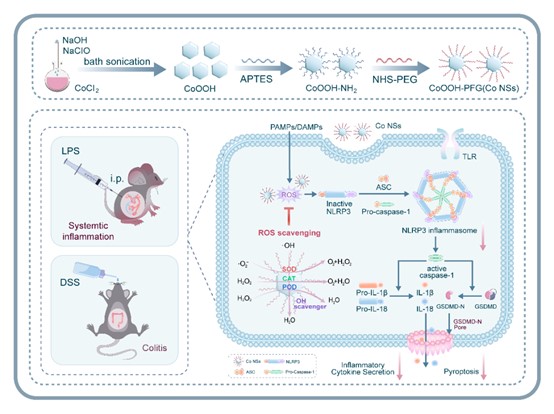
图1. Co NSs作为NLRP3抑制剂治疗系统性炎症和肠炎的机制示意图
文章要点
1.类酶催化活性和ROS清除能力评估
研究团队采用共沉淀法联合超声剥离合成了二维Co NSs,并对其进行了PEG化修饰使其具有更好的生物相容性。体外实验验证了Co NSs具有类过氧化物酶(POD)、过氧化氢酶(CAT)和超氧化物歧化酶(SOD)三种类酶催化活性,以及羟基自由基(•OH)的清除能力,使其能够针对性地清除过氧化氢(H2O2)、超氧阴离子(•O2⁻)和羟基自由基(•OH)这三种具有代表性的且生物相关的ROS。
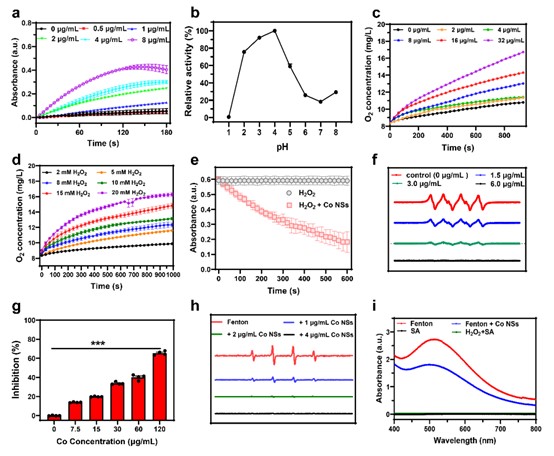
图2. Co NSs具有多种清除ROS的类酶催化活性
2.多种清除ROS的类酶催化活性潜在机制探究
研究团队还通过DFT计算进一步揭示了在生理条件下(pH 7.4)Co NSs能够清除多种ROS的潜在机制:三种类酶催化反应以及•OH的清除反应均可自发进行,且三种类酶催化反应的难易程度为CAT>SOD>POD,说明CAT催化活性最高,可能占主导地位。因此,说明了在生理条件下,Co NSs仍然具有多种类酶催化活性和强大的抗氧化ROS清除作用,具有有效保护细胞免受各种ROS损伤的潜力。
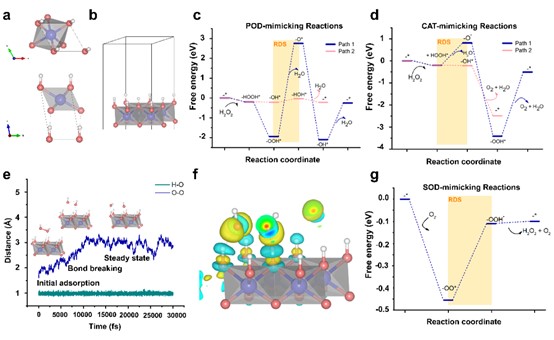
图3. Co NSs多种类酶活性的密度泛函理论研究
3.抑制NLRP3炎症小体活化和细胞焦亡及其潜在机制探究
鉴于在上述体外实验中Co NSs展现出令人钦佩的多种类酶催化活性和强大的ROS清除能力,研究团队通过酶联免疫吸附测定、免疫印迹法以及荧光显微镜检术、免疫荧光等方法发现Co NSs在胞内仍然可以发挥清除ROS的能力,显著抑制NLRP3炎症小体的活化及其介导的焦亡,保护细胞免受氧化损伤。研究团队对其抑制NLRP3炎症小体活化的潜在分子机制进行了更加深入的探究,发现除了减少ROS的产生以外,Co NSs还可以通过阻止NLRP3寡聚化和随后的ASC寡聚化,从而抑制NLRP3炎症小体的组装和活化,而不影响启动(priming)阶段和钙、钾离子的外流等上游信号通路。
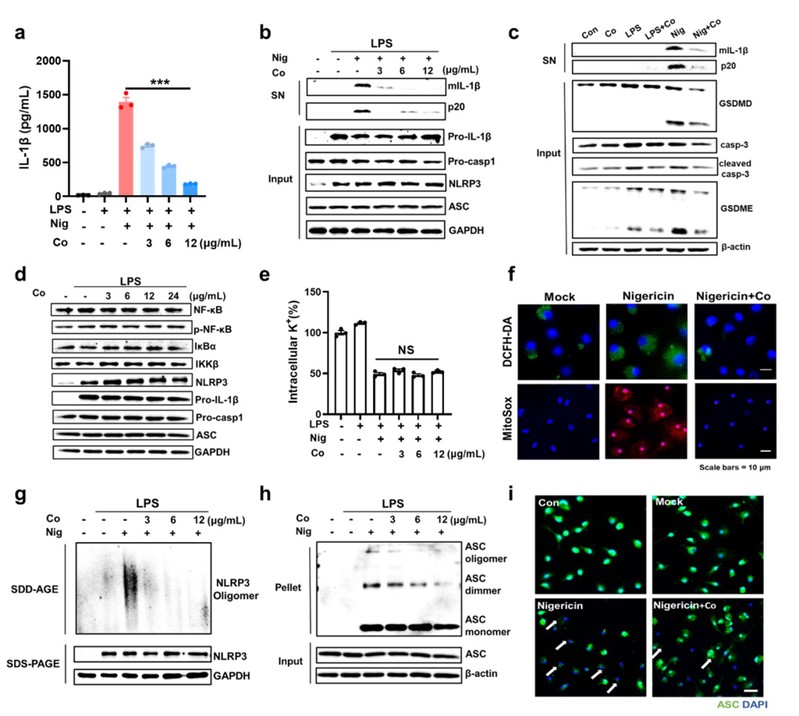
图4. Co NSs在胞内抑制NLRP3炎性小体活化和减少细胞焦亡
4.缓解系统性炎症和肠炎的治疗效果探究
由于Co NSs在体外表现出显著的抑制NLRP3炎症小体激活的能力,研究团队进一步在两个已报道与NLRP3炎症小体活化的动物模型——系统性炎症模型以及肠炎模型中证明了Co NSs在体内仍可有效地抑制NLRP3炎症小体的激活,缓解这两种炎性疾病的症状。
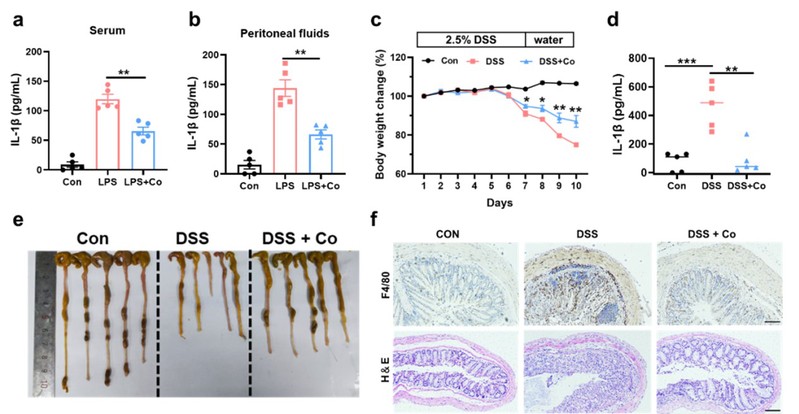
图5. Co NSs在体内缓解系统性炎症和急性结肠炎
结论与展望
在本研究中,研究团队展示了具有包括POD、CAT和SOD在内的多种类酶催化活性的二维Co NSs是一种广谱的活性氧清除剂。通过DFT计算进一步说明了Co NSs在生理条件下可以自发地清除H2O2、•O2⁻和•OH,CAT反应由于其具有最低的吉布斯自由能,因此它可能在其中起主导作用。除了清除ROS,Co NS还具有抑制寡聚化和下调焦亡相关蛋白的能力,因此Co NSs是潜在的NLRP3炎症小体抑制剂,同时也是焦亡的抑制剂。体内实验也证明Co NSs可以通过靶向NLRP3炎症小体从而在系统性炎症和肠炎中表现出抗炎作用。这项工作首次报道了利用钴基纳米酶靶向NLRP3炎症小体从而缓解炎症的成功策略,并为其潜在机制提供了有价值的见解,证明了纳米酶在预防和治疗NLRP3相关炎症性疾病方面的潜在治疗作用。
文章链接:DOI: 10.1002/adfm.202214693
