学院纳米生理学与医学团队在ACS Nano期刊上发表最新研究成果
日期:2026-02-26
近期,学院纳米生理学与医学团队在ACS Nano期刊上发表“Priming the Liver Endocytic Pathway to Accelerate Hepatobiliary Clearance of Nanoparticles”为题的研究成果。华南理工大学为论文的第一署名单位,华南理工大学蒋兴垭教授和华南理工大学附属第二医院杜步婕研究员为该论文的共同通讯作者,学院2022级生物学专业博士研究生任云锋、2022级生物医学工程专业硕士毕业生梅放为本文的共同第一作者。论文得到了国家重点研发计划、国家自然科学基金等项目的资助。
纳米药物在疾病诊疗领域展现出巨大潜力,然而其临床转化受困于一个重要瓶颈:绝大部分注入体内的纳米颗粒会被肝脏拦截并长期滞留,不仅无法抵达病灶,还可能带来潜在的毒性风险。传统的解决思路主要聚焦于对纳米颗粒进行表面修饰,试图减少肝脏的初始摄取。然而,即使采用了表面聚乙二醇修饰等逃逸免疫识别的策略,大多数纳米颗粒最终仍难逃被肝脏捕获的命运。如何加速已滞留肝脏的纳米颗粒清除,成为亟待解决的问题。
基于此,华南理工大学纳米生理学与医学团队报告了一种通过短暂调控肝脏内吞途径来加速多种纳米颗粒在肝胆中清除的全新策略。研究人员发现,利用临床药物氯丙嗪对小鼠进行预处理,暂时性抑制肝脏细胞摄取大尺寸颗粒的主要途径—网格蛋白介导的内吞作用,可显著改变纳米颗粒在细胞内的运输路径,使其从溶酶体转运途径转向高尔基体分泌途径,从而加速颗粒的在肝胆中清除。
该研究的灵感源于对纳米颗粒尺寸效应的系统观察。研究发现,小尺寸金纳米颗粒(2 nm)在肝脏中具有更快的固有清除速率,其胞吐效率约为大尺寸颗粒(55 nm)的3倍。进一步的机制研究表明,这种差异源于尺寸依赖的内吞途径:大尺寸颗粒主要经由网格蛋白介导的内吞作用进入肝细胞,而小尺寸颗粒则更多依赖非网格蛋白介导的摄取途径。这提示着,调控纳米颗粒的入胞途径可能影响其后续的胞内命运和清除速率。通过使用网格蛋白介导内吞作用抑制剂氯丙嗪,研究团队在细胞层面证实,抑制该途径可显著提升肝细胞对大尺寸金纳米颗粒的胞吐效率。荧光共定位分析显示,氯丙嗪处理使被内吞的纳米颗粒从溶酶体途径转向高尔基体分泌途径,且这一促排效应可被高尔基体分泌途径特异性抑制剂所阻断,证实了高尔基体在加速胞吐中的关键作用。
在动物水平上,单次氯丙嗪预处理即可显著加速多种纳米颗粒的在肝胆中清除:大尺寸金纳米颗粒的肝脏清除效率提升约219%,粪便排泄量增加85%;二氧化钛纳米颗粒的肝脏蓄积降低63%,粪便排泄增加141%。通过活体近红外荧光成像,研究者还观察到氯丙嗪处理使Cy7.5标记的聚合物纳米颗粒在给药后2小时即被快速排泄至肠道,而对照组颗粒直至12小时仍主要滞留于肝脏。尤为重要的是,在4T1荷瘤小鼠模型中,氯丙嗪预处理在显著促进纳米药物在肝胆中清除、降低肝脏非特异性蓄积的同时,并未影响纳米药物的血液循环时间及其对肿瘤的靶向递送效率。
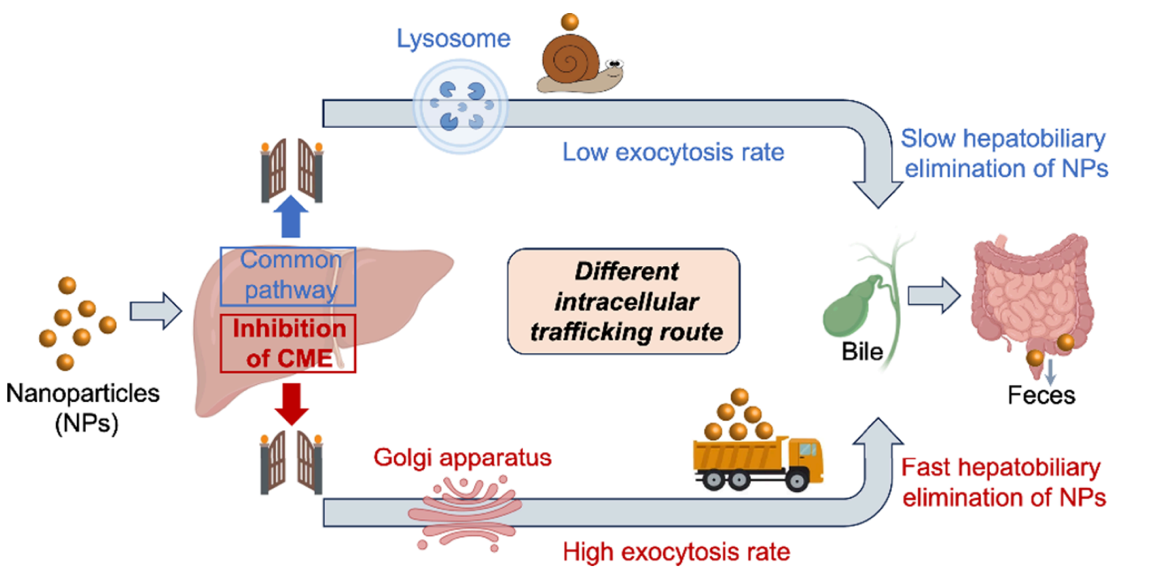
图:通过调控肝脏内吞途径加速纳米颗粒在肝胆中清除的示意图
综上所述,本研究提出并验证了一种不依赖纳米颗粒自身材料设计、通过短暂调控细胞内吞功能来加速纳米颗粒体内清除的全新策略。该策略具有广泛的适用性,其促排效应覆盖无机纳米材料(包括金纳米颗粒、二氧化钛纳米颗粒)与有机纳米材料(如聚合物纳米颗粒)等多种不同类型。在加速肝脏清除的同时,该策略不损伤纳米药物的肿瘤靶向能力。另外,由于所使用的氯丙嗪是已获批使用的临床药物,且研究中使用的剂量远低于临床最大安全剂量,因此展现出良好的临床转化潜力。这一发现不仅深化了对细胞内吞途径与胞吐途径之间内在联系的理解,也为纳米药物非特异性肝脏蓄积这一临床转化挑战提供了新策略。(通讯员/蒋兴垭教授课题组)
全文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c20532<p>
