谢建凌教授团队在肿瘤学权威期刊 Oncogene 发表研究成果:揭示丝氨酸蛋白酶驱动结直肠癌发生发展的分子机制,为靶向治疗提供新策略
近日,华南理工大学生物科学与工程学院谢建凌教授团队与上海中医药大学沈凯凯教授团队合作,在肿瘤学权威期刊Oncogene 上在线发表题为 “PRSS22 inhibits HMOX1-mediated ferroptosis and induces osteopontin cleavage to promote M2 macrophage polarization and colitis-associated carcinogenesis” 的研究论文。该研究首次系统阐明了丝氨酸蛋白酶PRSS22 在炎症相关性结直肠癌发生发展中的关键驱动作用及分子机制,为结直肠癌的诊断和靶向治疗提供了全新的理论依据与潜在靶点。华南理工大学生物科学与工程学院为该论文的第一通讯单位,谢建凌教授与沈凯凯教授为本论文的通讯作者,谢建凌教授课题组的硕士研究生邝子健为第一作者,博士研究生梁文垦为第三作者。

论文链接:https://www.nature.com/articles/s41388-026-03729-5#Sec24
结直肠癌是全球发病率和死亡率均位居前列的恶性肿瘤,每年导致近百万患者死亡。炎症- 癌症转化(ICT)是结直肠癌发生的核心病理过程,然而当前针对该过程的靶向治疗效果有限,亟需挖掘新的关键调控因子及作用机制。丝氨酸蛋白酶家族成员在肿瘤的发生发展中扮演重要角色,其表达异常会导致癌细胞蛋白质组重塑以适应恶性增殖需求。PRSS22 作为该蛋白酶家族的成员之一,已被发现与多种肿瘤相关,但在结直肠癌中的具体功能及分子机制此前尚未明确。
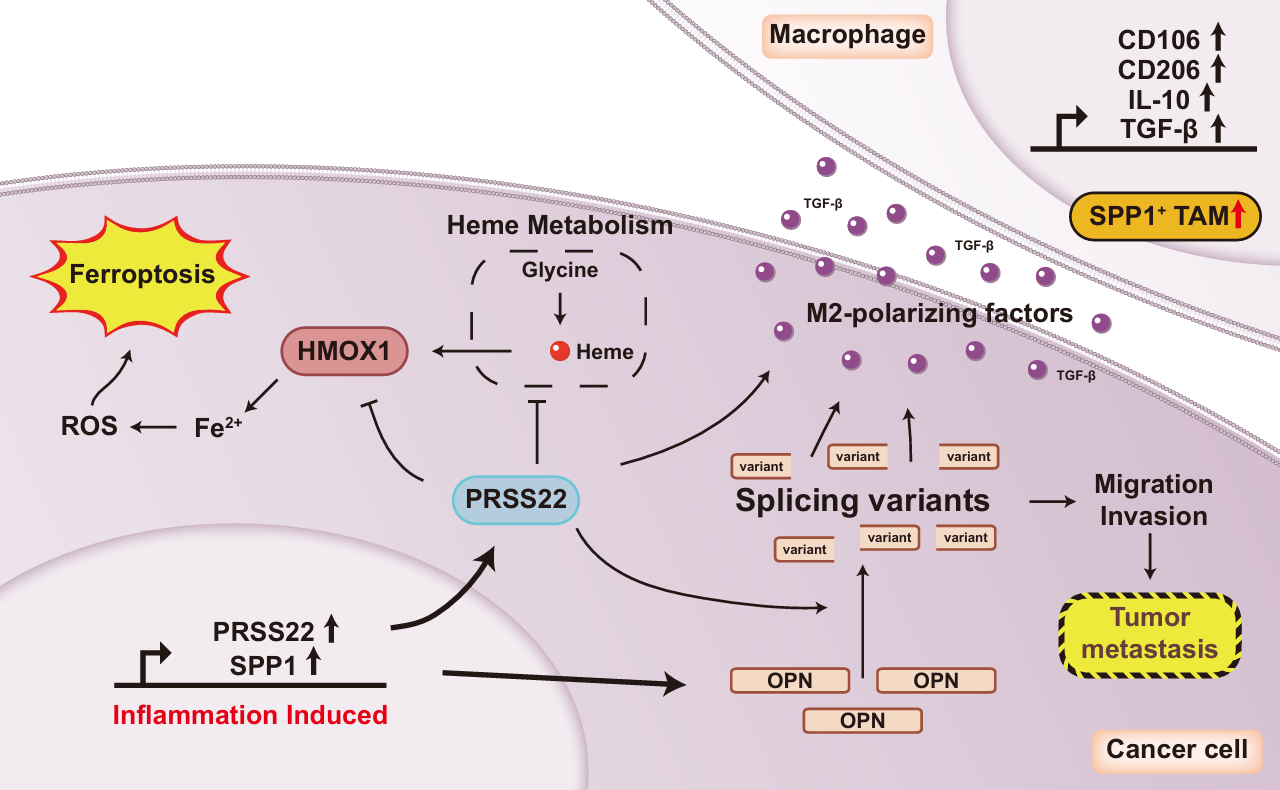
图1:PRSS22 通过抑制HMOX1 介导的铁死亡、切割骨桥蛋白(OPN)、促进M2 型巨噬细胞极化三条通路驱动结直肠炎癌转化。
研究团队通过整合分析结直肠炎/癌的多组学数据,发现PRSS22 在炎症性肠病患者和结直肠癌患者组织中显著高表达,且其表达水平与肿瘤病理进展、转移潜能及患者不良预后密切相关。ROC 曲线分析显示,PRSS22 对结直肠癌的诊断具有极高的准确性,有望成为结直肠癌诊断的新型生物标志物。
通过功能实验证实,研究团队发现沉默PRSS22 可显著抑制结直肠癌细胞的增殖及迁移能力,并诱导癌细胞死亡;而在裸鼠异种移植模型中,敲低PRSS22 能有效减少肿瘤体积和重量,充分验证了PRSS22 的促癌功能。机制研究进一步揭示,PRSS22 通过三条相互关联的通路调控结直肠癌进展:一是抑制HMOX1基因表达,阻断其介导的铁死亡,减少活性氧积累和铁离子过载,维持癌细胞存活;二是作为蛋白酶切割骨桥蛋白(OPN),生成具有促迁移活性的片段,增强癌细胞的侵袭转移能力;三是通过上调肿瘤细胞来源的转化生长因子β(TGFβ),促进巨噬细胞向M2 型免疫抑制表型极化,重塑肿瘤微环境,助力癌细胞免疫逃逸。
该研究首次揭示了PRSS22 在结直肠癌炎症- 癌症转化中的核心调控作用,建立了 “PRSS22-HMOX1-铁死亡”;“PRSS22-OPN-细胞迁移”与“PRSS22-TGFβ-M2巨噬细胞极化” 三条关键通路的分子网络,为理解结直肠癌的发病机制提供了新的视角。由于PRSS22 在正常结直肠组织中表达低,靶向抑制PRSS22 有望在高效杀伤癌细胞的同时,减少对正常组织的损伤,具有良好的临床转化潜力。
本研究工作得到了华南理工大学 “双一流” 建设、广东省引进创新创业团队、澳大利亚国家健康与医学研究委员会、弗林德斯基金会及上海市东方英才计划等多项科研基金的支持。