陈晓东院士等人Nature:受蜘蛛丝启发的超收缩薄膜
在电子器件领域,实现柔软的生物组织与硬质电子设备的标准化接口一直是一项挑战。生物组织不仅柔软,其形状和尺寸也多种多样。如果能开发出一种生物相容性薄膜,类似于工业包装中常见的“热收缩膜”,或许能够实现对各种形状和尺寸的生物-电子接口的理想匹配。然而,寻找能制造这种生物相容性收缩薄膜的材料并非易事。常见的热收缩膜往往比生物组织更硬,而且需要较高温度才能收缩,无法在人体温度下使用。在体温和水刺激下收缩的材料与生理环境更相容,但又往往收缩太过缓慢或稳定性不佳。水凝胶足够柔软,可以最大限度地减少与生物组织的机械不匹配,但它们的高含水量使它们与普通的微电子制造工艺不相容。
蜘蛛丝被认为是最坚韧的天然材料之一,兼具机械强度和延展性的优点。更独特的是,在高湿度环境下,蜘蛛牵引丝(dragline)的长度会急剧收缩约60%,该过程通常被称为超收缩现象,其机理归因于牵引丝独特的分层结构,以及高相对湿度触发微观结构的转变。
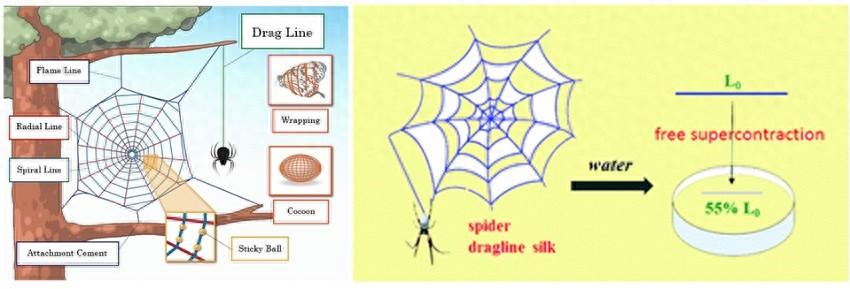
蜘蛛牵引丝及其超收缩现象。图片来源:Molecules [1]& J. Mater. Chem. B [2]
受到蜘蛛牵引丝遇水超收缩现象的启发,近日南洋理工大学陈晓东院士和高华健院士、中国科学院深圳先进技术研究院刘志远研究员、南京医科大学胡本慧教授等研究者合作,开发出一种新型水响应超收缩聚合物薄膜,解决了生物组织与电子器件界面的无缝连接问题,为实现生物和电子设备之间的标准化集成提供了新的可能性。
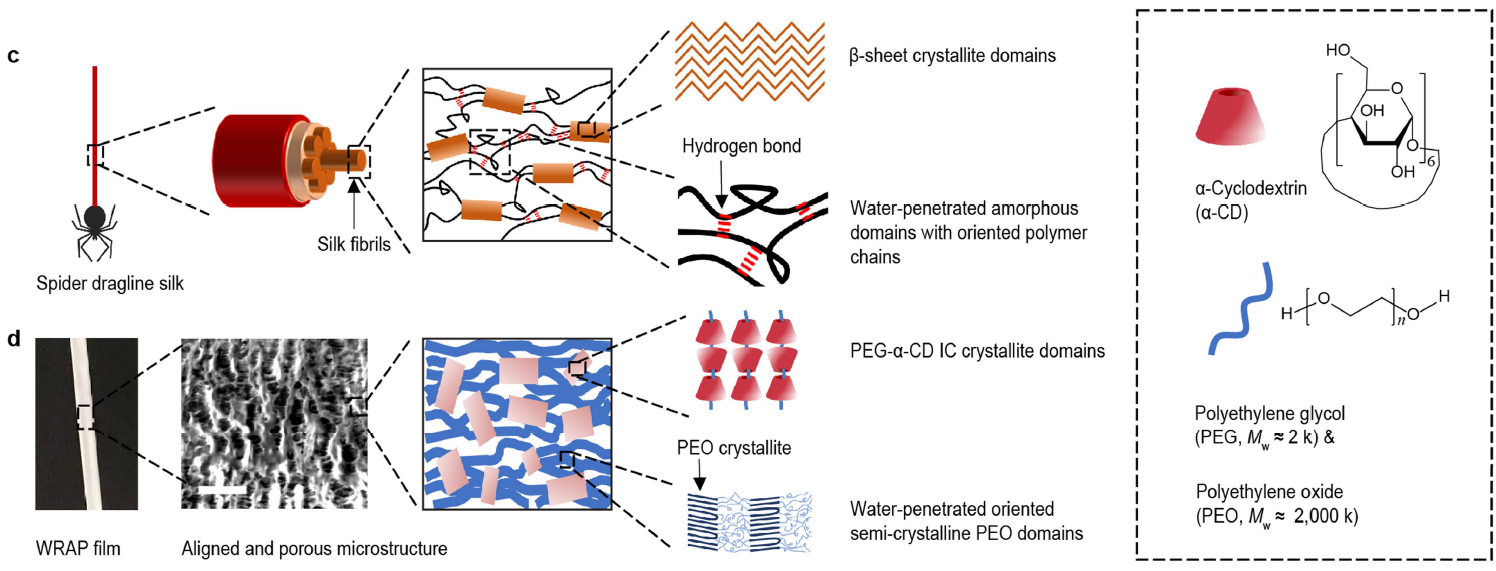
受蜘蛛牵引丝启发的水响应超收缩聚合物薄膜。图片来源:Nature
研究者将半晶态聚氧化乙烯(PEO)颗粒溶解在水中,与聚乙二醇-α-环糊精凝胶混合并进行交联,经过溶剂铸膜、干燥和反复冷拔就得到了水响应形状可塑聚合物薄膜(WRAP)。自然环境下,薄膜的可拉伸范围从218%到700%,将其浸泡在水中后,薄膜会迅速收缩,变成柔软且可拉伸的水凝胶薄膜,对应的收缩比从35%到65%,其杨氏模量也下降了三个数量级以上。而且,当相对湿度低于80%时,薄膜并不会发生收缩,这表明它们在普通环境湿度下具有稳定性。
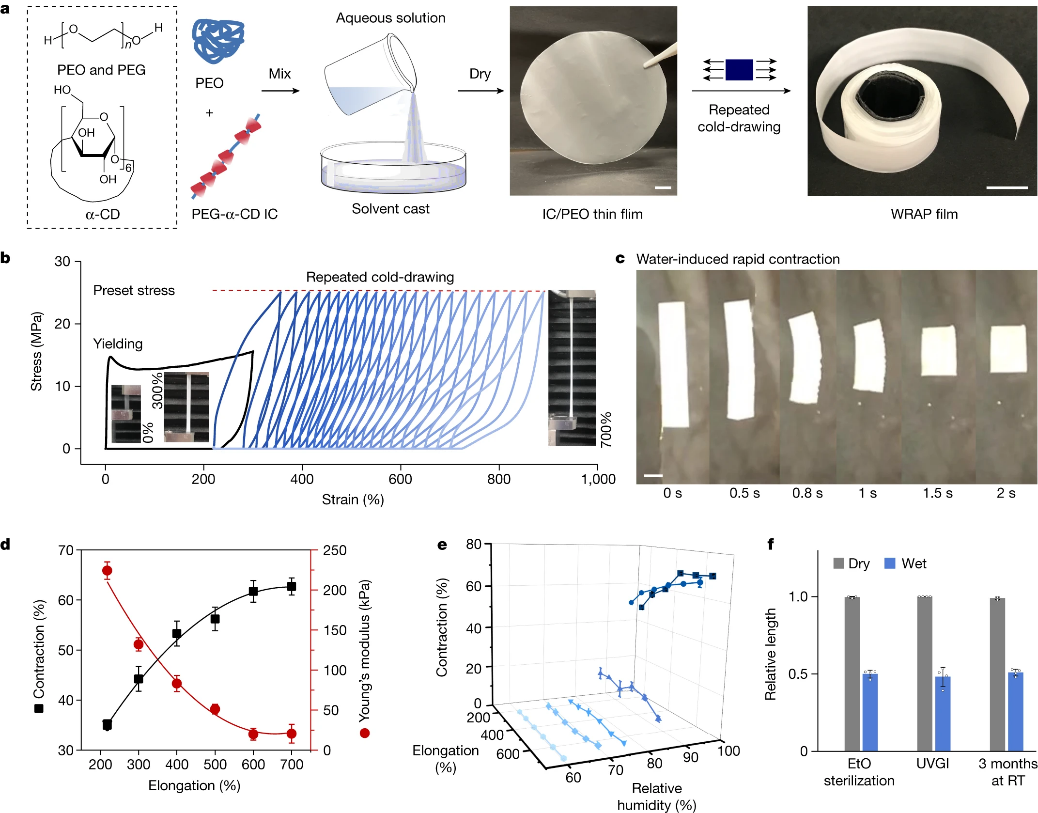
水响应形状可塑聚合物薄膜。图片来源:Nature

WRAP薄膜遇水超收缩。图片来源:Nature
薄膜的超收缩性能与微观结构密切相关。测试显示,薄膜在冷拔时产生多孔微结构,并使PEO微晶和链取向,暂时被PEO再结晶域固定。将薄膜放入水中后,PEO结晶域被水破坏和溶解,引起了薄膜的超收缩。而聚乙二醇-α-环糊精凝胶部分则保证了多孔微结构的形成,以及遇水收缩后薄膜的稳定性。
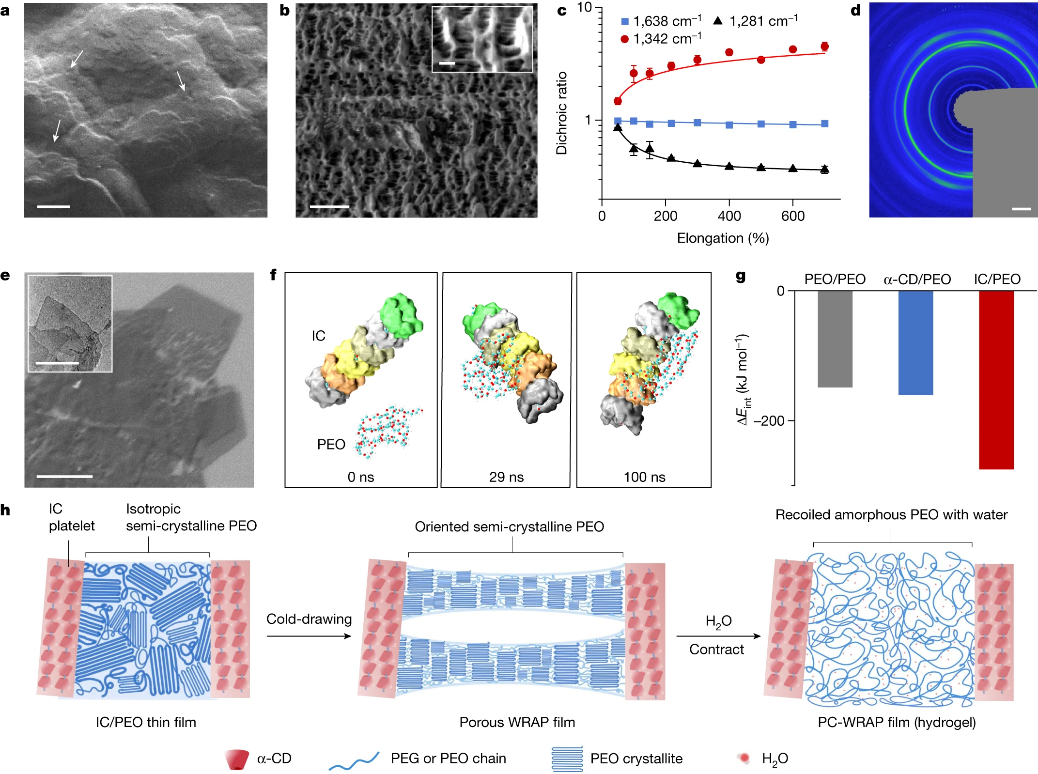
WRAP薄膜的微观结构和超收缩机理。图片来源:Nature
随后,研究者通过真空蒸镀和旋涂法在WRAP薄膜上分别沉积了金(Au)和嵌段共聚物SEBS,得到的WRAP-Au薄膜同样表现出良好的柔性。在湿润条件下,WRAP-Au薄膜发生收缩,其阻抗和相位角值在20%和40%应变时几乎保持不变。体外测试结果显示,经过循环拉伸和在生理盐水中浸泡2周后,WRAP-Au电极依旧具有稳定的性能。
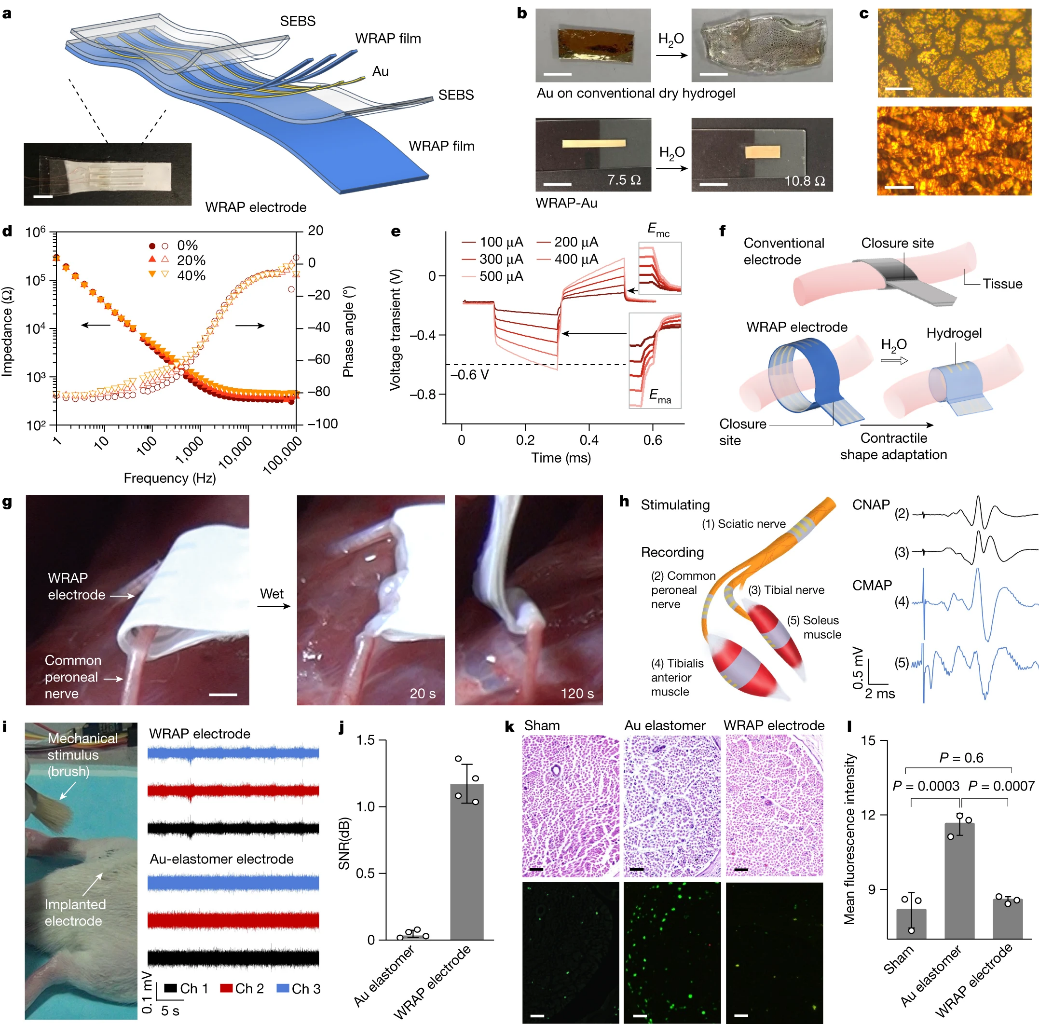
WRAP-Au电极制备及应用。图片来源:Nature
利用WRAP-Au电极的水响应超收缩以及形状自适应,可以轻松植入生物组织,并用于电生理信号记录或神经刺激。在植入组织时,可以事先在组织较远处放置电极,因此减小了组织损伤的风险。研究者在大鼠坐骨神经和较小的胫骨神经等处预置了WRAP-Au电极。尽管神经大小不同,但在浸湿后,电极都会收缩成适应形状的薄膜,包裹在神经周围,并应用于神经脉冲刺激以及记录神经动作电位和神经电图(ENG)。
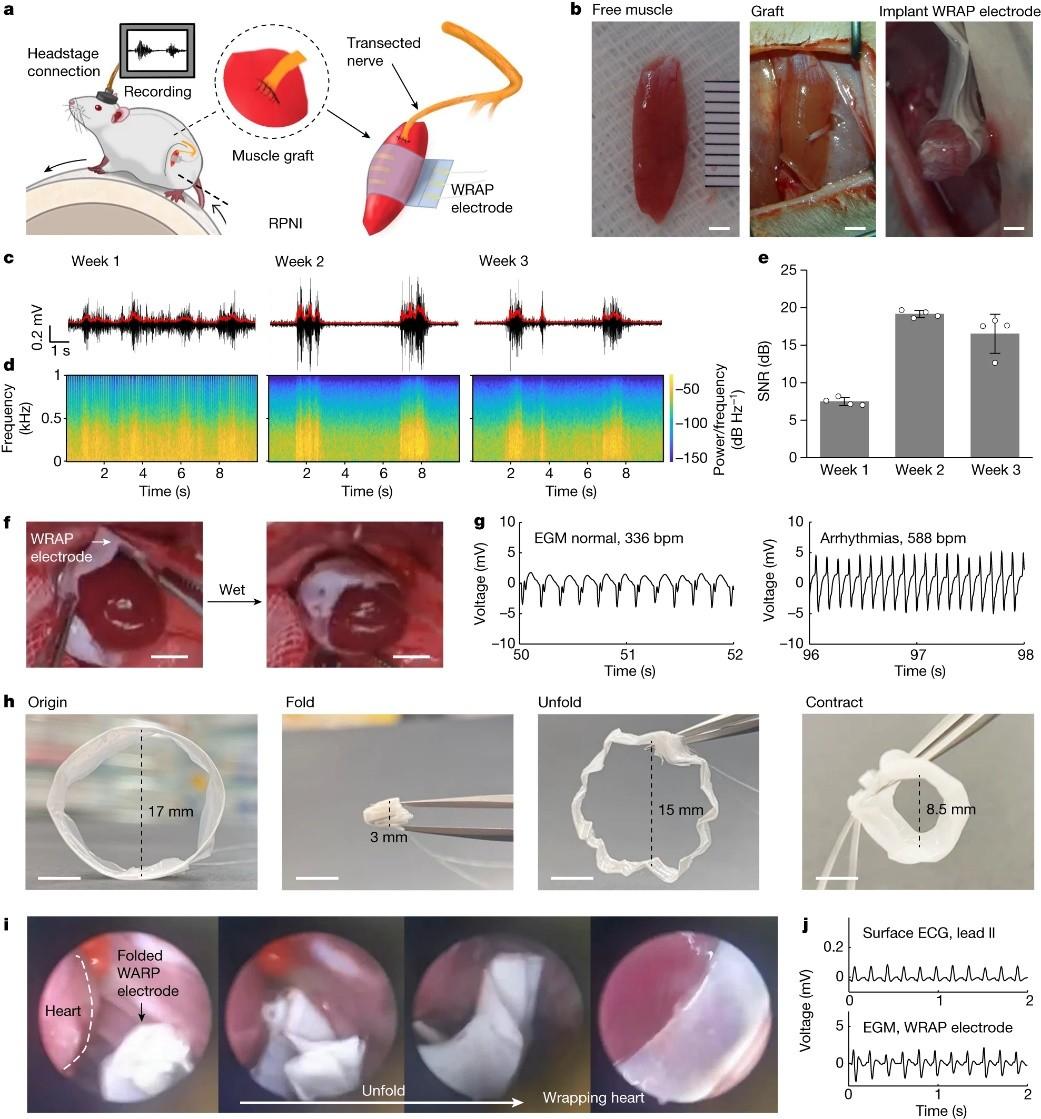
WRAP-Au电极微创植入及应用。图片来源:Nature
研究者进一步将WRAP-Au电极包裹在大鼠的肌肉上,记录了肌电图信号(EMG)。由于薄膜收缩后具有自适应性,可以紧贴在大小和形状都不规则的肌肉表面,使得振幅、信噪比等均表现良好。类似地,WRAP-Au电极还可以包裹在大鼠的心脏周围,并记录大鼠心脏的心电图。
“报道的材料与水接触时的收缩反应对生物医学领域非常有吸引力,尤其是植入手术。这是我读过的关于柔性材料的最令人印象深刻的论文之一”,约翰霍普金斯大学医学院Nitish Thakor评论道。Nature 杂志的首席编辑Karl Ziemelis也认为,“精密的生物组织可以有效地和电子元件一起被‘收缩包裹’,促进了各种传感和神经刺激应用”。研究者则表示,下一个挑战或许是进一步改进交联PEO,得到更稳定的薄膜。[3]
Water-responsive supercontractile polymer films for bioelectronic interfaces
Junqi Yi, Guijin Zou, Jianping Huang, Xueyang Ren, Qiong Tian, Qianhengyuan Yu, Ping Wang, Yuehui Yuan, Wenjie Tang, Changxian Wang, Linlin Liang, Zhengshuai Cao, Yuanheng Li, Mei Yu, Ying Jiang, Feilong Zhang, Xue Yang, Wenlong Li, Xiaoshi Wang, Yifei Luo, Xian Jun Loh, Guanglin Li, Benhui Hu, Zhiyuan Liu, Huajian Gao & Xiaodong Chen
Nature, 2023, 624, 295-302. DOI: 10.1038/s41586-023-06732-y
参考文献:
[1] T. Asakura, Structure and Dynamics of Spider Silk Studied with Solid-State Nuclear Magnetic Resonance and Molecular Dynamics Simulation. Molecules 2020, 25, 2634. DOI: 10.3390/molecules25112634
[2] Q. Dong, et al., Effect of stress on the molecular structure and mechanical properties of supercontracted spider dragline silks. J. Mater. Chem. B 2020, 8, 168-176. DOI: 10.1039/C9TB02032B
[3] Nature Research Briefing: Polymer films inspired by spider silk connect biological tissues and electronic devices. Nature, 2023, DOI: 10.1038/d41586-023-03653-8
https://www.nature.com/articles/d41586-023-03653-8
