《Nat. Mater.》:凝胶-凝胶相分离
动态生命系统中的液-液相分离会产生无膜有序结构,如核小体、应力颗粒和Cajal体。液-液相分离是生命科学领域的一个新挑战,与包括白内障和神经退行性疾病在内的多种疾病的发生有关。由于大分子的存在,相分离在生命系统中被广泛观察到。由于摩尔质量大,与小分子相比,大分子不利于混合,因为混合熵取决于分子的数量。
使用临界溶液温度(LCST)较低的单体进行聚合可导致相分离。聚(N-异丙基丙烯酰胺)在略高于 LCST 的恒温条件下进行聚合时,在水中会出现相分离现象。起初,反应混合物是透明的,因为单体与水混溶。随着反应的进行和摩尔质量超过临界值,LCST 出现,然后随着摩尔质量的增加而降低。当 LCST 低于反应温度时,就会发生微相分离。引入交联剂可阻止微相分离,形成相分离凝胶。这种相分离凝胶由显示 LCST 的聚合物制备而成。
这项研究,东京大学Naoyuki Sakumichi、Takamasa Sakai等确定了凝胶化诱导的相分离,即渗滤过程。在整个渗流过程中,水-聚乙二醇(PEG)二元体系中发生了凝胶-凝胶相分离(GGPS),这种相分离从未在标准大气压下观察到过。GGPS 是在溶质浓度低于特定值时,通过凝胶化被阻滞的异质结构诱导产生的;凝胶化是一个耗散过程,随后的消胀过程形成了亚毫米尺度的两个共连续凝胶相(图 1)。含有 GGPS 的水凝胶显示出意想不到的疏水性,皮下注射时可诱导类似脂肪组织的生长,而不含 GGPS 的类似水凝胶或传统 PEG 水凝胶则没有这些特征。相关研究工作以“Percolation-induced gel–gel phase separation in a dilute polymer network”为题发表在国际顶级期刊《Nature Materials》上。祝贺!


图1. 产生稀释渗透凝胶和c*凝胶的过程示意图
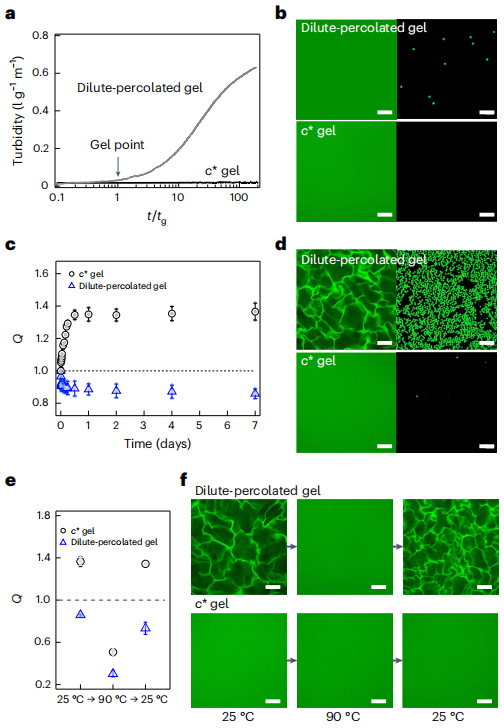
图2. 凝胶化过程中的混浊和热力学上稳定的亚毫米尺度相分离结构
PEG 前体与水的混溶性超过了 c 的研究范围(~300 g l-1)。此外,在重叠浓度 c* ≈ 60 g l-1 以上会形成透明凝胶(图 1 和 2a)。这里,c* 是水合 PEG 前体结构域吞噬整个体系的浓度。这些结果与之前的结果一致,即 PEG-水二元体系的 LCST 高于水的沸点(约 130 °C);因此 PEG 具有亲水性。然而,在 25 °C 时,当 PEG 浓度降低到 c* 以下时,胶凝溶液会变得浑浊(图 1 和 2a)。这种现象与传统的观点相矛盾,即当溶质浓度超过特定值时就会发生相分离。为了解释这种行为,他们研究了分别在 c = 10 和 60 g l-1 条件下形成的两种代表性凝胶(稀释渗透胶体和 c* 凝胶)。稀释的渗透凝胶在凝胶点之后会变得更加浑浊,因为前驱体会渗透并形成聚合物网络(图 1 和 2a)。尽管浑浊,稀释的渗透溶胶在亚毫米范围内没有明显的形态(图 2b)。
将凝胶在溶剂(水)中浸泡一周后,c*凝胶和稀释渗透凝胶会分别发生膨胀和去溶胀(图 2c)。他们观察到稀释渗透凝胶和 c* 凝胶在水中平衡去溶肿/溶胀一周后的中尺度结构。聚合物骨架的四聚乙二醇(tetra-PEG)末端基团部分被 Alexa Fluor 488 修饰,呈阳性染色,以便观察。亚毫米尺度的丝状网络结构仅在稀释渗透凝胶中生长(图 2d,顶部),并通过其三维结构(图 1)凸显出来。凝胶化需要一天时间,没有特定的结构(图 2b,左上角)。
丝状结构具有热稳定性(图 2e、f)。当温度升至 90 °C 时,稀释渗透凝胶收缩,混浊度降低,亚毫米尺度结构消失(图 2e,图 2b,顶部)。
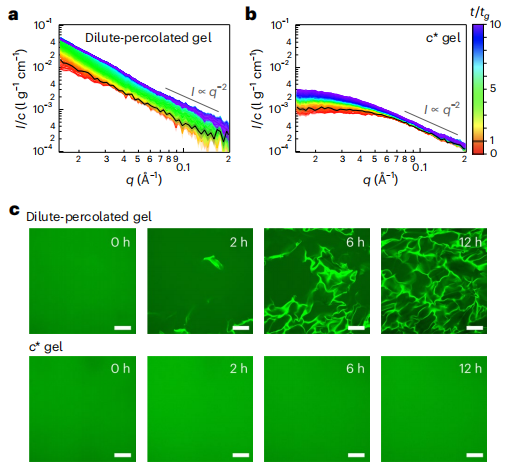
图3. GGPS的形成过程
他们进行了时间分辨小角 X 射线散射(SAXS)实验,以阐明稀释渗透凝胶和 c* 凝胶在凝胶化过程中的结构变化(图 3a、b)。
稀释渗透凝胶的丝状结构是在去溶胀过程中形成的(图 3c,上部)。从模具中取出并浸入水中后,凝胶没有显示出任何结构,但在 2 小时后形成了分散的丝状结构,但该结构可能会随着连续一周的去溶胀而进一步生长。然而,在相同的时间范围内,c*凝胶和 c*稀释凝胶都没有特征性结构。
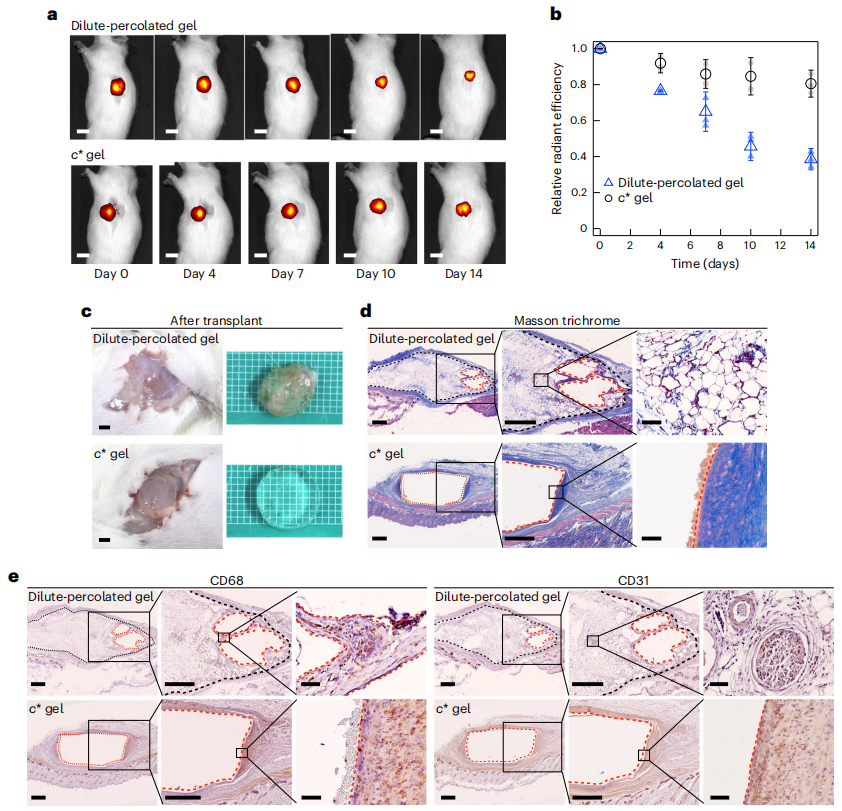
图4. 水凝胶的生物反应
生命系统中的细胞外基质在不透明性和中尺度结构方面类似于稀释的渗透凝胶。为了证明这一点,他们将处于平衡溶胀状态的圆盘状水凝胶植入大鼠皮下,并在 14 天内研究凝胶的生物反应差异(图 4)。他们首先通过对荧光标记的水凝胶进行体内成像来评估降解情况(图 4a)。通过分析相对于第 0 天信号的辐射效率(图 4b),只有稀释渗透凝胶的荧光信号总体上逐渐衰减。稀释的渗透凝胶的相对荧光在第 14 天达到约 50%,而 c* 凝胶的衰减则很微弱。这些结果表明,两种凝胶的某些生物反应是不同的。使用稀释渗透凝胶的大鼠的总体结果进一步凸显了生物反应;稀释渗透凝胶与活组织的界面相连(图 4c)。这是稀释渗透凝胶所特有的,而 c* 凝胶则没有。他们通过Masson三色染色、苏木精染色和免疫染色进一步阐明了水凝胶降解和随后组织替代的生物反应(图 4d、e)。
他们证明了凝胶的亲水性和相行为会受到网络形成的影响。以前,人们认为这些特性完全由化学结构决定。PEG 水凝胶在室温下通常具有亲水性,LCST 为 130 °C,UCST 为 300 °C。然而,他们的稀释渗透 PEG 凝胶在室温下表现为疏水性,UCST 低于 90 °C。他们的研究表明,基于其化学结构,其他稀释渗透凝胶可能具有意想不到的物理特性。
稀释渗透的 PEG 凝胶具有与细胞相互作用的丝状结构,类似于生命系统中的细胞外基质。PEG 是一种细胞惰性合成聚合物,许多基于 PEG 的生物医药产品已被列入美国食品药品监督管理局的药品主档案。由于生物安全法规十分严格,使用生物安全性未知的其他合成聚合物开发生物医药产品是不可取的。因此,细胞相互作用的 PEG 凝胶可用于开发基于 PEG 的生物医学产品,如再生医学支架。
要完全理解 GGPS,有以下几个方面的挑战:(1) 特征结构的大小有四个数量级的差异,从 10 nm到 105 nm不等;(2) 结构形成所需的时间各不相同,凝胶化需要不到一个小时,完成凝胶化反应大约需要一天,而形成丝状结构则需要长达一周的时间。揭示这种涵盖广泛长度和时间尺度的现象是一项艰巨的任务。尽管存在这些障碍,但他们的研究结果表明了一种范式的转变,即渗流过程可以极大地改变凝胶的物理性质,而此前人们认为凝胶的物理性质完全由其化学结构决定。本研究探索了 PEG-水二元体系中的 GGPS,这可能会激发讨论并推动发展,尤其是在材料科学、软物质物理学和生物学领域。
文献链接:https://www.nature.com/articles/s41563-023-01712-z
