《ACS Nano》: 可喷涂热敏性凝胶用于耐药性细菌感染伤口管理
*仅供医学专业人士阅读参考
点击右上方“关注”,准时接收每日精彩内容推送。
开发有效对抗细菌感染的敷料,并同步解决伤口并发症,如出血、长期炎症和再次感染,在临床实践中极具价值。
近期,南方医科大学南方医院郑磊教授、陈金香教授和Bo Li等人构建了近红外II区(NIR-II)响应性纳米杂化物,即ILGA。该杂化物由脂质体构成,其可包封亚胺培南,并具有金壳和脂多糖(LPS)靶向适体,可用于消除细菌。得益于其精细的结构,ILGA对耐多药铜绿假单胞菌(MDR-PA)表现出强大的亲和力和可靠的光热/抗生素治疗效果。此外,通过将ILGA与热敏水凝胶聚乳酸-聚乙二醇-聚乳酸-聚乙醇酸(PLGA-PEG-PLGA)结合形成可喷涂敷料ILGA@Gel,能够实现用于伤口止血的快速按需凝胶化(10s),并提供优异的光热/抗生素功效来消毒受感染的伤口。不仅如此,ILGA@Gel可通过重塑伤口相关巨噬细胞以减轻炎症并形成凝胶层以阻断外源性细菌再次感染,提供了令人满意的伤口愈合环境。这种仿生水凝胶显示出优异的细菌根除和伤口恢复效果,证明了其在管理复杂感染伤口方面的潜力。相关工作以“NIR-II Responsive Nanohybrids Incorporating Thermosensitive Hydrogel as Sprayable Dressing for Multidrug-Resistant-Bacteria Infected Wound Management”为题发表在ACS Nano。

【文章要点】
一、ILGA
在此,作者首次构建了NIR-II响应性纳米杂化物作为有效的抗菌剂。如图1所示,作者将亚胺培南(IMP)负载于脂质体囊泡中以获得IMP@Liposome(IL)。然后,通过Au3+还原在IL的外膜上原位形成金壳,并且还进一步修饰脂多糖(LPS)适体以产生ILGA。LPS适体是一种核苷酸序列,可以形成特定的3D结构来结合LPS,从而使ILGA能够靶向细菌以提高PTT效果。在NIR-II光照射(1064nm)下,ILGA的金壳和脂质体可以破裂,释放出包封的IMP,用于协同消除细菌。此外,作者还采用生物相容性热敏水凝胶(PLGA-PEG-PLGA)作为ILGA负载的基质构建了ILGA@Gel水凝胶敷料。
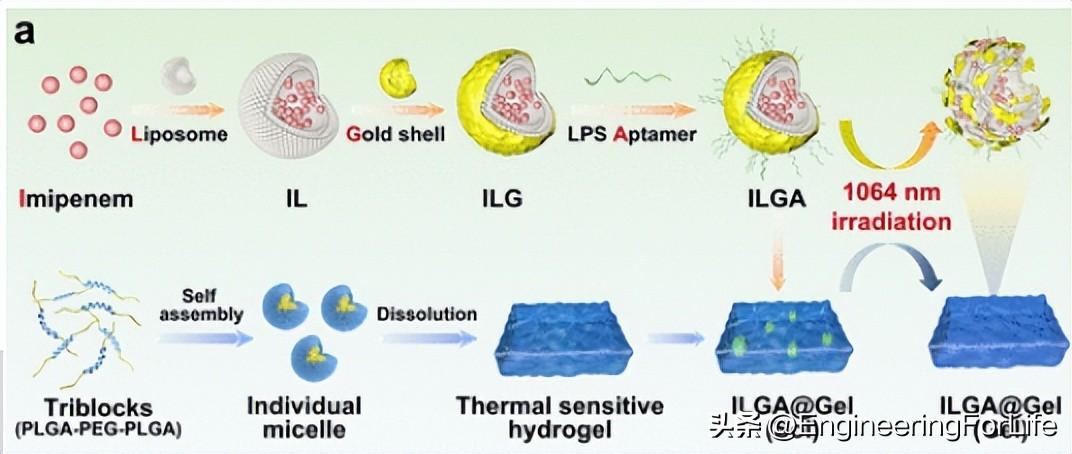
图1 材料制备与表征
二、伤口管理
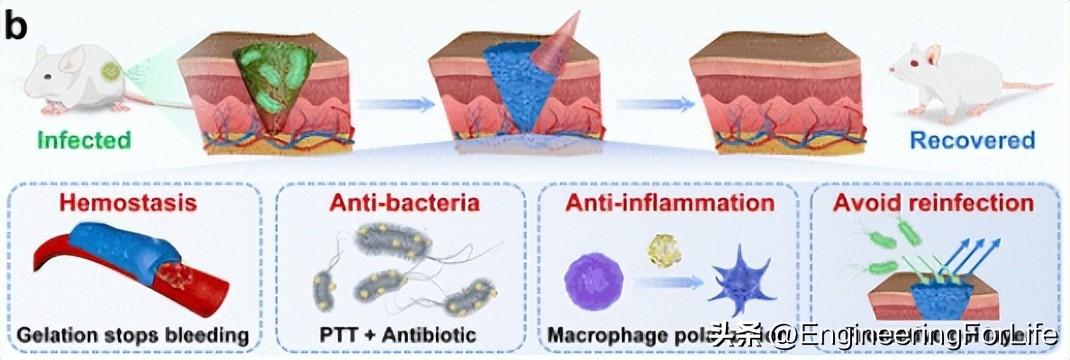
如图2所示,在典型的感染伤口管理中,可喷涂ILGA@Gel由于其良好的流动性,可以完全匹配伤口形状。随着NIR-II光的进一步照射,ILGA@Gel首先转变为粘性凝胶层来止血。同时,NIR-II光照通过PTT和IMP的协同作用触发ILGA杀死细菌。随后,在皮肤再生过程中ILGA@Gel还可以重新驯化伤口相关的巨噬细胞以减少炎症,从而加速伤口修复。此外,凝胶层起到保护屏障的作用,避免外源性细菌再次感染,同时为伤口愈合提供潮湿的微环境。因此,上述制造的ILGA@Gel不仅具有优异的抗菌作用,同时还能解决感染伤口的并发症。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.2c10742
