铁催化剂,登上Nature!
发布者:刘德桃发布时间:2023-05-01浏览次数:10

特别说明:本文由学研汇技术中心原创撰写,旨在分享相关科研知识。因学识有限,难免有所疏漏和错误,请读者批判性阅读,也恳请大方之家批评指正。挑战
CH4约占天然气的90%,是天然丰富的碳资源。利用甲烷作为C1原料合成增值化学品在化学工业中变得越来越重要。在温和的条件下,CH4选择性地转化为更复杂的碳基化合物是自然界和化学工业中最重要的转化之一。目前,CH4通常是通过蒸汽重整(高压、高温、CuO/ZnO/Al2O3催化剂)转化为CH3OH。因此,开发能够在温和条件下在水介质中进行CH4转化的高效和选择性催化体系被认为是与可持续发展相关的有价值的目标。因为CH4中的C-H键是高度惰性的,CH4选择性转化为CH3OH是最具挑战性的氧化反应之一。虽然有报道称多相催化剂可促进CH4直接氧化为CH3OH,但这些材料的转化率和选择性尚不令人满意。在生物系统中,金属酶在环境条件下催化CH4转化为CH3OH,也制备了许多金属配合物来人工催化CH4氧化为CH3OH,但使用了贵金属催化剂。在CH4催化氧化过程中抑制CH3OH过度氧化的最有希望的方法之一是使用具有底物捕集位点或靠近催化活性金属中心的疏水腔的催化剂。开发能够有效利用CH4作为天然原料的分子氧化催化剂将是有益的。新思路
基于此,日本筑波大学大学Takahiko Kojima等报道了利用含有一个N-杂环卡宾(NHC)部分的疏水SCSs的五齿形配体FeII配合物高效和选择性地催化气态烷烃氧化。通过捕获和释放机制,使气态CH4在水介质中作为疏水底物的选择性和环境友好转化成为可能。论文以《Selective methane oxidation by molecular iron catalysts in aqueous medium》题发表在Nature上。
Fe-NHC配合物的结构
FeII配合物具有通式[Fe(RPY4Cl2BIm)(CH3CN)](PF6)2 (图1a)。通过1H NMR谱和ESI-TOF-MS对低自旋FeII-NHC配合物1-AN、2-AN和3-AN进行了表征。还制备了含有BN分子的苯腈(BN)、2-BN(图1b-d)和3-BN(图1e-g)的FeII配合物,用X射线晶体学测定了Fe-C和Fe-N键的长度具有可比性,表明每种配合物第一配位球的电子相互作用几乎相同。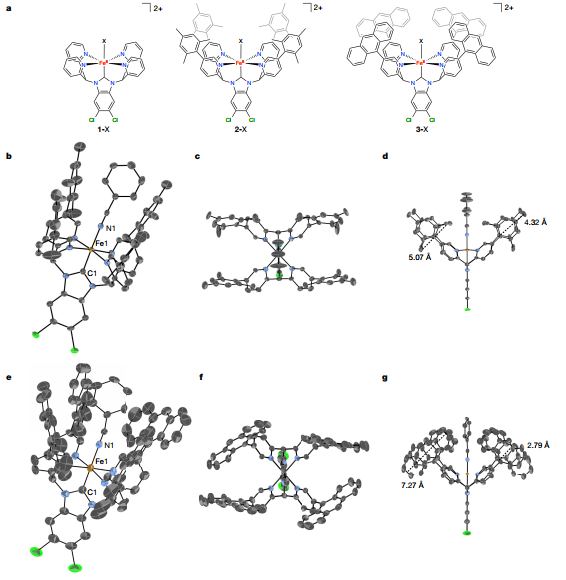
三种催化剂的TONs和醇选择性比较
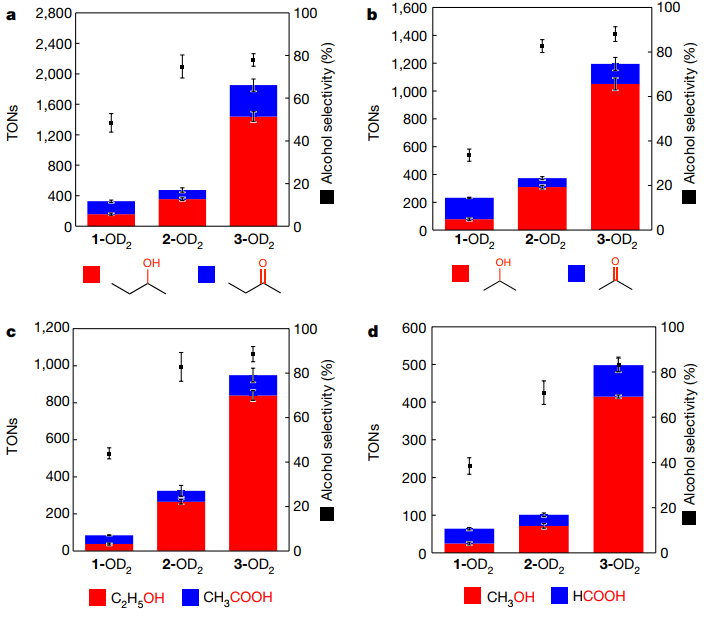
在323 K的气氛下,1-AN、2-AN或3-AN溶液(1.0 μM)为预催化剂,Na2S2O8为氧化剂,用正丁烷、丙烷、乙烷和甲烷作为气态烷烃底物进行催化氧化实验。催化氧化反应从正丁烷得到2-丁醇和2-丁酮,从丙烷得到2-丙醇和丙酮,从乙烷得到乙醇和乙酸,从甲烷得到甲醇和甲酸(表1和图2)。用1H NMR谱法测定了反应进行3 h时的催化周转量(TONs),3-OD2是最佳催化剂在3 h的CH4氧化试验中,用3-OD2获得的总吨为5.0×102和83%的CH3OH选择性,是使用分子金属配合物作为催化剂催化CH4氧化的最高值。3-OD2在323 K的4.1%的CH4转化率和83%的CH3OH选择性高于非均相催化剂。醇的氧化主要归因于Na2S2O8的存在。2-丙醇、乙醇和甲醇氧化反应得到的TON按1-OD2>2-OD2>3-OD2的顺序减少,表明疏水SCSs有效地促进了疏水底物的氧化,同时亲水氧化产物迅速释放,从而抑制了这些双电子氧化产物的过度氧化。对H218O: CH3CN中Na2S216O8催化氧化CH4反应混合物(95: 5,v/v)的GC-MS分析表明,只得到CH318OH,因此水是唯一的氧源。使用3-AN催化CH4氧化反应3 h后,发现催化剂是持久的,75%的催化剂保持了原来的结构。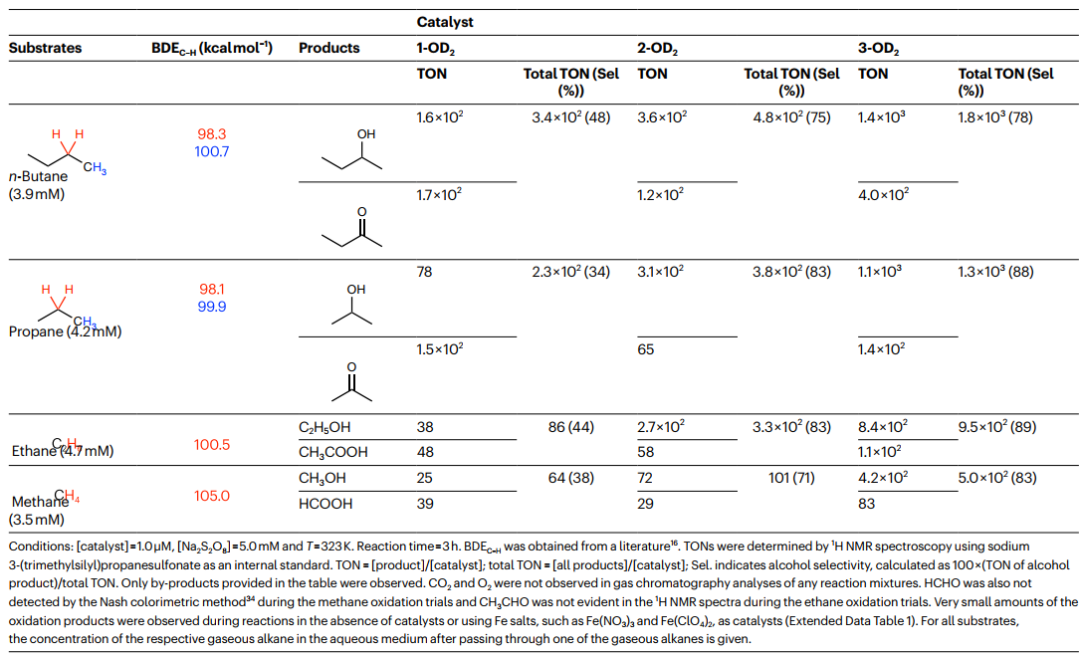
CH4氧化机理
3-OD2疏水SCSs中CH4分子的捕获是通过1H NMR滴定实验证实的,其中3-OD2添加到CH4 (0.05 mM)溶液中,D2O: CD3CN (1:1, v/v),温度298 K。δ = 0.221 ppm时,在没有3-OD2的情况下观察到CH4的1H NMR信号。随着3-OD2浓度的增加,信号上移。这表明,CH4分子由于CH π相互作用被困在3-OD2的疏水SCSs中。此外,CH4的1H NMR信号被观察到为一个单线态峰,表明在298 K时游离CH4分子与SCSs中捕获的CH4分子之间发生了快速交换。此外,使用3-OD2在D2O: CD3CN (1:1, v/v;600 μl)分析了增加3-OD2浓度后CH4 1H NMR信号化学位移的变化,以确定每个温度下的关联常数Ka,结果为3-OD2与气态烷烃在水介质中形成加合物提供了证据。进一步,研究了在323 K的H2O:CH3CN (95:5, v/v)中3-OH2催化氧化CH4的动力学以了解氧化过程。研究发现CD4的氧化速度比CH4慢,3-OH2氧化CH4时的KIE值为37。表明从CH4的C-H键中提取一个氢原子是整个过程中速率决定步骤的一个组成部分。此外,还对由3-OH2衍生的FeIV-oxo配合物进行了DFT计算解释3-O的性质。在优化的结构中,3-O的自旋密度主要集中在Fe中心(1.14)和末端氧氧配体(0.92)。氧氧配体末端的高自旋密度和Fe中心与末端氧配体之间的键序(1.5)表明3-O比典型的FeIV(O)配合物具有更大的FeIII(O·)电子结构贡献。由Fe-O键产生的较低能量拉曼散射(799 cm-1)反映了这一点。这导致CH4氧化活性的提高。综上,提出了以3-AN为预催化剂在H2O中氧化CH4的机理。如图3:第一步,3-AN的AN配体被水配体取代。3-OH2经过质子耦合电子被氧化产生相应的具有FeIII(O·)特征的FeIV(O)物种。疏水性SCS中捕获的CH4分子通过C-H键裂解氧化生成CH3OH。最后,弱结合的亲水CH3OH分子被溶剂中的H2O分子取代,并释放到水介质中再生3-OH2。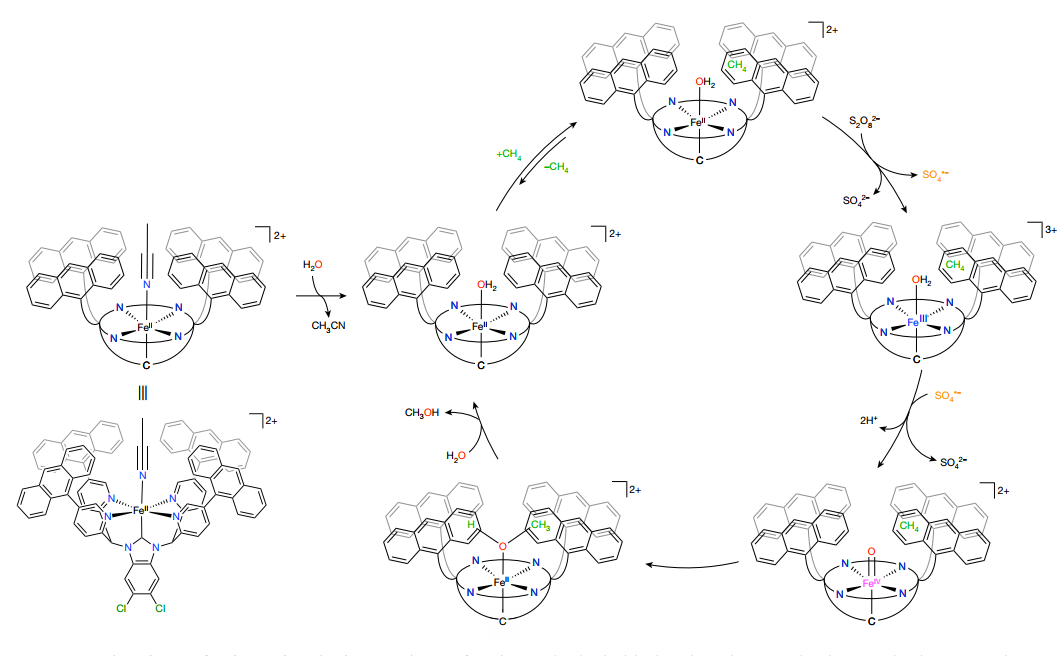
小结
研究在催化剂SCS区分疏水底物和亲水产物的基础上,对气态烷烃进行高效和选择性催化双电子氧化的方法,证明了针对天然气时捕捉-释放机制的可行性,这一策略的进一步发展可能会导致高效和选择性的催化过程,可以使用天然丰富的碳原料。https://doi.org/10.1038/s41586-023-05821-2Hiroto Fujisaki et al. Selective methane oxidation by moleculariron catalysts in aqueous medium. Nature (2023).DOI:10.1038/s41586-023-05821-2











